分子间(intermolecular)和分子内氢键(intramolecular hydrogen bonding)的区别
分子间的主要区别(main difference intermolecular) vs. 分子内氢键(intramolecular hydrogen bonding)
当同一元素或不同元素的原子**在一起共享电子并形成共价键时,分子就形成了。有两种吸引力使共价分子保持在一起。这些被称为分子间力和分子内力。分子间作用力是发生在两个分子之间的吸引力,而分子内作用力则发生在分子内部。氢键是一种特殊类型的键,由氢原子与高度负电的原子共享电子而形成。氢键既可以分子间作用力也可以分子内作用力。分子间氢键和分子内氢键的主要区别在于,分子间氢键发生在两个相邻分子之间,而分子内氢键发生在分子内部。
分别了解这两种力的作用对于理解它们是如何使分子或共价化合物保持在一起是很重要的。
这篇文章解释道,
1. What is Hydrogen Bonding? 2. What is Intermolecular Hydrogen Bonding? – Definition, Features and Properties, Examples 3. What is Intramolecular Hydrogen Bonding? – Definition, Features and Properties, Examples 4. What is the difference between Intermolecular and Intramolecular Hydrogen Bonding?
什么是氢键(hydrogen bonding)?
当中等电负性的氢共价键合到强电负性原子上时,它们共享的一对电子会更偏向于高电负性原子。这类原子的例子有N、O和F。氢键的形成必须有一个氢受体和氢供体。氢供体是分子中的高电负性原子,氢受体是相邻分子中的高电负性氢原子,应该拥有一对孤对电子。
氢键可以出现在两个分子之间或分子内部。这两种类型分别称为分子间氢键和分子内氢键。
什么是分子间氢键(intermolecular hydrogen bonding)?
分子间氢键可以发生在相似或不相似的分子之间。受主原子的位置应该适当地定向,以便它能与施主原子相互作用。
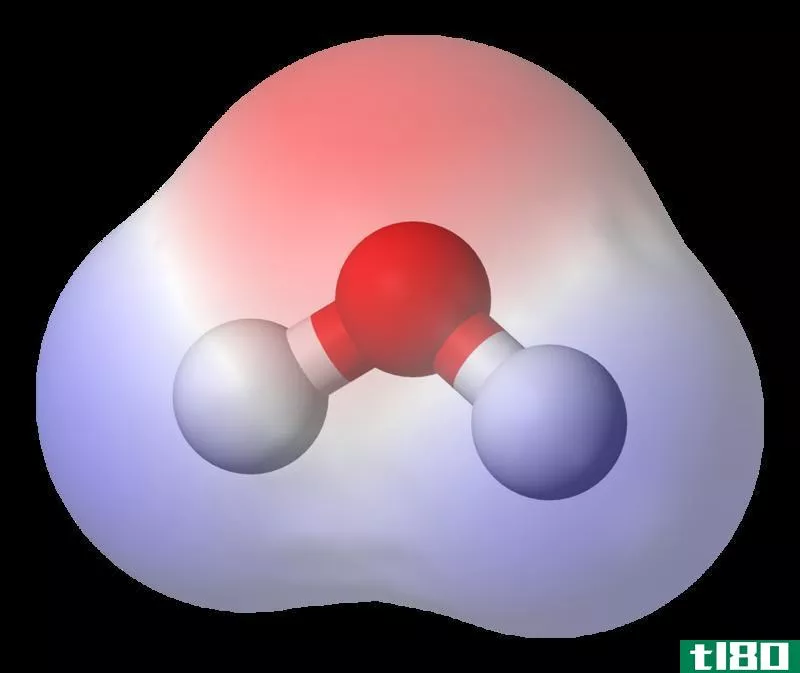
让我们看一个水分子来清楚地理解这个场景。

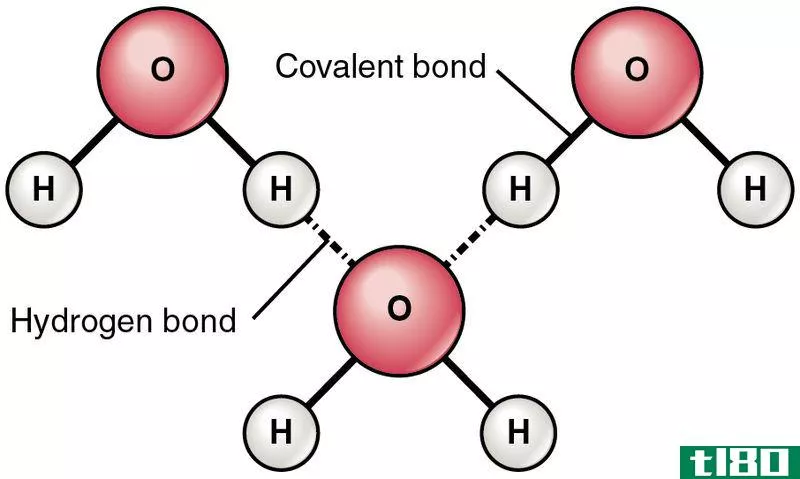
Figure 1: Hydrogen Bonding in Water Molecule
氢原子和氧原子之间共享的一对电子更容易被氧原子吸引。因此,与氢原子相比,氧原子带有轻微的负电荷。O原子被描绘成δ- 氢原子被描绘成δ+. 当第二个水分子靠近前者时,两个水分子之间形成静电键δ- 一个水分子的原子δ+ 另一个原子的氢原子。分子中的氧原子起着供体(B)和受体(A)的作用,其中一个氧原子向另一个氧原子供体氢。
由于氢键的作用,水具有非常特殊的性质。它是一种很好的溶剂,具有高沸点和高表面张力。再者,4点结冰̊C的密度比水低。因此,冰漂浮在液态水上,在冬天保护水下的水生生物。由于水的这些特性,它被称为万能溶剂,在维持地球生命方面发挥着重要作用。
什么是分子内氢键(intramolecular hydrogen bonding)?
如果一个氢键出现在同一分子的两个官能团内,则称为分子内氢键。当氢供体和受体都在同一个分子内时,就会发生这种情况。

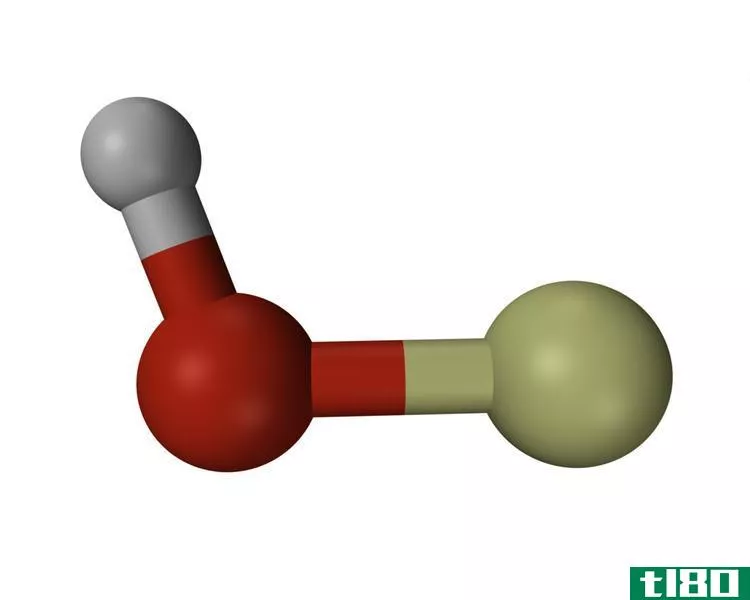
Figure 2: Structure of o-Nitrophenol (ortho-Nitrophenol) with intramolecular hydrogen bond
在邻硝基苯酚分子中,–OH基团中的O原子比H原子更负电,因此δ-. 另一方面,氢原子是δ+. 因此,-OH基团上的O原子充当H供体,而硝基上的O原子充当H受体。
分子间(intermolecular)和分子内氢键(intramolecular hydrogen bonding)的区别
键形成
分子间氢键:分子间氢键发生在两个相邻的分子之间。
分子内氢键:分子内氢键发生在分子本身。
物理性质
分子间氢键:分子间氢键具有高熔点和沸点,低蒸气压。
分子内氢键:分子内氢键具有低熔点、沸点和高蒸气压。
稳定性
分子间氢键:稳定性较高。
分子内氢键:稳定性较低。
示例
分子间氢键:水、甲醇、乙醇和糖都是分子间氢键的例子。
分子内氢键:邻硝基苯酚和水杨酸是分子内氢键的例子。
总结 - 分子间(intermolecular) vs. 分子内氢键(intramolecular hydrogen bonding)
具有分子间氢键的化合物比具有分子内氢键的化合物更稳定。分子间氢键负责将一个分子与另一个分子连接起来并使它们结合在一起。与此相反,当分子内发生氢键时,分子之间相互作用的可能性较小,分子之间粘在一起的倾向也较小。这导致沸点和熔点降低。此外,具有分子内氢键的分子相对而言更易挥发且具有更高的蒸气压。
具有分子间氢键的化合物易溶于性质相似的化合物中,而具有分子内氢键的化合物不易溶解。
参考文献:
“氢键。”化学剧本。Libretexts,2016年7月21日,网络。2017年2月7日。
“氢键:受体和捐赠者”威斯康星大学,N.D.WEB。2017年2月7日。
醇类、羧酸及其他分子的分子间及分子内氢键及其意义〉,《有机化学》。N.p.,2012年10月。网络。2017年2月7日。
“分子内氢键与分子间氢键的强度”,化学堆叠交换。N.p.,2013.网络。2017年2月7日。
Image Courtesy:
“O-Nitrophenol Wasserstoffbrücke” By NEUROtiker – Own work (Public Domain) via Comm*** Wikimedia
“210水分子之间的氢键-01”由OpenStax学院-解剖学和;生理学,连接网站(抄送3.0)通过公共维基媒体
- 发表于 2021-06-28 12:26
- 阅读 ( 371 )
- 分类:科学
你可能感兴趣的文章
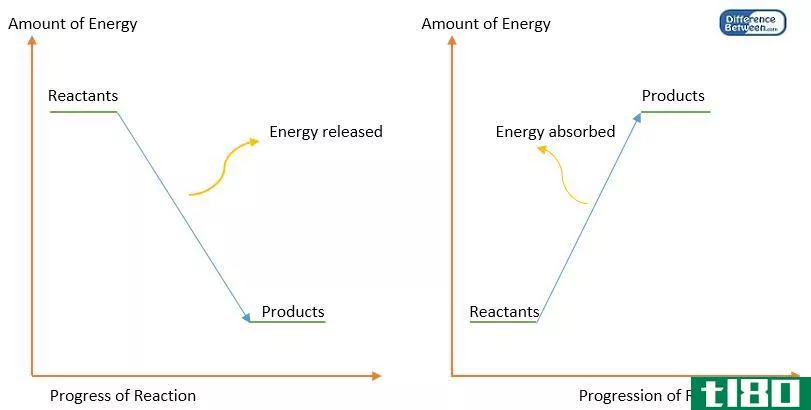
键能(bond energy)和键焓(bond enthalpy)的区别
...与键焓 键能和键焓都描述了同一个化学概念:将一摩尔分子分解成其组成原子所需的能量。它测量化学键的强度。所以也叫粘结强度。键能计算为气相化学物质在298K下的键离解能的平均值。键能和键焓这两个词之间没有很大的...
- 发布于 2020-09-24 09:39
- 阅读 ( 875 )
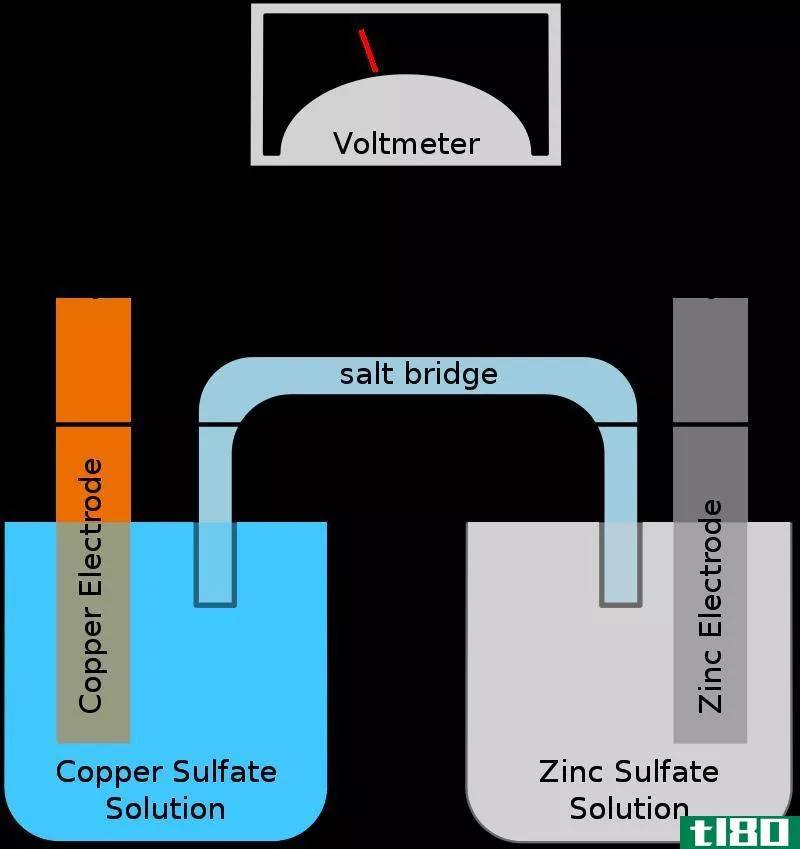
盐桥(salt bridge)和氢键(hydrogen bond)的区别
...在滤纸盐桥中,有一张滤纸浸透了电解液。 什么是氢键(hydrogen bond)? 氢键是两个不同分子的两个原子之间的一种吸引力。它是一种微弱的吸引力。但是,与其他类型的分子内作用力(如极性相互作用、非极性非极性相互作用(...
- 发布于 2020-10-14 03:27
- 阅读 ( 969 )
氢键给体(hydrogen bond donor)和接受者(acceptor)的区别
...较-氢键给体与受体的表格形式 5. 摘要 什么是氢键给体(hydrogen bond donor)? 氢键供体是含有待捐赠质子的化合物。在这里,质子是氢原子。氢键供体应该包含这些与自身共价结合的氢原子。例如,水有两个氢原子通过共价化学键...
- 发布于 2020-10-16 03:00
- 阅读 ( 1717 )
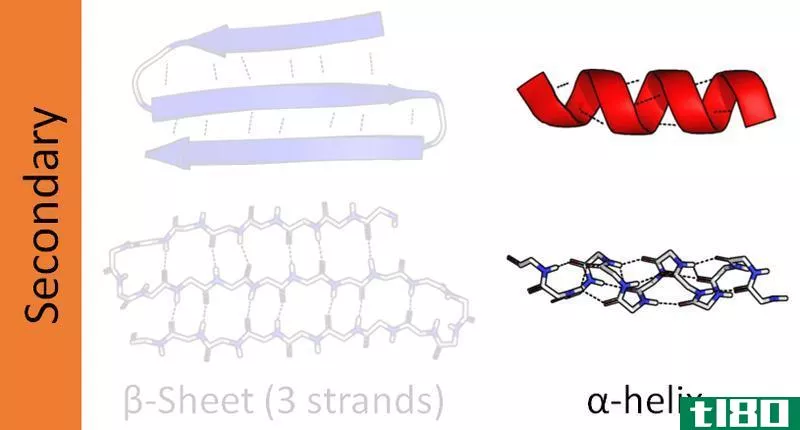
阿尔法(alpha)和β螺旋(beta helix)的区别
...决于它们在形成这些结构时形成的氢键类型。α螺旋形成分子内氢键,而β螺旋形成分子间氢键。 复杂蛋白质有四个结构层次-初级,二级,三级和四级。蛋白质的二级结构以不同的方向形成肽链。肽链由肽键结合的氨基酸序列组...
- 发布于 2020-10-17 10:48
- 阅读 ( 588 )
分子间(intermolecular)和分子内氢键(intramolecular hydrogen bonding)的区别
...氢键与分子内氢键的表格形式 5. 摘要 什么是分子间氢键(intermolecular hydrogen bonding)? 分子间氢键发生在物质中不同分子之间。因此,电子给体和电子受体应该存在于两个独立的分子中。如果有合适的电子给体和受体,任何分子都...
- 发布于 2020-10-19 06:10
- 阅读 ( 415 )
氢化(hydrogenation)和减少(reduction)的区别
... 4. 并列比较-表格形式的氢化与还原 5. 摘要 什么是氢化(hydrogenation)? 加氢是一种化学反应,包括向化学物质中添加分子氢。此外,这种反应通常在催化剂存在下发生:镍、钯、铂或它们的氧化物。它有助于减少或饱和一种化合...
- 发布于 2020-10-22 16:43
- 阅读 ( 207 )
共价(covalent)和非共价债券(noncovalent bonds)的区别
...两个原子共享一对电子时形成的一种化学键。它被称为“分子键”。当原子之间存在“共享对”或“键对”时,这些键就形成了。当原子共享电子时,由于原子间引力和斥力的稳定平衡而形成共价键。原子间共享电子使每个原子...
- 发布于 2020-10-23 12:39
- 阅读 ( 457 )
羟基(hydroxyl)和氢氧化物(hydroxide)的区别
...ucleophiles. However, they are the facilitators in the formation of strong intramolecular forces called ‘hydrogen bonds’. 什么是氢氧化物(hydroxide)? Hydroxide is a diatomic anion which contains an oxygen atom and a hydrogen atom. The bond between oxygen and hydrogen atom is covalent and...
- 发布于 2020-10-26 23:53
- 阅读 ( 338 )
氢键(hydrogen bond)和离子键(ionic bond)的区别
.... 并列比较-氢键与离子键的表格形式 5. 摘要 什么是氢键(hydrogen bond)? 当氢与氟、氧或氮等负电荷原子相连时,就会形成极性键。由于电负性,键中的电子比氢原子更容易被电负性原子吸引。因此,氢原子将得到部分正电荷,而...
- 发布于 2020-11-03 00:45
- 阅读 ( 908 )
分子内氧化还原(intramolecular redox)和不相称氧化还原反应(disproportionate redox reaction)的区别
...原反应的表格形式 5. 摘要 什么是分子内氧化还原反应(intramolecular redox reacti***)? 分子内氧化还原反应是一种涉及单一底物的化学反应,其中氧化和还原发生在同一个化学元素或两个不同的化学元素中。换句话说,在某些分子内...
- 发布于 2021-03-04 19:20
- 阅读 ( 441 )