分子内氧化还原和不相称氧化还原反应的关键区别在于,当单个分子在同一化学元素或不同化学元素中发生氧化还原反应时,就会发生分子内氧化还原反应,而不相称氧化还原反应则涉及同一化学元素的氧化还原反应单个基板中的元素。
分子内氧化还原反应和不相称氧化还原反应是氧化还原反应平行发生的两类无机化学反应。这两种化学反应都涉及发生在同一化合物/单一底物分子中的氧化和还原半反应。根据发生这些半反应的化学元素的不同,这两种类型是不同的。
目录
1. 概述和主要区别
2. 什么是分子内氧化还原反应
3. 什么是不相称的氧化还原反应
4. 并列比较-分子内氧化还原与不相称氧化还原反应的表格形式
5. 摘要
什么是分子内氧化还原反应(intramolecular redox reacti***)?
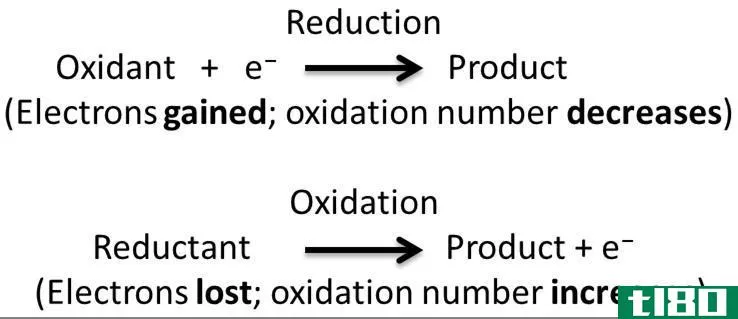
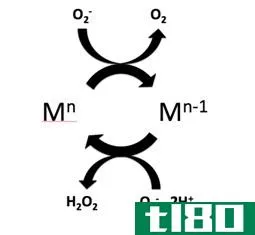
分子内氧化还原反应是一种涉及单一底物的化学反应,其中氧化和还原发生在同一个化学元素或两个不同的化学元素中。换句话说,在某些分子内氧化还原反应中,氧化和还原发生在同一化学元素中,而在其他分子内氧化还原反应中,氧化和还原发生在同一分子中的两种不同化学元素中。如果氧化和还原发生在同一个化学元素中,我们称之为歧化。
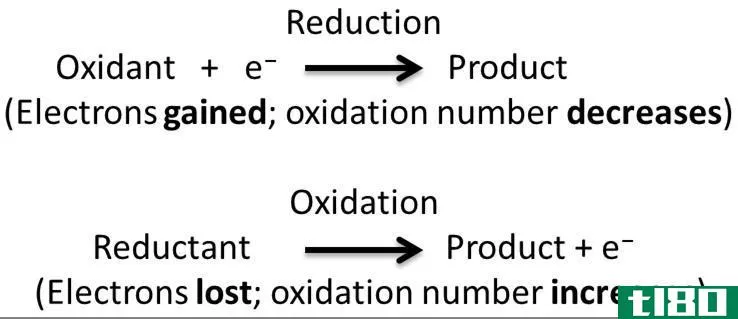
图01:氧化还原反应的化学过程
什么是不相称的氧化还原反应(disproportionate redox reacti***)?
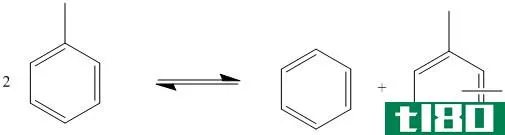
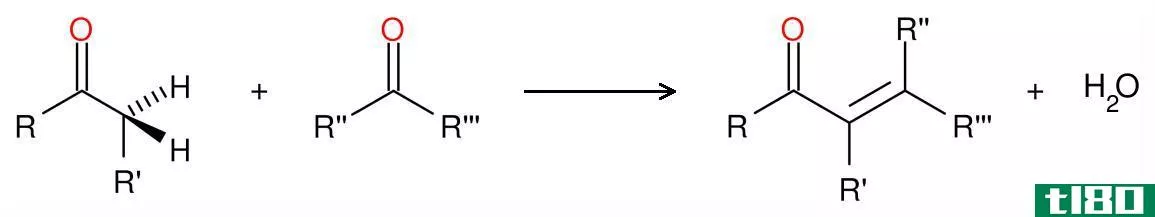
不相称的氧化还原反应是氧化和还原发生在单一底物分子的同一化学元素中的化学反应。在这类反应中,一个底物分子同时起氧化和还原半反应的作用。在这里,分子的一部分经历氧化而另一部分经历还原;然而,这两个分子部分都涉及发生氧化或还原的相同化学元素。示例如下:
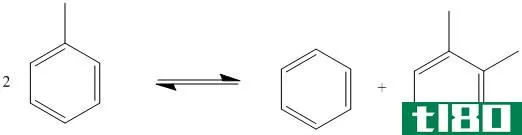
图02:不成比例的氧化还原反应示例
这种化学反应的另一个常见例子是过氧化氢分子中氧原子的歧化。在这里,过氧化氢分子中的氧经过氧化形成氧气,同一分子经过还原形成水分子。
分子内氧化还原(intramolecular redox)和不相称氧化还原反应(disproportionate redox reaction)的区别
氧化还原反应是氧化半反应和还原半反应平行发生的化学反应。分子内氧化还原和不相称氧化还原反应的关键区别在于,当两种不同物质的分子相互反应时,分子内氧化还原反应发生,而不相称氧化还原反应涉及单个分子的氧化和还原。
通过还原使C6H2(NO2)3CH3歧化形成N2,通过氧化使C歧化是分子内氧化还原反应的示例,而过氧化氢分子中氧原子歧化是不相称氧化还原反应的示例。
下面的信息图表以表格形式总结了分子内氧化还原和不相称氧化还原反应之间的差异,以便进行并列比较。

总结 - 分子内氧化还原(intramolecular redox) vs. 不相称氧化还原反应(disproportionate redox reaction)
氧化还原反应是一种化学反应,包括平行发生的氧化和还原反应。分子内氧化还原和不相称氧化还原反应的关键区别在于,当两种不同物质的分子相互反应时,分子内氧化还原反应发生,而不相称氧化还原反应涉及单个分子的氧化和还原。