歧化和氧化还原的关键区别在于,在歧化反应中,同一反应物经历氧化和还原。氧化和氧化反应通常会发生两种不同的氧化还原反应。
此外,歧化反应是一个分子转化为两个或两个以上不同产物的化学反应,而氧化还原反应是氧化和还原半反应同时发生的一种化学反应。最重要的是,歧化是一种氧化还原反应,因为有两个同时发生的氧化和还原反应。
目录
1. 概述和主要区别
2. 什么是不成比例
3. 什么是氧化还原
4. 并列比较-表格式的歧化与氧化还原
5. 摘要
什么是歧化(disproportionation)?
歧化是一种化学反应,其中一个分子转化成两个或两个以上不同的产物。基本上,它是一种氧化还原反应,同一分子同时经历氧化和还原。此外,这种反应的反作用称为混合反应。这些反应的一般形式如下:
2A⟶A’+A”
此外,这类反应的一些常见例子如下
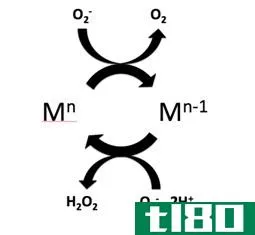
- 过氧化氢转化为水和氧
2H2O2⟶H2O+O2
- 氯化汞的歧化反应
Hg2Cl2→Hg+HgCl2
- 磷酸歧化制备磷酸和磷化氢
4 H**O3→3 H**O4+PH3
- 溴氟化物歧化生成三氟化溴和溴
3 BrF→BrF3+Br2
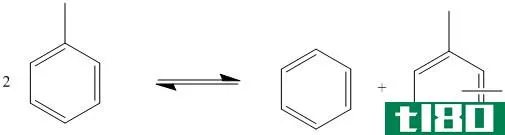
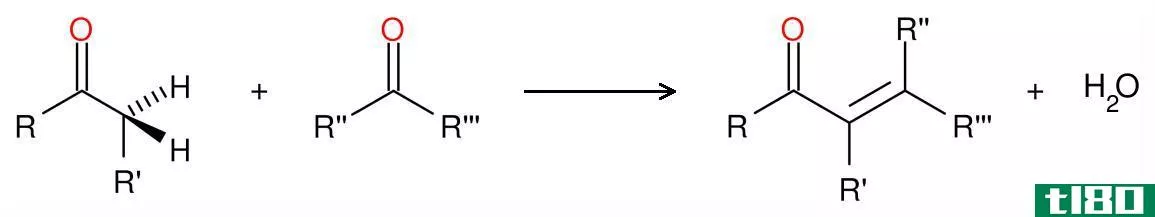
图01:甲苯歧化
什么是氧化还原(redox)?
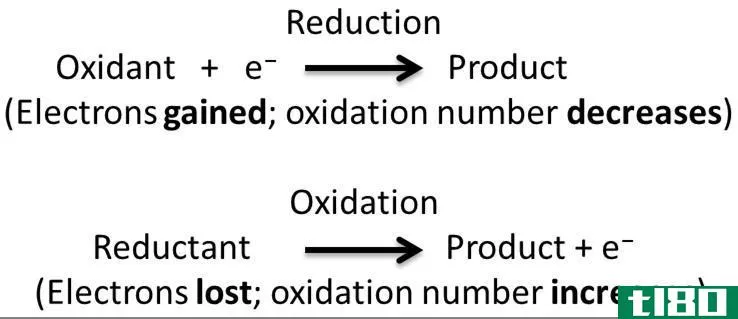
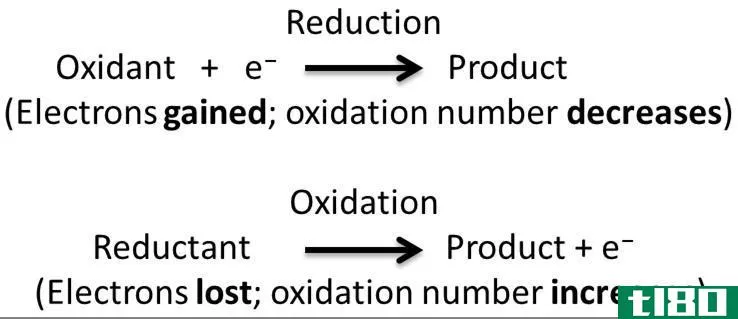
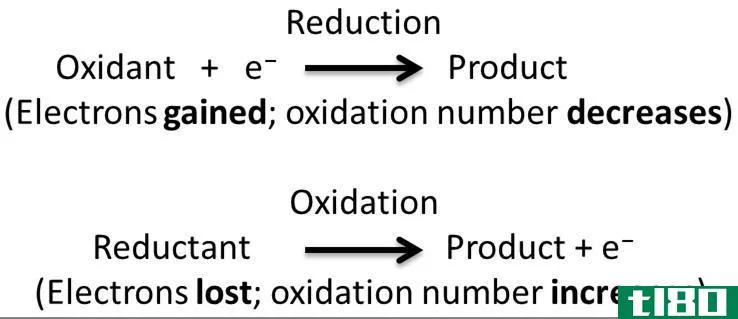
氧化还原反应是氧化和还原半反应同时发生的一种化学反应。此外,在这个反应中,我们认为氧化和还原是互补的过程。这里,氧化是电子的损失或氧化状态的增加,而还原是电子的增加或氧化状态的减少。

图02:生锈
此外,氧化还原反应的速率可以从非常慢的过程(如生锈)到快速的过程(如燃料燃烧)的变化。
歧化(disproportionation)和氧化还原(redox)的区别
歧化和氧化还原的关键区别在于,在歧化反应中,同一反应物经历氧化和还原,而在氧化还原反应中,两种不同的反应物通常经历氧化和还原。考虑到一些例子,歧化包括汞(I)氯化物歧化形成汞和汞(II)氯化物,溴氟化物歧化形成三氟化溴和溴等,而生锈、燃烧、燃料燃烧等是氧化还原反应的例子。
下面的信息图总结了歧化和氧化还原之间的区别。

总结 - 歧化(disproportionation) vs. 氧化还原(redox)
歧化反应是一个分子转化为两个或两个以上不同产物的化学反应,而氧化还原反应是氧化和还原半反应同时发生的一种化学反应。歧化和氧化还原的关键区别在于,在歧化反应中,同一反应物经历氧化和还原,而在氧化还原反应中,通常两种不同的反应物进行氧化和还原。
引用
1赫尔曼斯汀,安妮·玛丽。“化学中的歧化定义”,ThoughtCo,2019年8月6日,可在这里查阅。