复分解反应和氧化还原反应的关键区别在于,在复分解反应中,两个分子之间发生两种离子交换,而在氧化还原反应中,两种化学物质之间发生电子交换。
元分解和氧化还原反应是两种化学反应。但它们有不同的行动机制。元分解是一个单步反应,而氧化还原反应具有两个平行的半反应,电子交换过程需要。
目录
1. 概述和主要区别
2. 什么是复分解
3. 什么是氧化还原反应
4. 复分解反应和氧化还原反应的相似性
5. 并列比较-表格式的置换反应与氧化还原反应
6. 摘要
什么是复分解(metathesis)?
复分解或双置换反应是两个分子之间发生两种离子交换的化学反应。通式如下:
A-B+C-D⟶A-C+B-D
在这个反应中断裂和形成的键可以是离子键,也可以是共价键。这类反应包括沉淀反应、酸碱反应、烷基化反应等。
在上面的方程中,每种反应物的A和C组分都发生了位置转换。通常,这些反应发生在水溶液中。此外,我们可以将这些反应分类如下:;
- 沉淀反应-沉淀在反应结束时形成。例如,硝酸银和氯化钠的反应形成氯化银沉淀和硝酸钠水溶液。
- 中和反应-酸在与碱的反应中中和。例如,HCl溶液(酸)可从NaOH溶液(碱)中和。图01:双置换反应示例
什么是氧化还原反应(redox reaction)?
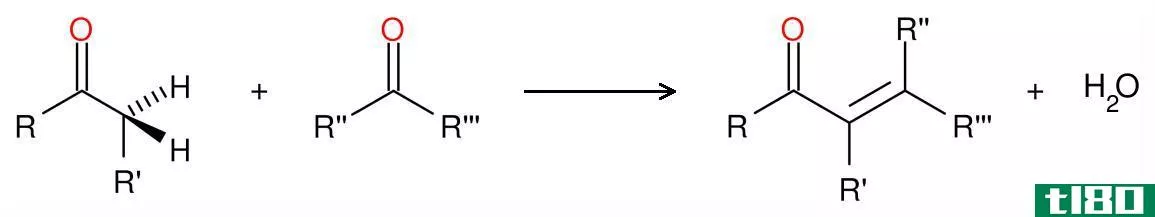
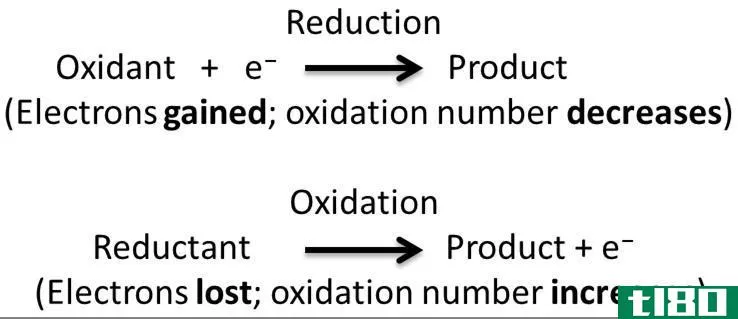
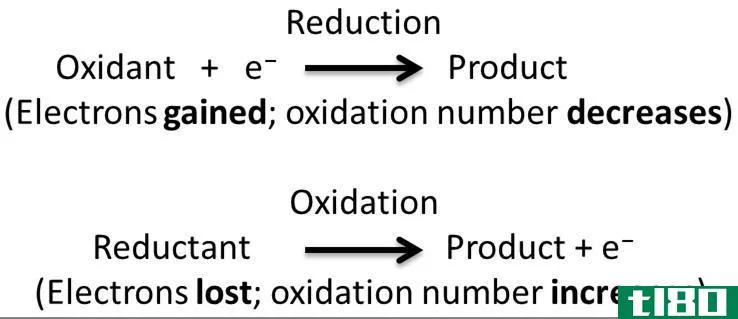
氧化还原反应是氧化和还原半反应同时发生的一种化学反应。在这个反应中,我们认为氧化和还原是互补的过程。这里,氧化是电子的损失或氧化状态的增加,而还原是电子的增加或氧化状态的减少。
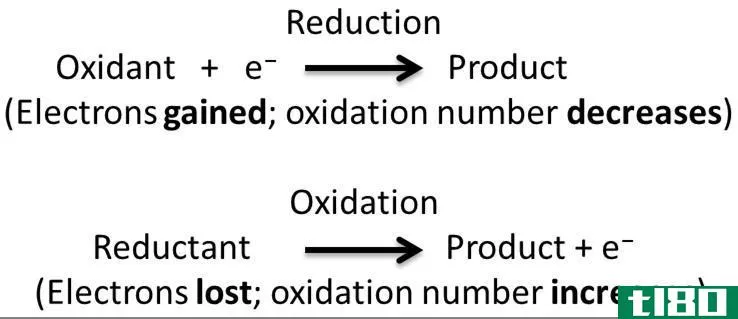
图02:氧化和还原反应的机理
此外,氧化还原反应的速率可以从非常慢的过程(如生锈)到快速的过程(如燃料燃烧)的变化。
复分解(metathesis)和氧化还原反应(redox reacti***)的共同点
- 复分解反应和氧化还原反应是产物与反应物完全不同的化学反应。
- 这两种反应都涉及到反应物之间的某种物质的交换以得到产物。e、 电子交换,化学部分。
- 这些反应包括两个互补反应。E、 氧化还原反应中的氧化还原反应,复分解反应中的破键成键反应。
复分解(metathesis)和氧化还原反应(redox reacti***)的区别
复分解反应和氧化还原反应是两种类型的化学反应。复分解反应和氧化还原反应的关键区别在于,在复分解反应中,两个分子之间发生两种离子交换,而在氧化还原反应中,两种化学物质之间发生电子交换。双置换反应或复分解是一个单步反应,但氧化还原反应有两个平行的半反应需要电子交换过程。此外,在氧化还原反应中,原子的氧化状态必然发生变化,但在复分解反应中,它可能改变,也可能不改变。
下面的信息图总结了置换反应和氧化还原反应之间的区别。

总结 - 复分解(metathesis) vs. 氧化还原反应(redox reacti***)
复分解反应和氧化还原反应是两种类型的化学反应。复分解反应和氧化还原反应的关键区别在于,在复分解反应中,两个分子之间发生两种离子交换,而在氧化还原反应中,两种化学物质之间发生电子交换。此外,复分解是一个单步反应,而氧化还原反应有两个平行的半反应需要电子交换过程。
引用
1“置换反应”,化学剧本,剧本,2019年6月5日,可在这里查阅。“氧化还原反应”,化学剧本,歌词,2019年6月5日,可在这里查阅。
2“氧化还原反应”,化学剧本,歌词,2019年6月5日,