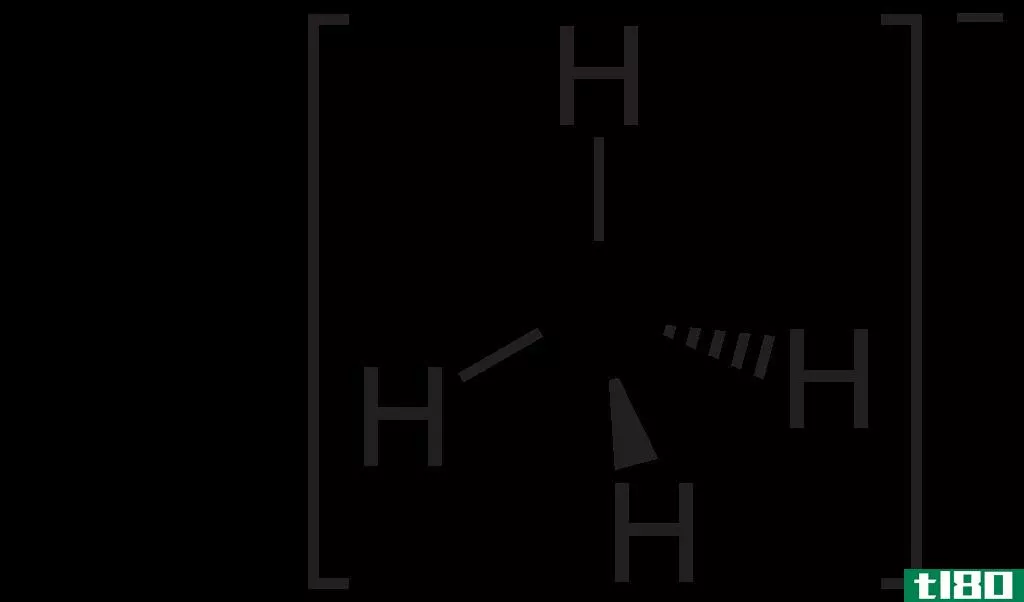
氧化还原反应和非氧化还原反应的关键区别在于,在氧化还原反应中,某些化学元素的氧化状态会从一种状态改变到另一种状态,而在非氧化还原反应中,化学元素的氧化状态不会改变。
氧化还原和非氧化还原反应是两种主要的化学反应。这两个基团的区别取决于反应物所用化学元素氧化状态的变化。
目录
1. 概述和主要区别
2. 什么是氧化还原反应
3. 什么是不可逆反应
4. 并列比较-氧化还原与非氧化还原反应的表格形式
5. 摘要
什么是氧化还原反应(redox reacti***)?
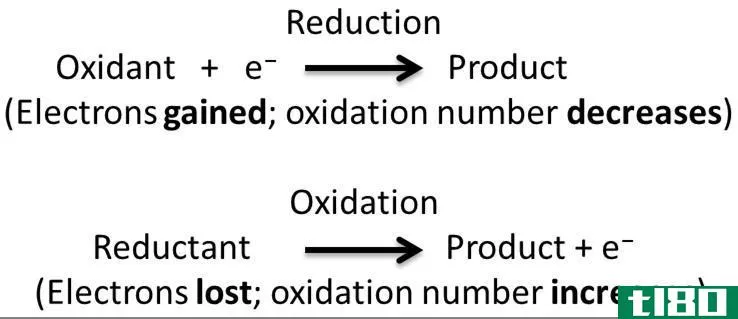
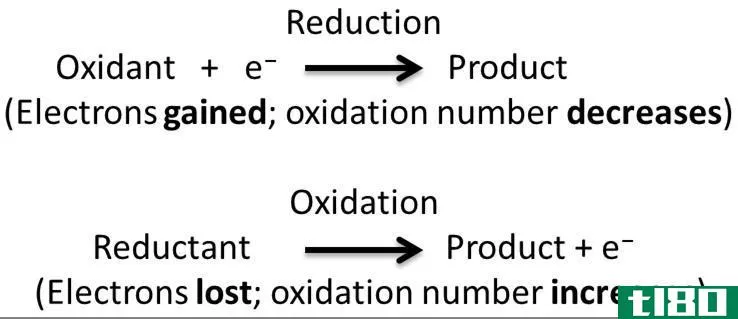
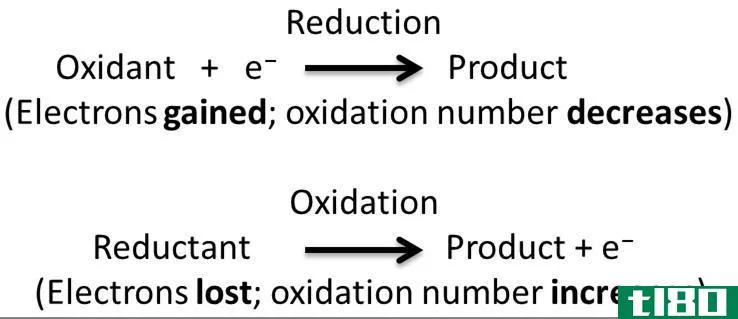
氧化还原反应是氧化和还原半反应同时发生的一种化学反应。在这个反应中,我们认为氧化和还原是互补的过程。这里,氧化是电子的损失或氧化状态的增加,而还原是电子的增加或氧化状态的减少。术语“氧化还原”是还原-氧化过程的缩写。
在氧化还原反应中,经历还原的化合物/反应物称为氧化剂,而经历氧化的化合物称为还原剂。这是因为氧化剂使另一种化合物氧化,反之亦然。
在氧化还原反应中,实际发生的是电子通过半反应在两个反应物之间转移。通过观察化学元素的氧化状态,我们可以很容易地识别这种电子转移。在电子转移过程中,由于电子在原子中留下不平衡的质子而失去电子时,氧化态增加;由于电子是亚原子粒子的负电荷而获得电子时,氧化态减少。氧化还原反应有多种类型,如分解反应、结合反应、置换反应和歧化反应。
什么是非还原反应(nonredox reacti***)?
非氧化还原反应是化学元素的氧化状态没有变化的化学反应。因此,这些化学反应不像氧化还原反应那样具有半氧化半还原反应。换言之,在化学反应的进行过程中会发生电子转移。

图02:NaOH和HCl中和反应
非氧化还原反应的常见例子包括中和反应和双置换反应。
氧化还原(redox)和非还原反应(nonredox reacti***)的区别
氧化还原和非氧化还原反应是两种不同类型的化学反应。氧化还原反应和非氧化还原反应的关键区别在于,在氧化还原反应中,某些化学元素的氧化状态会从一种状态改变到另一种状态,而在非氧化还原反应中,化学元素的氧化状态不会改变。此外,氧化还原反应有氧化半反应和还原半反应,而非氧化还原反应中没有特殊的半反应。分解反应、置换反应、歧化反应等是氧化还原反应的例子,而中和反应、双置换反应等是非氧化还原反应的例子。
下面的信息图表列出了氧化还原和非氧化还原反应之间的差异。

总结 - 氧化还原(redox) vs. 非还原反应(nonredox reacti***)
氧化还原和非氧化还原反应是两种不同类型的化学反应。氧化还原反应和非氧化还原反应的关键区别在于,在氧化还原反应中,某些化学元素的氧化状态会从一种状态改变到另一种状态,而在非氧化还原反应中,化学元素的氧化状态不会改变。
引用
1“氧化还原反应”,《化学文集》,文集,2020年8月15日,可在此查阅。