极地的(polar)和非极性键(nonpolar bonds)的区别
主要差异极性(main difference polar) vs. 非极性键(nonpolar bonds)
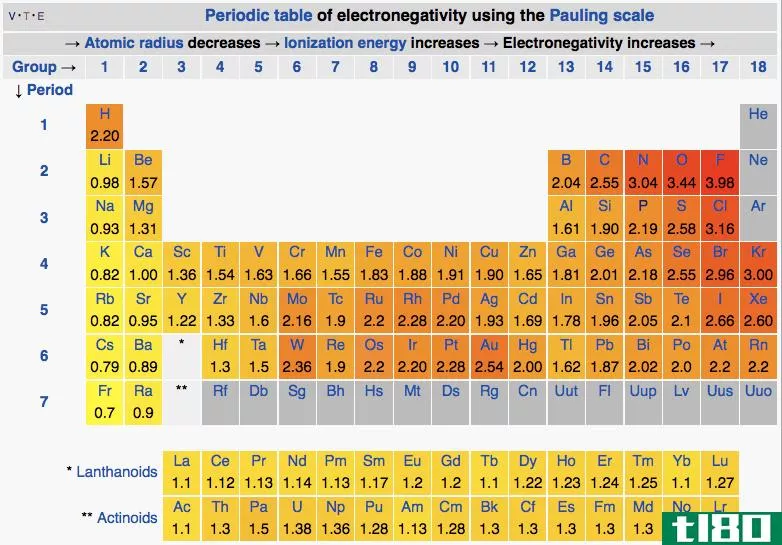
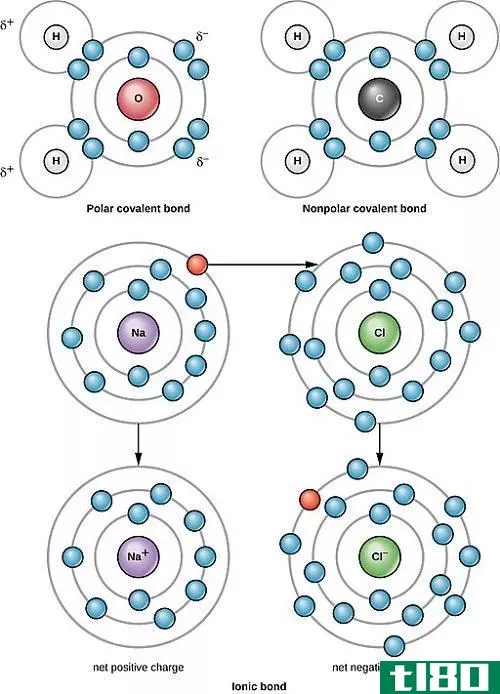
极性键和非极性键都是原子间的两种共价键。在共价键合中,电子在两种原子之间共享,而不是完全的电子的送出或接受。然而,根据所涉及的原子类型,共享的一对电子不会一直驻留在键的中心。有些元素对电子的亲和力比其他元素高。因此,键内的电子倾向于被对电子有较高亲和力的元素吸引。结果,键在电子位置上表现出不平衡。这种现象叫做“极性”。表现出这种性质的键是极性键,电子位于中心而不偏向键两边的键称为非极性键。因此,极性键和非极性键的主要区别在于极性键发生在具有不同电负性的元素之间,而非极性键发生在具有相同电负性的元素之间。
什么是极性键(polar bonds)?
极性键是一种共价键,当两种元素的电负性不同时,它们之间会发生共价键。电负性是指对电子的亲和性。电负性高的原子比电负性低的原子更容易吸引电子。氟是电负性最强的元素。
当两个原子之间形成共价键时,电子在它们之间共享,这些共享的电子通常位于键中两个原子之间的空间中。这多少有点像电子云。因此,当一种元素比另一种元素更容易吸引电子时,电子云的密度就会向电子亲和性更高的元素移动。从而使电子分布发生畸变。
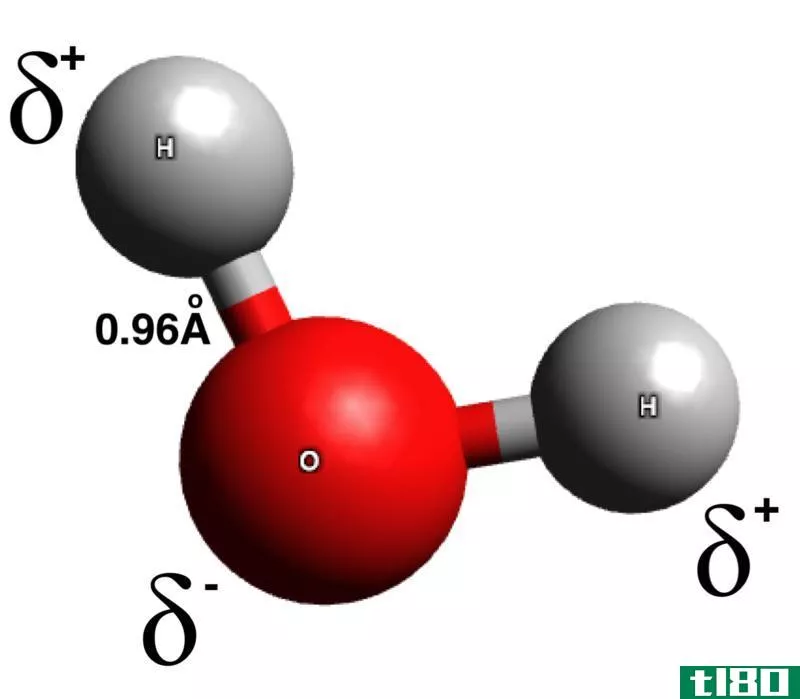
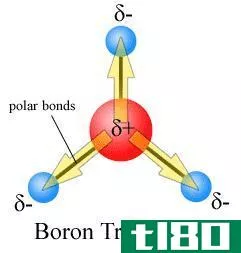
结果,在键的任何一角都有一个轻电荷,在电负性高的一端有一个负电荷,在另一端分别有一个互补的正电荷。这些极化键能够形成强大的分子间相互作用,如“H键”。据说,极化键中含有一个“偶极矩”,键中的每个元素称为“偶极子”。然而,并不是所有情况下,极化键都会导致极性化合物的形成。这取决于原子内键的取向。如果偶极力被抵消了,那么即使化合物有极性键,化合物本身也不会被称为极性化合物。
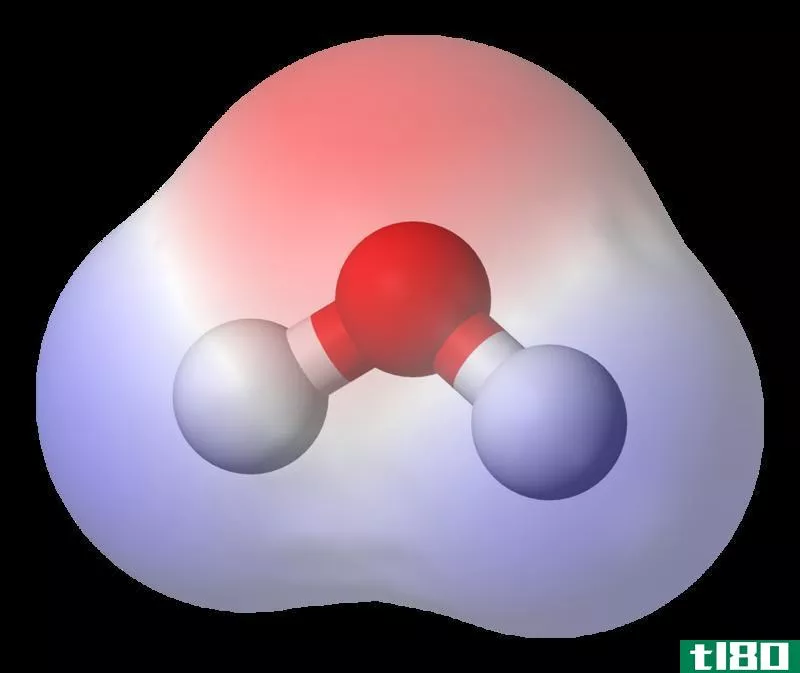
Water molecule (negative charge is shaded in red.)
什么是非极性键(non-polar bonds)?
当两种元素的电负性相同时,它们之间会形成共价键。因此,通常当参与键的原子相似时,就会产生非极性键。这类化合物被称为“双原子化合物”。在这种情况下,共享的电子倾向于驻留在键合平面的中心,保持平衡/集中的电子云。因此,云中看不到任何扭曲。
两极也没有电荷积聚,键保持中性。然而,由于电子云的瞬时运动,极性有可能发生瞬时变化,这些变化引起非极性化合物之间的分子间吸引,如范德华相互作用。一般来说,所有含有非极性键的化合物都是非极性化合物。
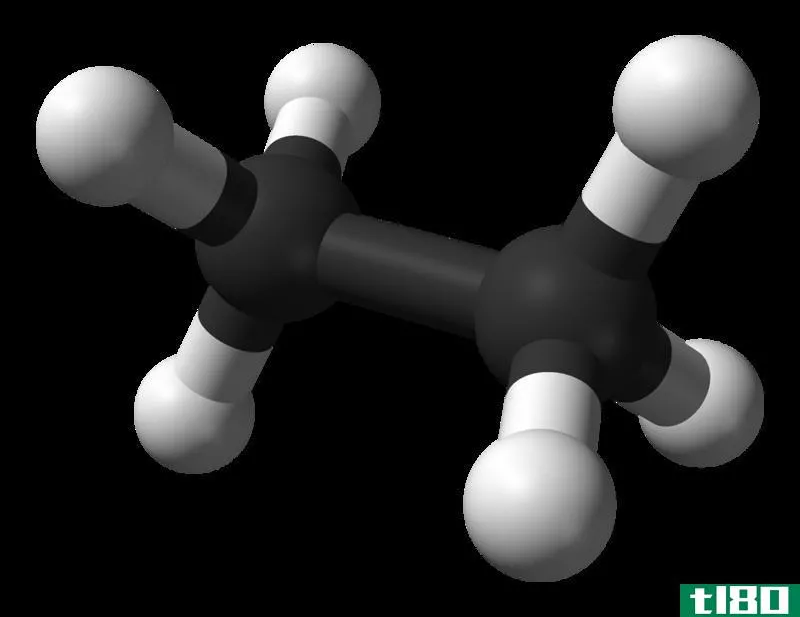
Ethane
极地的(polar)和非极性键(nonpolar bonds)的区别
定义
极性键是具有不同电负性的元素之间的共价键。
非极性键是具有相同电负性的元素之间的共价键,换句话说,是相似原子之间的共价键。
电子云的性质
极性键的电子云是扭曲的。
非极性键的电子云没有扭曲。
带电极
极性键的极性上有电荷积聚。
非极性键没有这样的电荷积累。
偶极矩
极性键有一个偶极矩。
非极性键没有偶极矩。
分子间相互作用
氢键发生在极性键的带电极之间。
Van der Waal interacti*** are commonly seen between non-polar compounds.
Image Courtesy:
“Water-elpot-transparent-3D-balls”. (Public Domain) via Comm***
“伊桑三维球”由本米尔斯-自己的工作(公共域)通过Wikimedia Comm***
- 发表于 2021-06-27 10:16
- 阅读 ( 403 )
- 分类:科学
你可能感兴趣的文章
极地的(polar)和偶极分子(dipolar molecules)的区别
...。一些例子包括羰基氧化物、重氮甲烷、膦叶立德等。 极地的(polar)和偶极分子(dipolar molecules)的区别 极性分子和偶极分子的关键区别在于,极性分子有两个相反的两端,带着相反的电荷,而极性分子有两个极性。然而,一般来...
- 发布于 2020-09-24 05:10
- 阅读 ( 532 )
键偶极子(bond dipole)和分子偶极子(molecular dipole)的区别
...区别在于,键偶极子是指在一个特定的化学键中产生两个极性端。而分子偶极子是指在一种特定化合物中产生两个极性末端。 键偶极子和分子偶极子是决定化合物的化学和物理性质的重要术语。偶极子是指在同一化学键或化合...
- 发布于 2020-10-01 16:53
- 阅读 ( 1020 )
极地的(polar)和非极性溶剂(nonpolar solvents)的区别
...,极性非质子溶剂不能提供氢原子。 什么是非极性溶剂(nonpolar solvents)? 非极性溶剂是没有偶极矩的液体。因此,这些溶剂不含部分正电荷或负电荷。由于这个原因,这些溶剂不能溶解极性化合物,因为没有相反的电荷来吸引极...
- 发布于 2020-10-12 14:40
- 阅读 ( 493 )
盐桥(salt bridge)和氢键(hydrogen bond)的区别
...种微弱的吸引力。但是,与其他类型的分子内作用力(如极性相互作用、非极性非极性相互作用(如范德瓦尔力)相比,氢键的强度更大。 Usually, hydrogen bonds form between polar covalent molecules. These molecules contain polar covalent bonds, which f...
- 发布于 2020-10-14 03:27
- 阅读 ( 971 )
共价键(covalent bond)和与格键(dative bond)的区别
...原子之间共价键的形成 共价键主要有两种类型:极性键和非极性键。两个原子之间存在极性键,它们的电负性值相差在0.4到1.7之间。如果这个差值小于0.4,就会形成非极性键。这是因为,电负性值之间的高差异意味着,一个原...
- 发布于 2020-10-17 17:57
- 阅读 ( 845 )
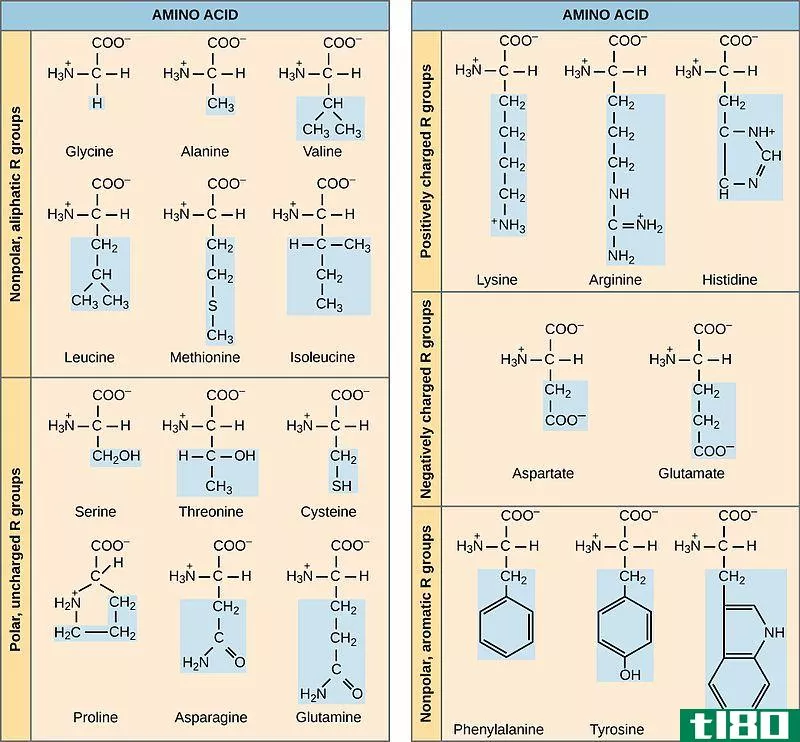
极地的(polar)和非极性氨基酸(nonpolar amino acids)的区别
...类的例子包括天冬氨酸和谷氨酸。 什么是非极性氨基酸(nonpolar amino acids)? 非极性氨基酸是没有极性的氨基酸。这是因为这些氨基酸的羧基和胺基数目相等。这使得这些非极性氨基酸具有中性电荷。他们对“R”组没有收费。 非...
- 发布于 2020-10-19 04:50
- 阅读 ( 1158 )
电负性(electronegativity)和极性(polarity)的区别
电负性和极性的关键区别在于,电负性是原子吸引键中电子的倾向,而极性意味着电荷的分离。 极性是由于电负性的不同而产生的。因此,这两个术语是密切相关的术语。然而,电负性和极性之间有明显的区别。电负性和极...
- 发布于 2020-10-22 10:07
- 阅读 ( 892 )
共价(covalent)和非共价债券(noncovalent bonds)的区别
共价键和非共价键的关键区别在于,当两个原子共享它们的电子时,共价键就形成了,而非共价键则是通过两个原子之间完全交换电子或不交换任何电子而形成的。 化学键主要有四种类型:共价键、离子键、氢键和范德华相...
- 发布于 2020-10-23 12:39
- 阅读 ( 459 )
极地的(polar)和非极性(non-polar)的区别
极性与非极性 当我们第一次了解化学时,我们大多数人都觉得它有趣而令人兴奋。但是当你只研究化学性质,化学键,元素表等等的时候,你会觉得很无聊。我们在记忆不同的属性,不同的过程,以及更多的东西时会感到沮丧...
- 发布于 2021-06-23 19:30
- 阅读 ( 397 )
非极性(non-polar)和极性共价键(polar covalent bonds)的区别
...类,也属于共价键的两类。所有这三种类型(离子、极性和非极性)都被归类为化学键,其中有一种力(电负性)允许两种特定元素的原子相互吸引。可能的共价键的数目由特定元素的电子外壳中空位的数目决定。 出于某种考...
- 发布于 2021-06-24 05:05
- 阅读 ( 608 )