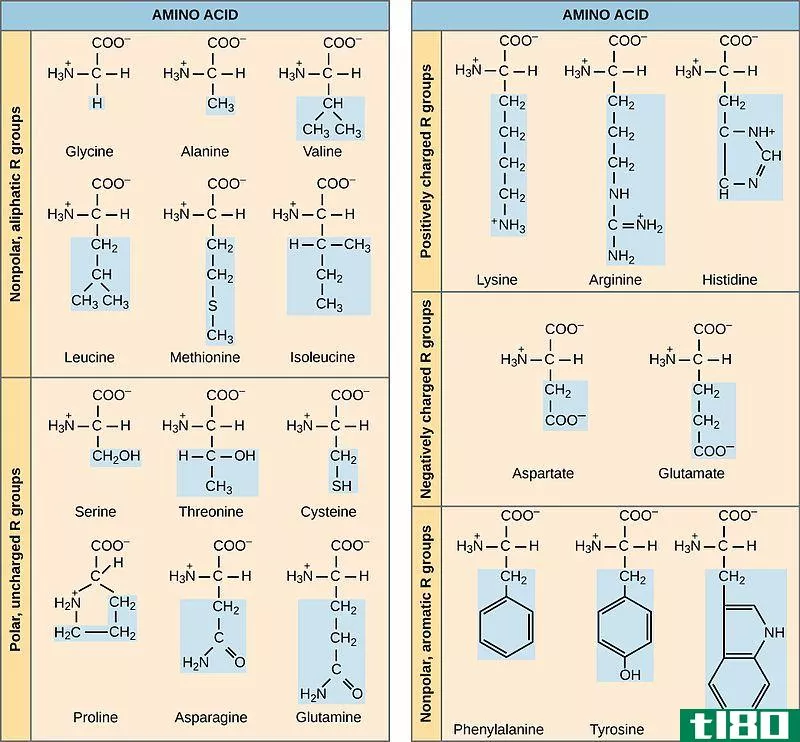
极地的(polar)和非极性分子(nonpolar molecules)的区别
主要差异极性(main difference polar) vs. 非极性分子(nonpolar molecules)
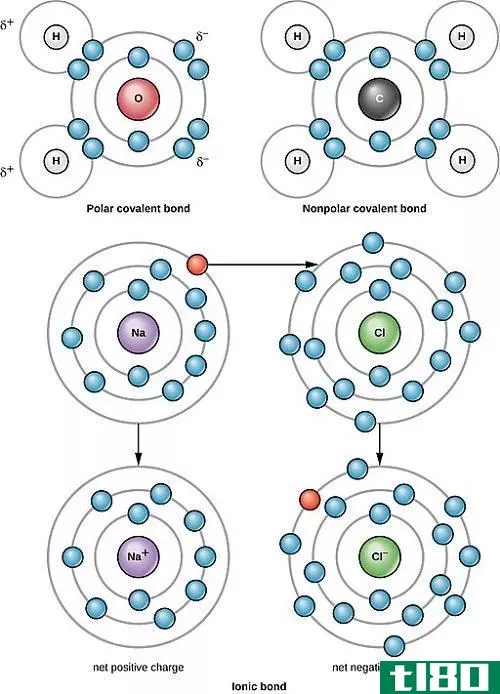
不同或相同元素的原子聚在一起形成分子。由两个原子共用一对电子形成的键称为“共价键”。不同的原子对电子有不同程度的吸引力。它们把电子拉向它们的能力叫做电负性。与C、P、S等原子相比,F、Cl、O等原子表现出更大的电负性。当两个原子;电负性差键合形成极性分子。如果原子间的电负性差为<;0.4分子变成非极性。极性分子和非极性分子的主要区别是净偶极矩。在极性分子的原子上形成净偶极矩,而在非极性分子上不形成。
这篇文章解释道,
1.什么是极性分子-定义、形成、性质、示例
2.什么是非极性分子-定义、形成、性质、示例
3. What is the difference between Polar and Nonpolar Molecules
什么是极性分子(polar molecules)?
极性分子的形成要么是由于电负性原子,要么是由于非极性键和同一分子上的孤对电子的不对称排列。下面的例子将更详细地解释这两种现象。
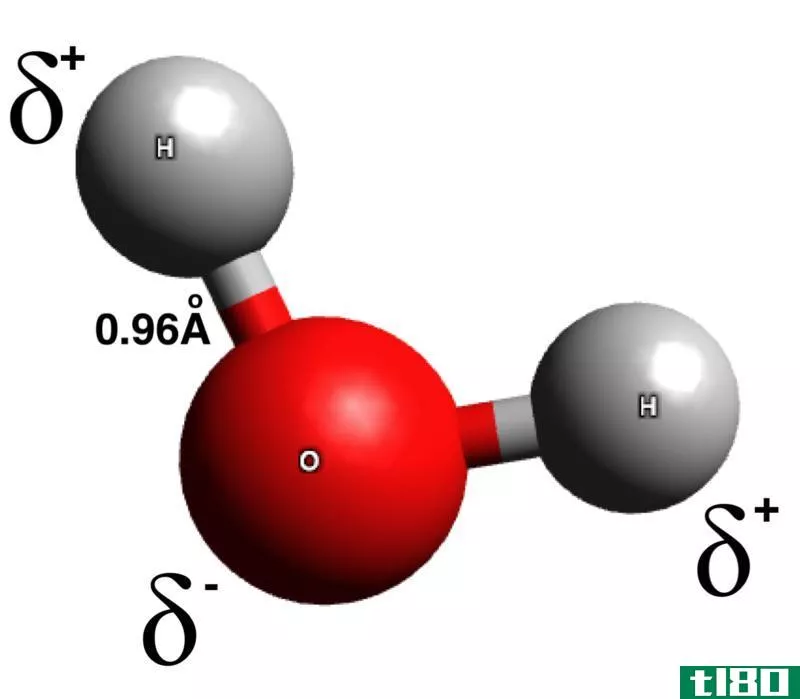
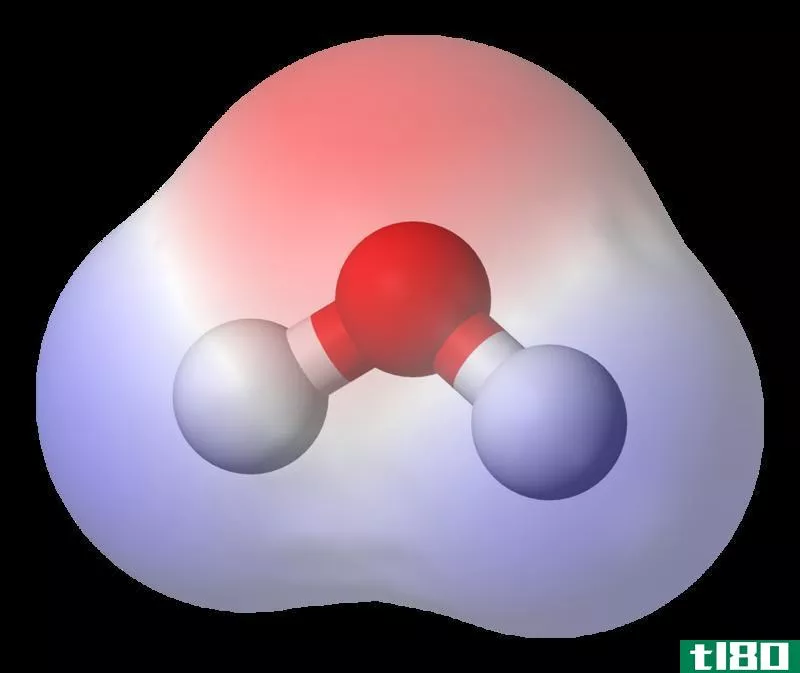
Water Molecule:
氢和氧的电负性分别为2.20和3.44。其差值为1.24,符合形成极性键的主要标准。电子更容易被电负性相对较大的氧原子吸引。因此分子上有一个净偶极子。据说O有点阴性(δ-), 而氢原子是微正的(δ+).
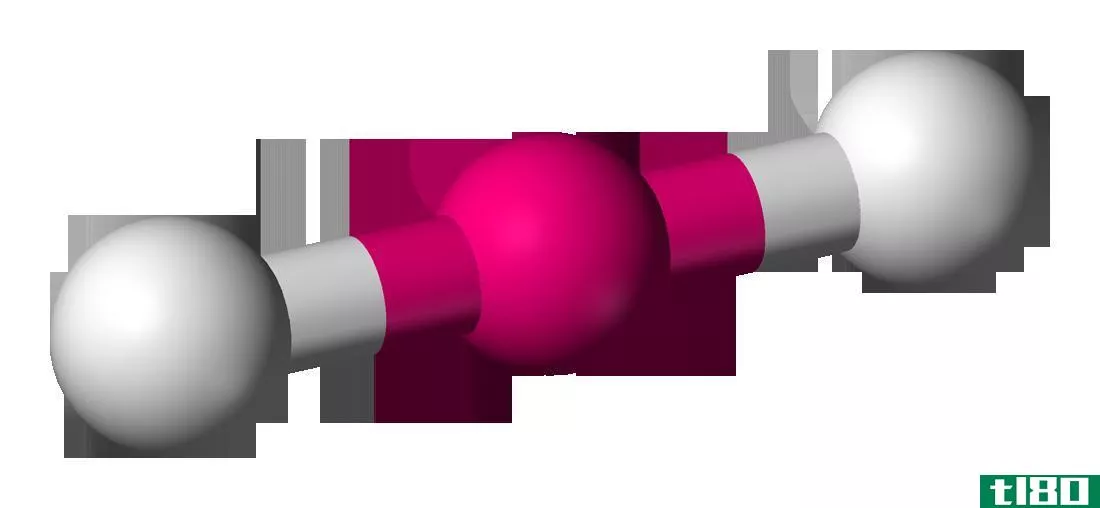
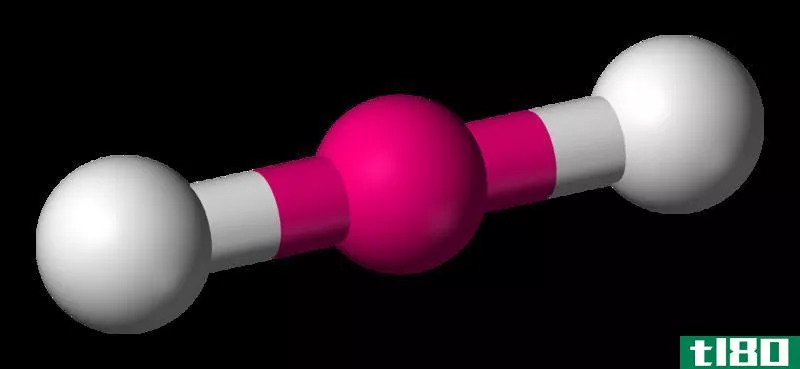
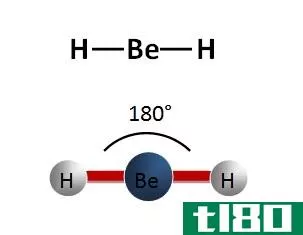
在决定分子的极性时,分子的形状也起着重要作用。让我们通过考虑二氧化碳分子来更好地理解这个场景。

C是比O(2.55和3.44)电负性小的原子,满足0.4电负性差的要求。然而,由于分子的形状,两个C-O键上的偶极矩方向相反,相互抵消。因此,净偶极矩为零。
极性分子在一起时,通过原子上相反的电荷相互吸引。这些力比非极性分子间的力强,但比离子力弱。
带正电荷的氢原子与带负电荷的氧原子形成氢键。如果氢原子参与形成这样的吸引力,它们被称为氢键,在没有氢原子参与的情况下形成的分子间作用力被称为偶极-偶极作用力。极性分子只溶于极性溶剂,因为它们不能与非极性溶剂形成任何吸引力。
极性化合物的熔点和沸点高于分子量相近的非极性化合物。应该提供能量来打破分子间的键。因此,熔点和沸点都很高。这导致低蒸气压,蒸发率低于非极性分子。此外,极性分子表现出更大的表面张力。
什么是非极性分子(nonpolar molecules)?
与极性分子不同,非极性分子上没有正负电荷。这是因为这两个原子对它们共享的电子有相似的吸引力。两个原子的电负性差<0.4。因此,电子对均匀地分布在原子之间。同一元素的双原子气体大多是非极性分子。例如:O2、N2、Cl2等。碳氢化合物分子如甲烷、戊烷和己烷是非极性分子。
应注意的是,非极性分子可能表现出伦敦色散力,这是由电子的不对称分布引起的。这是一种自发的、暂时的力,是所有分子间力中最弱的。这些伦敦力足以使非极性分子溶解在非极性溶剂中。然而,由于这些力比极性偶极力弱,如果非极性分子溶解在极性溶剂中,它们就不会混合。相反,将形成一个异构系统。在这种情况下,溶解过程没有能量上的优势。
与相同分子质量的极性分子相比,非极性分子由于缺乏强大的分子间作用力而具有较低的熔点和沸点。此外,由于分子很容易蒸发掉,非极性化合物表现出很高的蒸气压。因此,大多数非极性分子形成挥发性化合物。
例如:戊烷、己烷

极地的(polar)和非极性分子(nonpolar molecules)的区别
净偶极子
极性分子:由于参与原子的电负性差异或分子的不对称排列,出现了净偶极子。
非极性分子:当涉及到具有类似电负性的原子或由于对称排列,不存在净偶极子。
电负性差
极性分子:原子间电负性差为<;0.4.
非极性分子:原子间的电负性差为>;0.4.
分子力
极性分子:分子力相当强,形成氢键或偶极键。
非极性分子:分子力是最弱的;形成了分散的军队。
物理性质
极性分子:极性分子具有高沸点、熔点、低蒸气压和高表面张力。
非极性分子:非极性分子具有低沸点、熔点、高蒸气压和低表面张力。
示例
极性分子:例如水、HF和CHF3。
非极性分子:例如戊烷、己烷和二氧化碳。
参考文献:
“Molecule – Formation.” Atoms, Molecules, Substances, and Kinds – JRank Articles. n、 p.,n.d.网站。2017年2月2日。
“Water Treatment Soluti***.” LENNTECH. n、 p.,n.d.网站。2017年2月2日。
“Polar vs Non-Polar Molecules: What you Need to Know.” Udemy Blog. n、 p.,n.d.网站。2017年2月2日。
“What are the properties of non-polar molecules? | Socratic.” Socratic.org. n、 p.,n.d.网站。2017年2月2日。
“London Dispersion Forces.” London Dispersion Forces. n、 p.,n.d.网站。2017年2月2日。
“Non-Polar dissolves Non-polar?” Chemical Forums. n、 p.,n.d.网站。2017年2月2日。
Image Courtesy:
“Figure 02 01 11” By CNX OpenStax(抄送4.0)通过Comm*** Wikimedia
- 发表于 2021-06-28 12:20
- 阅读 ( 1808 )
- 分类:科学
你可能感兴趣的文章
线性的(linear)和弯曲分子(bent molecules)的区别
...性和弯曲分子的表格形式 5. 摘要 什么是线性分子(linear molecules)? 线性分子是键角为180度的直分子。基本上,这些分子包含一个中心原子,通过单键或双键(有时也有三键)与另外两个原子结合。如果两个键合的原子相同,这种...
- 发布于 2020-09-21 13:37
- 阅读 ( 315 )
极地的(polar)和偶极分子(dipolar molecules)的区别
...极性与偶极分子的表格形式 5. 摘要 什么是极性分子(polar molecules)? 极性分子是具有极性键的化学物质。这些极性键的偶极矩之和不等于零。极性键有部分正电荷端和部分负电荷端。这些电荷是由于整个化学键中电子分布的差异...
- 发布于 2020-09-24 05:10
- 阅读 ( 532 )
线性的(linear)和非线性分子(nonlinear molecules)的区别
...和非线性分子的表格形式 5. 摘要 什么是线性分子(linear molecules)? 线性分子是具有线性几何的化合物。这意味着,这些线性分子的原子连接性是直线的。分子中的所有原子都排列成一条完美的线。 图01:线性几何 在线性几何中...
- 发布于 2020-09-25 02:34
- 阅读 ( 732 )
极地的(polar)和非极性溶剂(nonpolar solvents)的区别
...,极性非质子溶剂不能提供氢原子。 什么是非极性溶剂(nonpolar solvents)? 非极性溶剂是没有偶极矩的液体。因此,这些溶剂不含部分正电荷或负电荷。由于这个原因,这些溶剂不能溶解极性化合物,因为没有相反的电荷来吸引极...
- 发布于 2020-10-12 14:40
- 阅读 ( 493 )
盐桥(salt bridge)和氢键(hydrogen bond)的区别
...键的强度更大。 Usually, hydrogen bonds form between polar covalent molecules. These molecules contain polar covalent bonds, which form as a result of the difference in the electronegativity values of the atoms that are in the covalent bond. If this difference is high, the highly electronegati...
- 发布于 2020-10-14 03:27
- 阅读 ( 971 )
分子元素(molecule of element)和化合物分子(molecule of compound)的区别
...分子与化合物分子的表格形式 5. 摘要 什么是分子元素(molecule of element)? 元素的分子是两个或两个以上同类型原子的组合。这意味着这些分子是由同一化学元素的原子组成的。我们可以根据分子中存在的原子数进一步对它们进...
- 发布于 2020-10-18 02:47
- 阅读 ( 506 )
极地的(polar)和非极性氨基酸(nonpolar amino acids)的区别
...类的例子包括天冬氨酸和谷氨酸。 什么是非极性氨基酸(nonpolar amino acids)? 非极性氨基酸是没有极性的氨基酸。这是因为这些氨基酸的羧基和胺基数目相等。这使得这些非极性氨基酸具有中性电荷。他们对“R”组没有收费。 非...
- 发布于 2020-10-19 04:50
- 阅读 ( 1157 )
形状(shape)和分子几何学(geometry of a molecule)的区别
...分子形状与几何结构 5. 摘要 什么是分子的形状(shape of a molecule)? 分子的形状是用中心原子上的键-电子对预测的分子结构。换句话说,除了中心原子的孤电子对之外,分子的形状是确定的。分子的形状可以用VSEPR模型(价层电...
- 发布于 2020-11-02 15:58
- 阅读 ( 507 )
极地的(polar)和非极性(non-polar)的区别
...性的,它就有正负电荷。 另一方面,与极性分子不同,非极性分子没有足够的电荷。非极性分子以对称的方式分布,并且不包含附着在其上的大量电荷。具有极性分子的物质的一个例子是水。水是由极性分子组成的,因为原子...
- 发布于 2021-06-23 19:30
- 阅读 ( 397 )
非极性(non-polar)和极性共价键(polar covalent bonds)的区别
非极性与极性共价键 非极性和极性共价键既属于极性的三类,也属于共价键的两类。所有这三种类型(离子、极性和非极性)都被归类为化学键,其中有一种力(电负性)允许两种特定元素的原子相互吸引。可能的共价键的数...
- 发布于 2021-06-24 05:05
- 阅读 ( 608 )