极性溶剂和非极性溶剂的关键区别在于极性溶剂溶解极性化合物,而非极性溶剂溶解非极性化合物。
化合物的极性是指具有极性的性质。在化学中,它是指一个分子中含有具有不同电负性的原子或原子群的电荷分离。因此,它在同一化合物中产生部分正电荷和部分负电荷。
目录
1. 概述和主要区别
2. 什么是极性溶剂
3. 什么是非极性溶剂
4. 并列比较-极性和非极性溶剂的表格形式
5. 摘要
什么是极性溶剂(polar solvents)?
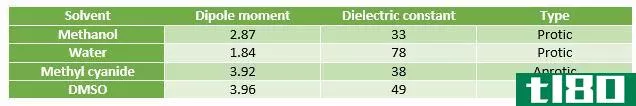
极性溶剂是具有大偶极矩的液体。这些是能溶解极性化合物的液体。这是因为极性溶剂和极性化合物在同一化合物中都有偶极矩和相反的电荷部分。固体化合物的正电荷部分可被溶剂分子的带负电部分吸引,反之亦然,这会导致极性化合物在极性溶剂中溶解。
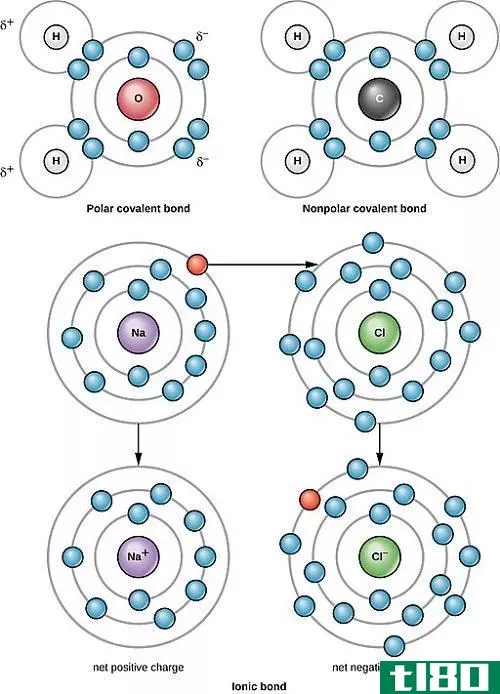
溶剂的极性是由于具有不同电负性值的原子连接性而形成的分子。在这里,电负性越强的原子会吸引键-电子对,这最终会使电负性较低的原子由于其周围电子密度的降低而带有部分正电荷。另一方面,由于原子周围的电子密度增加,电负性越强的原子就得到部分负电荷。
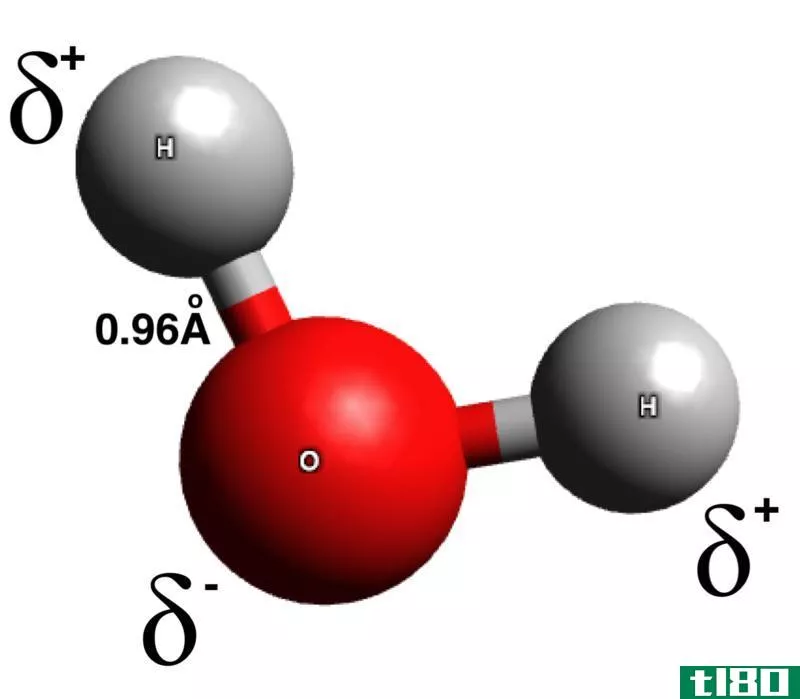
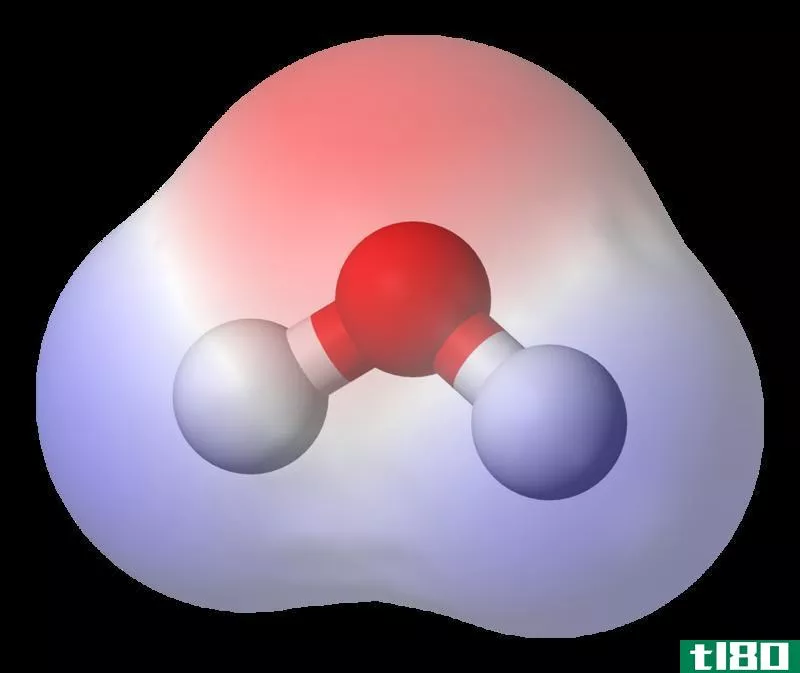
极性溶剂最常见的例子是水。水分子有两个O-H键。氧原子和氢原子之间的电负性差别相当大。因此,它是极性共价键。氧原子的电负性更强。因此,氧原子得到部分负电荷,而两个氢原子得到部分正电荷。

图01:水是极性溶剂
此外,我们还将极性溶剂分为极性质子溶剂和极性非质子溶剂两大类。极性质子溶剂含有不稳定的H+离子。这意味着这些溶剂的分子可以提供氢原子。然而,极性非质子溶剂不能提供氢原子。
什么是非极性溶剂(nonpolar solvents)?
非极性溶剂是没有偶极矩的液体。因此,这些溶剂不含部分正电荷或负电荷。由于这个原因,这些溶剂不能溶解极性化合物,因为没有相反的电荷来吸引极性化合物。

图02:己烷是一种非极性溶剂
非极性溶剂可以通过吸引力(如范德华力)溶解非极性化合物。一些非极性溶剂包括戊烷、己烷、苯、甲苯等。
极地的(polar)和非极性溶剂(nonpolar solvents)的区别
溶剂主要分为极性溶剂和非极性溶剂两大类。极性溶剂和非极性溶剂的关键区别在于极性溶剂溶解极性化合物,而非极性溶剂溶解非极性化合物。另外,极性溶剂和非极性溶剂的另一个显著区别是极性溶剂具有较高的偶极矩,而非极性溶剂没有偶极矩。极性溶剂的一个常见例子是水。一些非极性溶剂包括戊烷、己烷、苯、甲苯等。
此外,极性溶剂中有带有极性键的分子(由于键中原子的电负性不同,这些键显示电荷分离)。非极性溶剂中含有化学键的分子,这些化学键由具有几乎相似电负性的原子组成。

总结 - 极地的(polar) vs. 非极性溶剂(nonpolar solvents)
溶剂主要分为极性溶剂和非极性溶剂两大类。极性溶剂和非极性溶剂的关键区别在于极性溶剂溶解极性化合物,而非极性溶剂溶解非极性化合物。
引用
1“极性溶剂”,维基百科,维基媒体基金会,2019年10月17日,可在这里查阅。