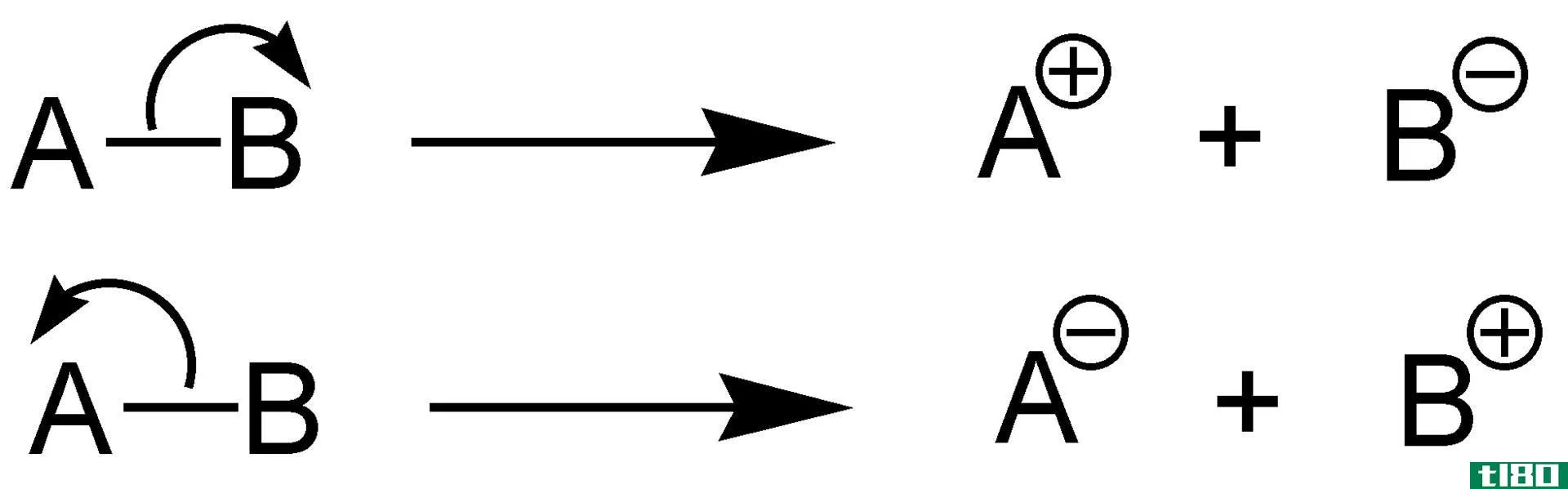
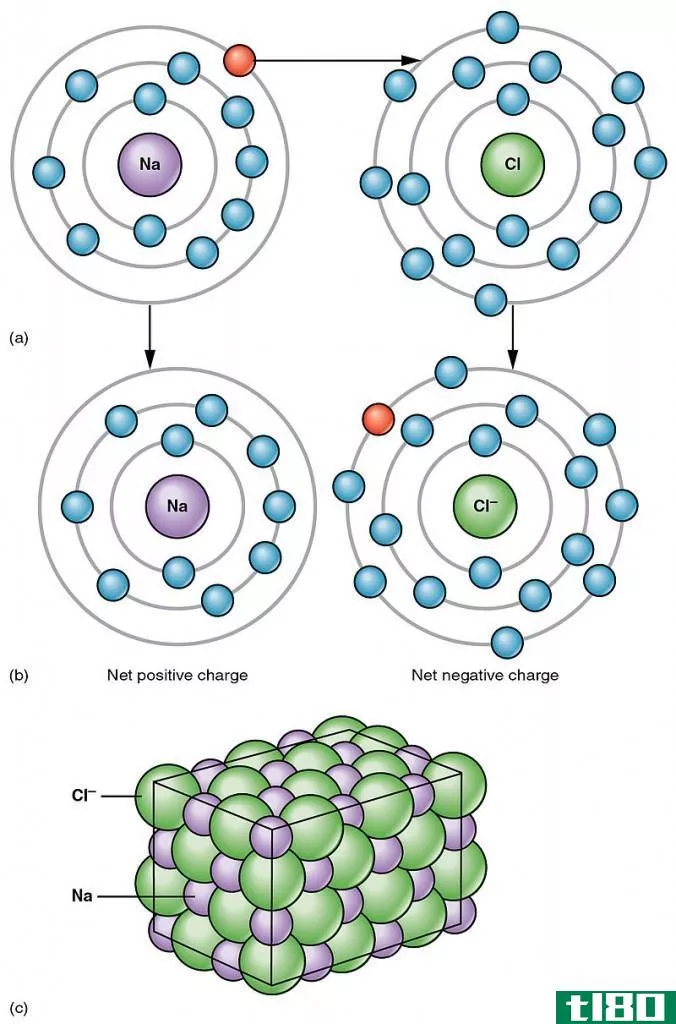
关键区别-键能与键焓
键能和键焓都描述了同一个化学概念:将一摩尔分子分解成其组成原子所需的能量。它测量化学键的强度。所以也叫粘结强度。键能计算为气相化学物质在298K下的键离解能的平均值。键能和键焓这两个词之间没有很大的区别,但键能用“E”表示,而键焓用“H”表示。
目录
1. 概述和主要区别
2. 什么是键能
3. 什么是键焓
4. 并列比较-以表格形式表示的键能与键焓
5. 摘要
什么是键能(bond energy)?
键能或键焓是键强度的量度。键能是将一摩尔分子分解成其组成原子所需的能量。这意味着键能是打破化学键所需的能量。键能用“E”表示。计量单位为kJ/mol。
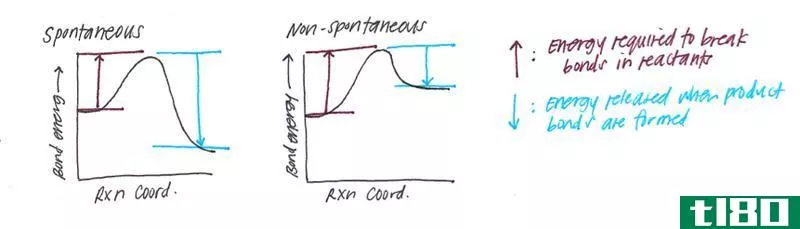
当单个原子具有不稳定的高能量时,原子间形成化学键以获得稳定状态。这意味着化学键的形成降低了系统的能量。因此,当形成化学键时,一些能量被释放(通常是热)。因此,键的形成是一个放热反应。为了打破这种化学键,应该提供能量(与键形成时释放的能量相等)。这个能量量被称为键能或键焓。
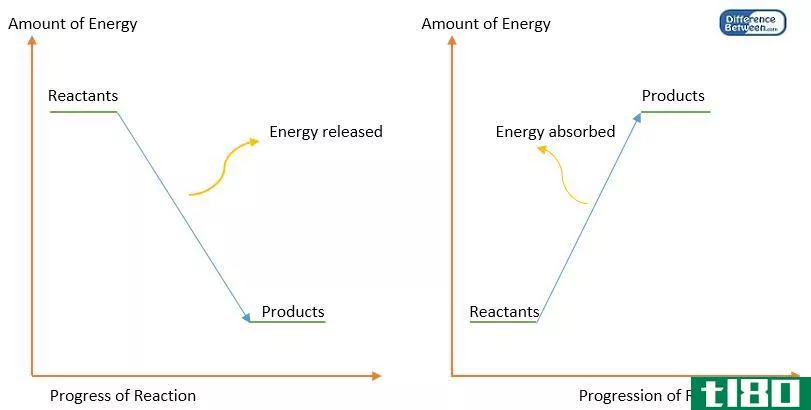
图1:键形成(左)和键离解(右)的能量图。
键能等于产物(原子)和反应物(起始分子)的焓差。每个分子都应该有自己的键能值。但也有例外。例如,C-H键的键能取决于发生键的分子。因此,键能计算为键离解能的平均值。
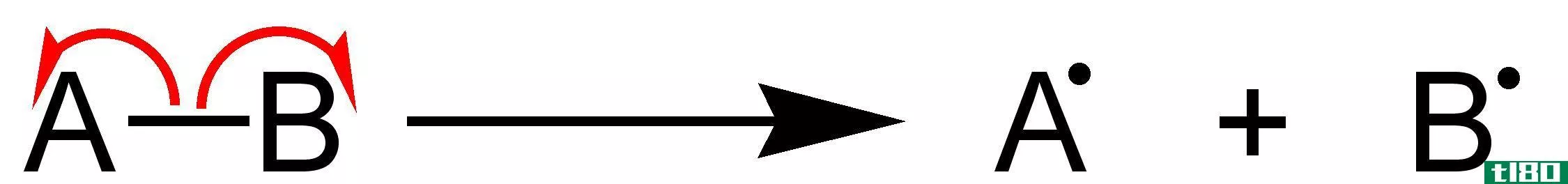
键能是同一物种在气相(298K温度下)的平均键离解能。例如,甲烷分子(CH4)的键能是形成一个碳原子和4个氢自由基所需的能量。然后取每个C-H键的键离解能之和除以4,即可计算出C-H键的键能。
例:水分子中O-H键的键能可计算如下。
打破氢键所需的能量=498.7 kJ/mol
打破O-H键所需的能量(在剩余的OH自由基中)=428 kJ/mol
平均键离解能=(498.7+428)/2
=463.35千焦/摩尔≈464千焦/摩尔
因此,H2O分子中O-H的键能为464kj/mol。
什么是键焓(bond enthalpy)?
键焓或键能是将分子分离成原子组分所需的能量。它是一种力量的衡量标准。键焓用“H”表示。
键能(bond energy)和键焓(bond enthalpy)的区别
- 键能或键焓是将一摩尔分子分解成其组成原子所需的能量。
- 键能用“E”表示,键焓用“H”表示。
总结 - 键能(bond energy) vs. 键焓(bond enthalpy)
键能或键焓是将一摩尔分子分离成气态原子组分所需的能量。它是用化学键的键离解能值来计算的。因此,键能是键离解能的平均值。它总是一个正值,因为键的离解是吸热的(键的形成是放热的)。键能和键焓之间没有明显差别。