水化和氢化的关键区别在于水合作用是指将水分子添加到有机化合物中,而氢化是指将氢分子添加到有机化合物中。
水合和加氢在化学合成反应中起着重要作用。这两种反应都涉及到通过在双键中的碳原子加上一个取代基来打开有机化合物中的双键。在这些过程中加入的取代基是不同的。
目录
1. 概述和主要区别
2.什么是水合作用
3. 什么是氢化
4. 并列比较-表格形式的水合与氢化
5. 摘要
什么是水合作用(hydration)?
水合作用是将水分子添加到有机化合物中。碳原子之间通常有一个双键。水分子以羟基(OH-)和质子(H+)的形式加入双键。因此,水分子在加入前分解成离子。羟基附着在双键的一个碳原子上,而质子附着在另一个碳原子上。
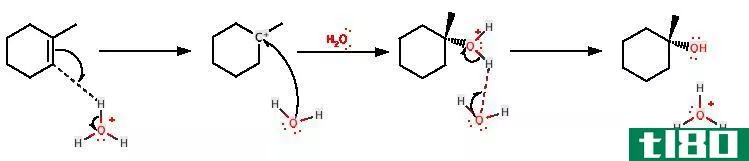
图01:简单的水合反应
由于它涉及到键的断裂和键的形成,所以反应具有很强的放热性。这意味着,反应以热的形式释放能量。它是一个逐步反应;在第一步,烯烃起到亲核作用,攻击水分子的质子,并通过较少取代的碳原子与之结合。这里,反应遵循Markonikov规则。
第二步包括水分子的氧原子与另一个双键的碳原子(高取代碳原子)的连接。此时,水分子的氧原子携带正电荷,因为它有三个单键。然后,另一个水分子,它占据附加水分子的额外质子,使羟基留在较少取代的碳原子。因此,这种反应导致酒精的形成。然而,炔烃(含烃的三键)也可以发生水化反应。
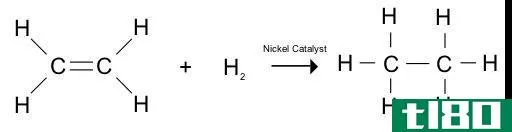
什么是氢化(hydrogenation)?
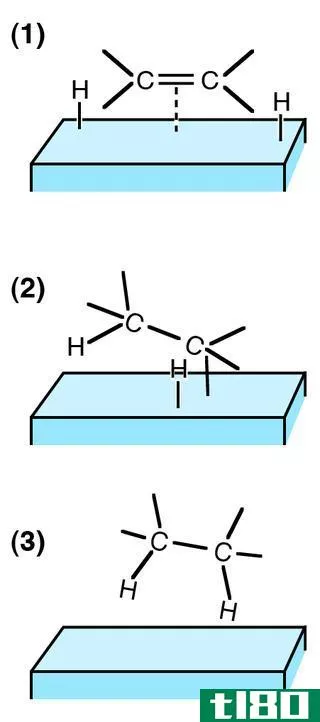
加氢是把氢分子加到有机化合物中的过程。此外,该反应涉及到用氢气处理有机化合物。通常,反应发生在催化剂存在下,如镍、钯或铂。非催化加氢只能在非常高的温度下进行。此外,这一过程对不饱和有机化合物的还原也很重要。也就是说,加氢可以打开有机化合物中的双键或三键,并把它们变成含有单键的化合物。
加氢过程由三部分组成:不饱和底物、氢源和催化剂。反应条件,如温度和压力取决于不饱和化合物和催化剂的类型。底物可以是烯烃或炔烃。加氢反应有两种方式:均相催化和多相催化。
在均相催化中,催化剂金属与烯烃和氢气结合生成中间产物(烯烃催化剂-氢中间化合物)。然后一个氢原子通过双键(或三键)从金属转移到碳。接下来发生的是另一个氢原子从氢源转移到烷基,同时烷烃也发生解离。
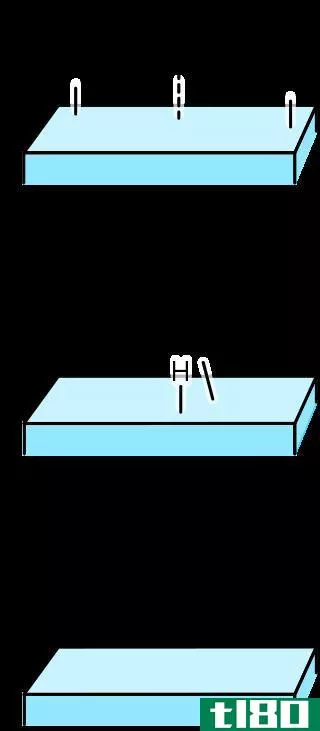
图02:加氢三步
在多相催化中,不饱和键与催化剂结合,而氢源则分解成两个氢原子。然后一个可逆的步骤发生在一个氢原子与不饱和键结合的地方。最后,当另一个氢原子附着在烷基上时,会发生不可逆反应。
水合作用(hydration)和氢化(hydrogenation)的区别
水合和加氢是化学合成中的重要过程。水化和氢化的关键区别在于水合作用是指将水分子添加到有机化合物中,而氢化是指将氢分子添加到有机化合物中。
下面的信息图总结了水合和氢化之间的区别。

总结 - 水合作用(hydration) vs. 氢化(hydrogenation)
水合和加氢是化学合成中的重要过程。水化和氢化的关键区别在于水合作用是指将水分子添加到有机化合物中,而氢化是指将氢分子添加到有机化合物中。
引用
1“测定溶液中离子用离子选择电极、参比电极、组合电极和离子选择电极仪表规范。”doi:10.3403/002222406U。