原子和离子的主要区别在于它们的电荷;原子是中性的,而离子则带正电荷或负电荷。
原子是能形成键的最小中性单元,而离子是任何带电分子。离子可以由几个原子或单个原子组成。原子是唯一的,不分为各种类型,而离子有两种类型,即正离子(阳离子)和负离子(阴离子)。
目录
1. 概述和主要区别
2. 什么是原子
3. 什么是离子
4. 并排比较——表格形式的原子与离子
5. 摘要
什么是原子(an atom)?
原子是物质的最小单位,某个原子代表它所属的化学元素的性质。所有的气体、固体物质、液体和等离子体都是由原子组成的,原子是非常小的单位,其大小约为100皮米。

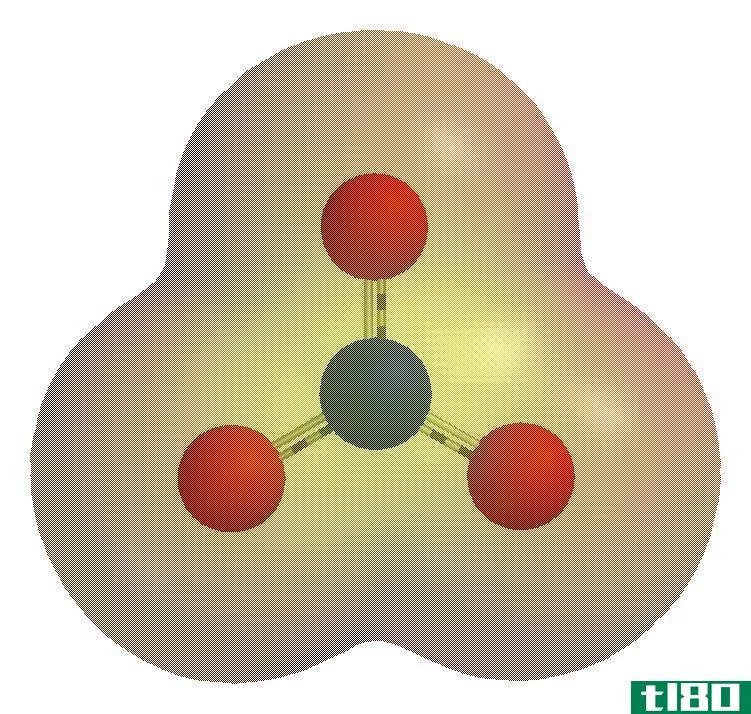
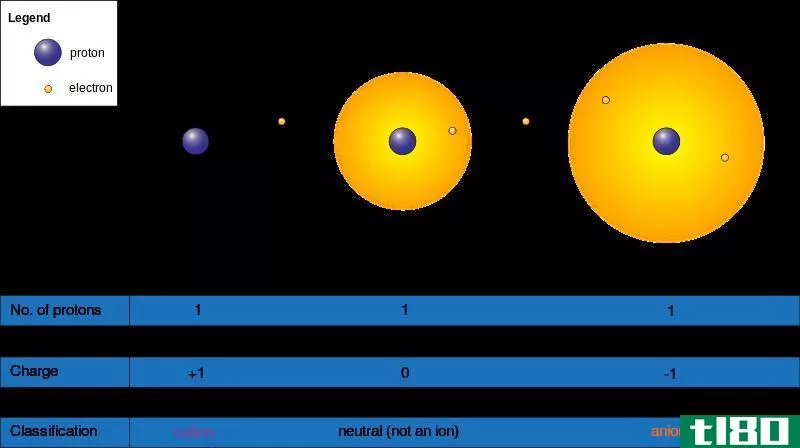
图01:原子的一般结构
当考虑原子的结构时,它包含一个原子核和围绕原子核运动的电子。此外,质子和中子(还有一些其他亚原子粒子)构成了原子核。通常情况下,中子、质子和电子的数量是相等的,但在同位素的情况下,中子的数量不同于质子。我们称质子和中子为“核子”。
大约99%的原子质量集中在原子核中,因为电子的质量几乎可以忽略不计。在这些亚原子粒子中,质子有+1电荷;电子有-1电荷,中子没有电荷。如果原子有相同数量的质子和电子,那么原子的总电荷为零;缺少一个电子会产生+1电荷,而增加一个电子则会给原子带-1电荷。
什么是离子(an ion)?
离子是一种带电的化学物质。它们的电子和质子数量总是不相等。有两种类型的离子,如阳离子和阴离子。由于缺少电子来平衡质子的电荷,阳离子带有正电荷。另一方面,阴离子有过量的电子,并且由负电荷组成。

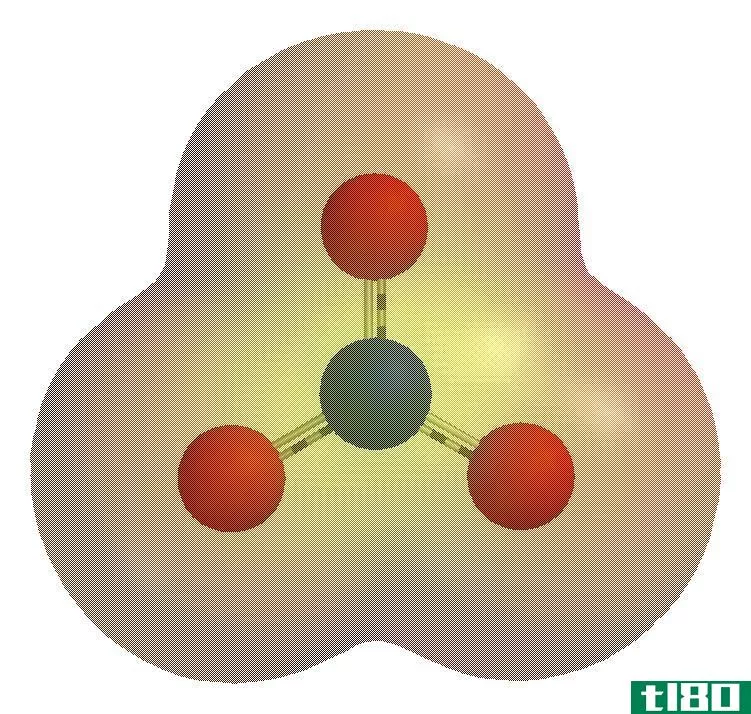
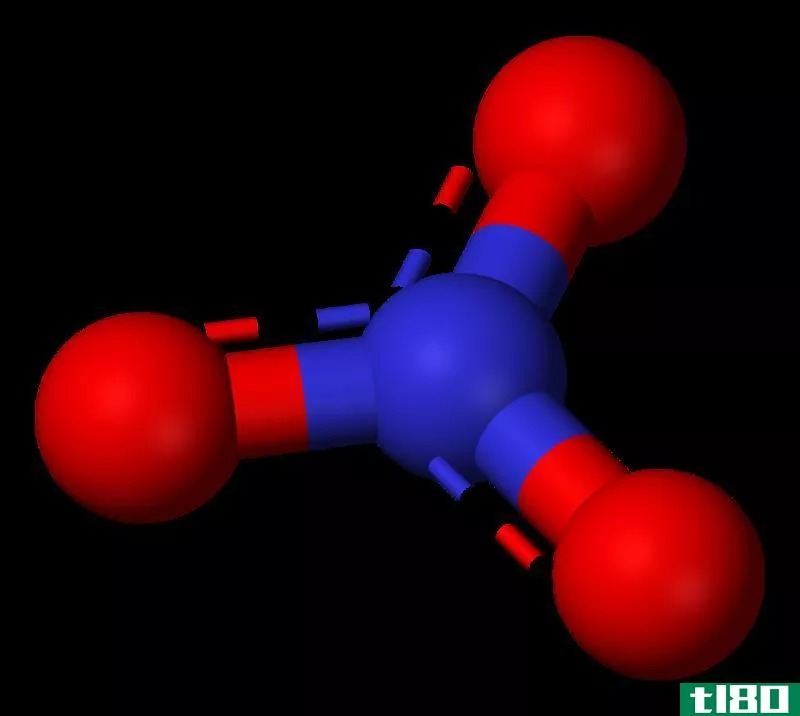
图02:阴离子
离子存在于物质的所有三个阶段:固态、液态和气态。有些离子是带电荷的单原子,但大多数情况下,离子是多原子的。
原子(atom)和离子(ion)的区别
原子和离子的主要区别是电荷。原子是电中性的,而离子是带电的。原子总是含有相等数量的电子和质子,但在离子中,电子和质子的数量总是不同的。一个离子能带的最大正电荷数是6;负电荷的最大数目是3。发生这种情况有两个原因。第一个原因是电子的损失,这导致了正离子。另一个原因是电子的增加,产生负离子。原子总是有原子轨道,而离子要么有原子轨道要么有分子轨道,要么既有原子轨道又有分子轨道。这是原子和离子的另一个区别。此外,原子只能在气相中找到,而离子可以在气相、液相和固相中找到。

总结 - 原子(atom) vs. 离子(ion)
原子和离子的主要区别是电荷。原子是电中性的,而离子是带电的。原子中电子和质子的数量总是相等的,但在离子中,电子和质子的数量总是不同的。