半当量点与当量点的关键区别在于,半当量点是某一特定滴定的起始点和当量点之间的中点,而当量点是化学反应结束的地方。
滴定法是化学中的分析技术,在确定给定样品的未知浓度时非常重要。
目录
1. 概述和主要区别
2. 什么是等值点
3. 什么是半等价点
4. 并列比较-半等价点与等价点的表格形式
5. 摘要
什么是半等价点(half equivalence point)?
滴定的半当量点是当量点和起始点(原点)之间的中间点。这一点的重要性在于,此时分析物溶液的pH值等于滴定中所用酸的离解常数或pKa。半当量点出现在滴定的第一个当量点的一半体积处。如果滴定中存在多个等效点,则会有多个半等同性点,这些半等同点的个数相等。例如,第二个半等价点出现在第一个和第二个等价点之间的中点处。
什么是等效点(equivalence point)?
滴定中的当量点是反应混合物中所需化学反应结束的实际点。我们通常用滴定法来测定液体中某种物质的浓度。如果我们知道物质,可以使用具有已知浓度的滴定剂(用于测定液体混合物中成分浓度的溶液)与分析物反应。这里,我们称滴定液为标准溶液,因为它的准确摩尔浓度已知。
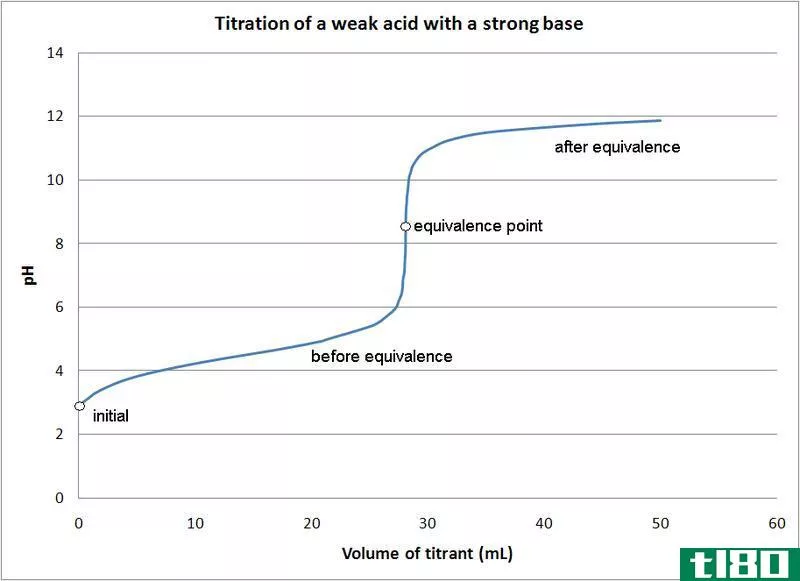
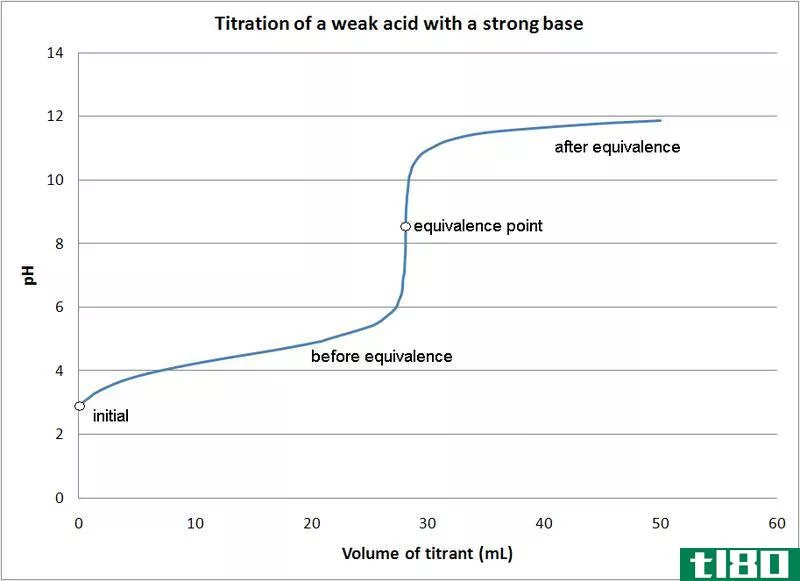
图01:指示等效点的滴定曲线
在NaOH和HCl的反应中,这是一个酸碱反应,我们可以用NaOH或HCl作为已知浓度的滴定剂。在这里,滴定剂被放置在滴定管中,我们可以慢慢地将其添加到滴定和/分析物中,直到反应混合物发生颜色变化。我们需要使用指示剂,因为NaOH和HCl不是自指示剂。发生颜色变化的点是滴定终点,而不是反应的等效点。
在该滴定法中,当量点是所有HCl分子与NaOH反应的点(或所有NaOH分子与HCl反应的点)。那么滴定液的摩尔数应等于未知分析物的摩尔数,因为HCl和NAOH之间的化学计量比为1:1。测定滴定的当量点有不同的方法。
- 自指示剂的颜色变化-在使用自指示剂作为反应物的反应中,颜色变化揭示了滴定的等效点,因为它们不使用指示剂。
- 端点–有时,等效点可以作为端点,因为它们近似相等。
- 电导-在这种方法中,电导是在整个滴定过程中测量的,等效点是电导发生快速变化的地方。这是一个有点困难的方法。
- 光谱-这是一种适用于彩色反应混合物的方法。根据样品吸收波长的快速变化来确定等效点。
半等价点(half equivalence point)和等效点(equivalence point)的区别
滴定法是化学中的分析技术,在确定给定样品的未知浓度时非常重要。半当量点与当量点的关键区别在于,半当量点是某一特定滴定法的起始点和当量点之间的中点,而当量点是化学反应结束的地方。
下表总结了半等效点和等效点之间的区别。

总结 - 半等价点(half equivalence point) vs. 等效点(equivalence point)
滴定法是化学中的分析技术,在确定给定样品的未知浓度时非常重要。半当量点与当量点的关键区别在于,半当量点是某一特定滴定法的起始点和当量点之间的中点,而当量点是化学反应结束的地方。
引用
1“滴定曲线和等效点(文章)”