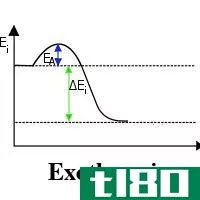
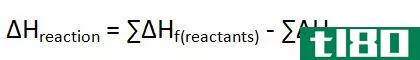冰对水蒸气的焓变
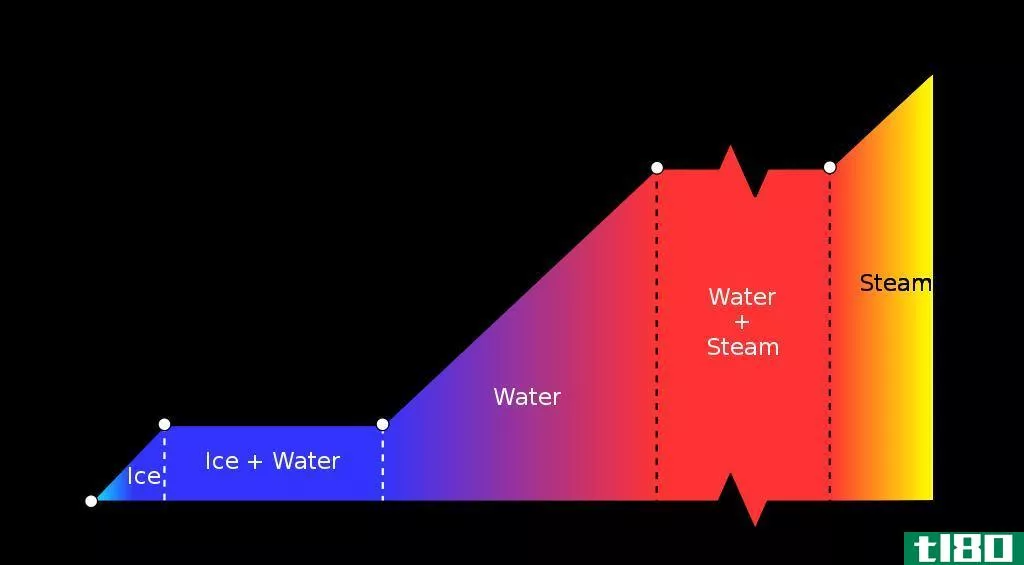
这个焓变示例问题是当冰的状态从固态转变为液态水,最后转变为水蒸气时的焓变。

焓回顾
在开始之前,您可能希望复习热化学定律以及吸热和放热反应。
问题
给出:冰的熔化热为333 J/g(即当1克冰融化时,333 J被吸收)。液态水在100°C下的蒸发热为2257 J/g。
a部分:计算这两个过程的焓变化ΔH。
H2O(s)→ H2O(l);ΔH=?
H2O(l)→ H2O(g);ΔH=?
第二部分:使用刚才计算的值,确定0.800 kJ热量可以融化的冰的克数。
解决方案
a) 你注意到聚变热和汽化热是焦耳而不是千焦耳吗?使用周期表,我们知道1摩尔水(H2O)为18.02克。因此:
熔合ΔH=18.02 g x 333 J/1 g熔合ΔH=6.00 x 103 J熔合ΔH=6.00 kJ
蒸发ΔH=18.02 g x 2257 J/1 GVA蒸发ΔH=4.07 x 104 J蒸发ΔH=40.7 kJ
因此,完成的热化学反应为:
H2O(s)→ H2O(l);ΔH=+6.00 kJH2O(l)→ H2O(g);ΔH=+40.7千焦
b) 现在我们知道:
1 mol H2O(s)=18.02 g H2O(s)~6.00 kJ
因此,使用这个转换系数:
0.800千焦x 18.02克冰/6.00千焦=2.40克融化的冰
回答
a) H2O(s)→ H2O(l);ΔH=+6.00 kJ H2O(l)→ H2O(g);ΔH=+40.7千焦
b) 2.40克冰融化
- 发表于 2021-09-15 09:46
- 阅读 ( 194 )
- 分类:化学
你可能感兴趣的文章
高热值(hhv)和低热值(lhv)的区别
...后化合物的共同温度。此外,如果在燃烧反应过程中产生水蒸气,它会经过冷凝形成液态水。 图01:水的相变 此外,在测量高热值时,还必须考虑水的汽化潜热。在计算发生冷凝的燃料的热值时,该值很重要。这意味着,在进...
- 发布于 2020-09-28 21:03
- 阅读 ( 498 )
键焓(bond enthalpy)和晶格焓(lattice enthalpy)的区别
...用标准定义,它说键焓是物质在298 K下一摩尔键被破坏时的焓变。由于这个术语涉及键断裂,我们也可以将其命名为键离解能。其他同义词包括键强度和平均键能。 图01:一些化学键的键能 如果键的焓值很高,说明键很强,很难...
- 发布于 2020-10-15 02:15
- 阅读 ( 437 )
生成热(heat of formation)和反应热(heat of reaction)的区别
...区别在于,生成热是在标准条件下形成一摩尔物质过程中的焓变化,而反应热是在恒压下发生的化学反应过程中焓的变化。 生成热和反应热是化学反应的重要焓值。我们将这些术语定义为标准条件,即标准压力和标准温度。在...
- 发布于 2020-10-18 06:22
- 阅读 ( 523 )
焓(enthalpy)和熵(entropy)的区别
...的变化取决于反应物的相。例如,当氧气和氢气反应生成水蒸气时,焓变为-483.7kj。当相同反应物反应生成液态水时,焓变为-571.5kj。 2H2(g)+O2(g)→2H2O(g);∆H=-483.7千焦 2H2(g)+O2(g)→2H2O(l);∆H=-571.7 kJ 什么是熵(entr...
- 发布于 2020-11-04 20:59
- 阅读 ( 1864 )
焓(enthalpy)和热(heat)的区别
...的变化取决于反应物的相。例如,当氧气和氢气反应生成水蒸气时,焓变为-483.7kj。但是,当相同反应物反应生成液态水时,焓变为-571.5kj。 什么是热(heat)? 一个系统做功的能力就是这个系统的能量。我们可以在系统上做功,也...
- 发布于 2020-11-05 19:40
- 阅读 ( 881 )
放热的(exothermic)和吸热的(endothermic)的区别
...光或其他类似的能源,这个反应就无法完成。 放热反应的焓变总是负的,而吸热反应的焓变总是正的。这分别是由于反应中热能的释放和吸收。最终产物在放热反应中是稳定的。吸热反应的最终产物不太稳定。这是由于形成的...
- 发布于 2021-06-22 11:50
- 阅读 ( 439 )
键能(bond energy)和键离解能焓(bond dissociation energy enthalpy)的区别
...能量。我们可以把它定义为当一个键因均裂而断裂时发生的焓变。键的离解能是单键所特有的。 键焓(一个系统的热力学性质)或键离解能,被称为标准焓变化,当一个键在0 K(绝对零度)下被同分解物(分解成小块)和同分...
- 发布于 2021-06-26 10:13
- 阅读 ( 471 )
焓(enthalpy)和内能(internal energy)的区别
...了变化,这种变化被测量为焓。在恒定压力下发生的过程的焓可以如下所示。 h=u+pv 哪里, H是焓,U是内能之和,P是系统的压力,V是系统的体积 因此,焓实际上是内能和在给定压力下维持系统体积所需的能量之和。术语“PV”...
- 发布于 2021-06-29 08:17
- 阅读 ( 934 )
吸热的(endothermic)和放热反应(exothermic reactions)的区别
...为吸热反应和放热反应,我们可以计算反应物和产物之间的焓变。如果没有,我们可以观察反应混合物的温度变化。吸热反应和放热反应的主要区别在于,吸热反应从周围吸收能量,而放热反应向周围释放能量。 覆盖的关键领...
- 发布于 2021-06-29 08:53
- 阅读 ( 1300 )
自发的(spontaneous)和非自发性反应(nonspontaneous reactions)的区别
...一个例子。火灾的产物部分由两种气体组成:二氧化碳和水蒸气。燃烧产生热量。因此,它是一个火用反应。热增加了系统的熵。但是,燃烧产物的熵有一个约化熵。 什么是非自发性反应(n***pontaneous reacti***)? 非自发反应是指...
- 发布于 2021-06-29 21:57
- 阅读 ( 702 )