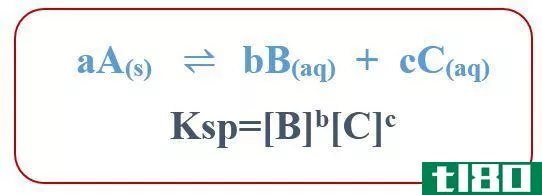从溶解度积问题看溶解度
这个示例问题演示了如何通过物质的溶解度积来确定离子固体在水中的溶解度。

问题
- 氯化银(AgCl)在25℃时的溶解度积为1.6 x 10-10。
- 氟化钡(BaF2)在25°C下的溶解度积为2 x 10-6。
计算两种化合物的溶解度。
解决
解决溶解度问题的关键是正确设置解离反应并定义溶解度。溶解度是使溶液饱和或达到离解反应平衡所消耗的试剂量。
氯化银
氯化银在水中的离解反应为:
AgCl (s) ↔ Ag+ (aq) + Cl- (aq)对于该反应,溶解的每摩尔AgCl产生1摩尔Ag+和Cl-。溶解度将等于银离子或氯离子的浓度。
solubility = [Ag+] = [Cl-]要找到这些浓度,请记住溶解度积的公式:
Ksp = [A]c[B]d所以,对于反应AB↔ cA+dB:
Ksp = [Ag+][Cl-]由于[Ag+]=[Cl-]:
Ksp = [Ag+]2 = 1.6 x 10-10 [Ag+] = (1.6 x 10-10)½ [Ag+] = 1.26 x 10-5 M solubility of AgCl = [Ag+] solubility of AgCl = 1.26 x 10-5 MBaF2
BaF2在水中的离解反应为:
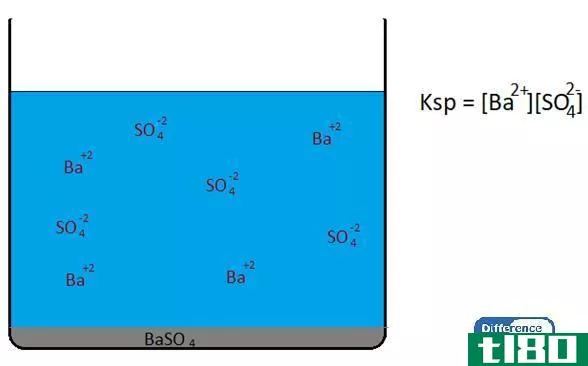
BaF2 (s) ↔ Ba+ (aq) + 2 F- (aq)溶解度等于溶液中钡离子的浓度。对于形成的每摩尔Ba+离子,产生2摩尔F-离子,因此:
[F-] = 2 [Ba+] Ksp = [Ba+][F-]2 Ksp = [Ba+](2[Ba+])2 Ksp = 4[Ba+]3 2 x 10-6 = 4[Ba+]3 [Ba+]3 = ¼(2 x 10-6) [Ba+]3 = 5 x 10-7 [Ba+] = (5 x 10-7)1/3 [Ba+] = 7.94 x 10-3 M solubility of BaF2 = [Ba+] solubility of BaF2 = 7.94 x 10-3 M答案
- 氯化银AgCl在25℃下的溶解度为1.26 x 10-5 M。
- 氟化钡BaF2在25℃下的溶解度为3.14 x 10-3 M。
- 发表于 2021-09-21 19:56
- 阅读 ( 137 )
- 分类:化学
你可能感兴趣的文章
ksp公司(ksp)和凯克(keq)的区别
Ksp和Keq之间的关键区别在于Ksp一词描述了物质的溶解度,而Keq一词描述了特定反应的平衡状态。 Ksp代表溶度积常数,Keq代表平衡常数。Ksp也是一种平衡常数,但它只涉及固体物质的溶解度。Keq是一个更一般的术语,我们可以...
- 发布于 2020-10-12 08:40
- 阅读 ( 536 )
摩尔溶解度(molar solubility)和产品溶解度常数(product solubility constant)的区别
摩尔溶解度和产品溶解度常数之间的关键区别在于摩尔溶解度描述了每升溶液中物质的溶解,而产品溶解度常数描述了固体物质在水溶液中的溶解。 摩尔溶解度和产物溶解度常数都是描述物质在溶液中溶解的化学概念。我们...
- 发布于 2020-10-15 10:26
- 阅读 ( 1101 )
溶解度(solubility)和溶解度积(solubility product)的区别
溶解度和溶解度积之间的关键区别在于溶解度描述了一种物质在溶剂中的溶解,而溶解度积则描述了溶解离子浓度的数学乘积,其值为其化学计量系数的幂次方。 根据上述区别,溶解度和溶度积是两个相关的术语。因此,我...
- 发布于 2020-10-17 23:41
- 阅读 ( 645 )
ksp公司(ksp)和qsp公司(qsp)的区别
...数,Qsp是溶度积商。Ksp和Qsp的关键区别在于Ksp表示物质的溶解度,而Qsp表示溶液的当前状态。溶解度积是当一种物质溶解在诸如水这样的溶剂中时,溶液中离子种类浓度的乘积。 溶解度积是在溶液被该物质饱和时测定的。在饱...
- 发布于 2020-10-19 02:41
- 阅读 ( 414 )
离子产物(ionic product)和溶解度积(solubility product)的区别
关键区别-离子产物与溶解度乘积 离子积和溶解度积表达了溶液中离子种类浓度乘积的相同概念。离子积和溶度积的关键区别在于离子积是离子在不饱和或饱和溶液中的乘积,而溶度积是离子在饱和溶液中的乘积。 溶解度积...
- 发布于 2020-10-19 02:48
- 阅读 ( 504 )
饱和的(saturated)和过饱和溶液(supersaturated solution)的区别
...“过饱和度”这两个化学性质主要取决于溶质在溶剂中的溶解度。在给定的温度下,溶质在特定溶剂中的溶解度是常数(Q)。 Q被定义为溶质的离子产物。 示例:AgCl在水中的溶解度(QAgCl)=[Ag+][Cl–] 一般来说,如果我们继续向...
- 发布于 2020-10-25 10:24
- 阅读 ( 905 )
溶质(solute)和溶剂(solvent)的区别
... 均质混合物是溶质完全均匀地溶解在溶液中的溶液。而溶解度是物质溶解成另一种物质的能力。在本指南中,我们将讨论溶质和溶剂的区别和特点。 对比图 根据 溶质 溶剂 意义 在溶液或混合物中溶解在溶剂中的物质称为...
- 发布于 2021-07-08 07:32
- 阅读 ( 512 )
常见的一般化学问题列表
...标准差 科学符号 重要人物 由百分比组成的最简单公式 溶解度积的溶解度 溶解度积 温度转换 温度转换开尔文到摄氏度和华氏度 温度转换摄氏度到华氏度 温度转换摄氏度到开尔文 温度转换开尔文到摄氏度 温度从华氏到摄氏的...
- 发布于 2021-09-08 10:26
- 阅读 ( 255 )
测定浓度和摩尔浓度
...浓度是化学中最常见和最重要的浓度单位之一。这个浓度问题说明了如果你知道有多少溶质和溶剂存在,如何找到溶液的摩尔浓度。 浓度和摩尔浓度示例问题 通过将20.0 g NaOH溶解在足够的水中以产生482 cm3溶液来测定溶液的...
- 发布于 2021-09-15 09:43
- 阅读 ( 160 )
万圣节反应还是老拿骚反应
...化物离子→ I-+3SO42-+3H+ 当碘化物离子的浓度足以使HgI2的溶解度积超过4.5 x 10-29 mol3 dm-9时,橙色碘化物汞(II)沉淀,直到Hg2+离子被消耗(假设I-离子过量):Hg2++2 I-→ HgI2(橙色或黄色) 如果I-和IO3-离子残留,则发生碘化物-碘...
- 发布于 2021-09-21 03:55
- 阅读 ( 207 )