Ksp和Keq之间的关键区别在于Ksp一词描述了物质的溶解度,而Keq一词描述了特定反应的平衡状态。
Ksp代表溶度积常数,Keq代表平衡常数。Ksp也是一种平衡常数,但它只涉及固体物质的溶解度。Keq是一个更一般的术语,我们可以用来确定任何类型的平衡态的性质。
目录
1. 概述和主要区别
2. 什么是Ksp
3. 什么是Keq
4. 并列比较——Ksp与Keq表格形式
5. 摘要
什么是ksp公司(ksp)?
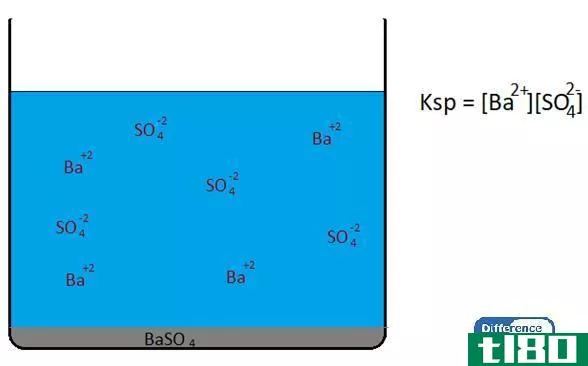
Ksp代表溶度积常数。适用于固体物质在水溶液中的溶解。这个常数描述了化学物质在水溶液中溶解的程度。溶解度越高,Ksp值越高。对于一般溶解度反应,我们可以给出Ksp的方程如下:
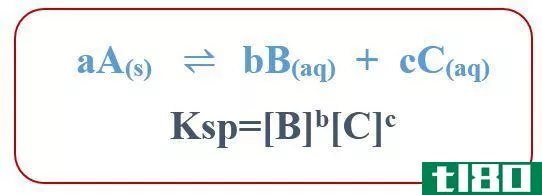
因此,溶解度积常数来自固体物质溶解产物摩尔浓度的乘积。但是,如果反应物和产物之间存在化学计量关系,我们必须在方程中包含化学计量系数。有必要将产物浓度提高到系数幂。
共离子效应:
我们应该永远记住,平衡反应的溶解度会因共离子效应而降低。例如,如果溶液中有一个公共离子,而我们要溶解在该溶液中的固体化合物,我们可以观察到比预期更低的Ksp。如果没有这个离子,Ksp值会很大。
盐效应:
溶液中不寻常离子的存在也会影响平衡的Ksp。例如,如果溶液中除了固体中存在的离子外,还有一种盐离子,那么我们称之为稀有离子,它可以增加Ksp的值。
什么是凯克(keq)?
Keq代表平衡常数。平衡常数是平衡时产物浓度与反应物浓度之比。这个术语只适用于处于平衡状态的反应。对于处于平衡状态的反应,反应商和平衡常数是相同的。
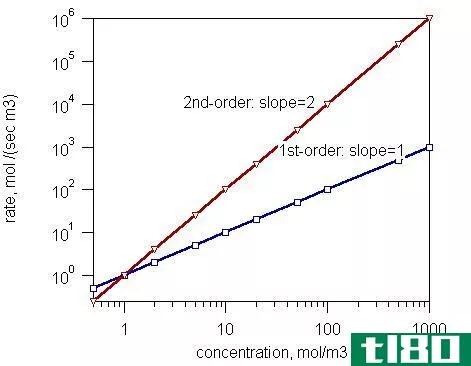
当浓度上升到化学计量系数的幂次时,我们可以给出平衡常数。由于温度影响组分的溶解度和体积膨胀,平衡常数取决于所考虑体系的温度。然而,平衡常数的方程式不包括反应物或产物中固体的任何细节。只考虑液相和气相的物质。
例如,让我们考虑碳酸和碳酸氢根离子之间的平衡。
H2CO3(水)↔ HCO3–(aq)+H+(aq)
上述反应的平衡常数如下所示。
平衡常数(K)=[HCO3–(aq)][H+(aq)]/[H2CO3(aq)]
ksp公司(ksp)和凯克(keq)的区别
Ksp是Keq的一种。Ksp代表溶度积常数,Keq代表平衡常数。Ksp和Keq之间的关键区别在于Ksp一词描述了物质的溶解度,而Keq一词描述了特定反应的平衡状态。当考虑方程时,Ksp只得到固体溶解后的产物,而Keq则同时含有水溶液中的产物和反应物。所以,这是Ksp和Keq的另一个显著区别。

总结 - ksp公司(ksp) vs. 凯克(keq)
Ksp是Keq的一种。Ksp代表溶度积常数,Keq代表平衡常数。Ksp和Keq之间的关键区别在于Ksp一词描述了物质的溶解度,而Keq一词描述了特定反应的平衡状态。