饱和的(saturated)和过饱和溶液(supersaturated solution)的区别
在进行饱和和过饱和溶液之间差异的复杂分析之前,让我们先简单地看一下饱和的概念。溶液是通过在溶剂中溶解溶质而制成的。溶剂中的“饱和”和“过饱和度”这两个化学性质主要取决于溶质在溶剂中的溶解度。在给定的温度下,溶质在特定溶剂中的溶解度是常数(Q)。
Q被定义为溶质的离子产物。
示例:AgCl在水中的溶解度(QAgCl)=[Ag+][Cl–]
一般来说,如果我们继续向溶剂中添加溶质,在溶剂中可以添加的溶质有一个最大量。达到一定限度后,溶质开始在溶剂中沉淀。在这个极限之后,它变成了一个过饱和解。当我们能溶解溶质而不形成沉淀时,它被称为饱和溶液。
饱和和过饱和之间的关键区别在于,饱和是指一种物质的溶液不能再溶解该物质的状态,并且它的额外量将作为一个单独的相出现,而过饱和是一种溶液的状态,它含有的溶解物质比能被溶解的物质要多正常情况下有溶剂。
什么是饱和溶液(a saturated solution)?
在溶剂中无限溶解的化合物数量非常有限;这意味着,我们可以在溶剂中以任何比例混合溶质而不形成沉淀物。然而,大多数溶质并不是无限不溶的;如果你往溶剂中加入更多的溶质,它们会形成沉淀。
饱和溶液中含有的溶质分子数量最多,不需要沉淀即可溶解。
什么是过饱和溶液(a supersaturated solution)?
如果向饱和溶液中添加额外的溶质,就会形成过饱和溶液。换句话说,这是饱和溶液中的条件,当你在溶液中加入一些额外的溶质。然后它会在溶液中形成沉淀,因为溶剂已经超过了它能溶解的最大溶质分子量。如果你提高溶剂的温度,你可以通过溶解溶质分子而得到饱和溶液。

糖在水中的过饱和使冰糖得以形成。
饱和的(saturated)和过饱和溶液(supersaturated solution)的区别
饱和和过饱和溶液的定义
饱和溶液:在特定温度下,如果溶液中含有的溶质分子量与溶剂所能容纳的量相同,则称之为饱和溶液。
过饱和溶液:在特定温度下,如果溶液中含有更多的溶质分子,则称其为过饱和溶液。
化学解释
对于饱和溶液;Q=Ksp(无沉淀)
对于过饱和溶液;Q>;Ksp(将形成沉淀)
哪里;
Q=溶解度(反应商)
K sp=溶解度积(溶解离子浓度的数学乘积,等于其化学计量系数的幂次方)
示例:考虑在水中溶解氯化银(AgCl)。
氯化银-溶质和水-溶剂

氯化银溶于水大量氯化银溶于水。
溶液清澈沉淀物清晰可见
Q=[Ag+][Cl–]=Ksp Q=[Ag+][Cl–]>;Ksp
哪里,
[Ag+]=水中Ag+的浓度
[Cl-]=水中Cl-的浓度
对于AgCl,Ksp=1.8×10–10 mol2dm-6
我们怎样才能得到饱和和过饱和溶液?
饱和溶液和过饱和溶液都是在你不断向溶剂中加入某种特定的溶质时形成的。在给定的温度下,首先形成不饱和溶液,然后形成饱和溶液,最后形成过饱和溶液。
例:在水中溶解盐
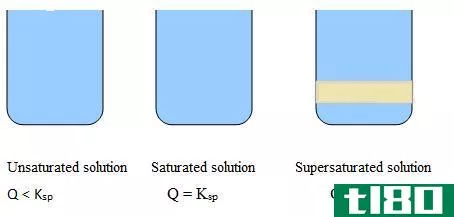 Unsaturated Solution: Less amount of salt in water, clear solution, no precipitation.
Unsaturated Solution: Less amount of salt in water, clear solution, no precipitation.
饱和溶液:最大量的盐溶于水,溶液颜色略有变化,但无沉淀。
过饱和溶液:水溶盐较多,溶液浑浊,可见沉淀。
Image Courtesy: