饱和键和不饱和键的关键区别在于饱和键没有π键,而非饱和键总是有π键。
化学键是原子间的键。这些键导致分子的形成。有两种主要的键,它们是共价键和离子键。然而,金属中的键是金属键。两个原子共用价电子时形成共价键。这些共价键可以是饱和的,也可以是不饱和的,这取决于两个原子之间存在的键的数量和类型。
目录
1. 概述和主要区别
2. 什么是饱和键
3. 什么是不饱和键
4. 并列比较-表格形式的饱和键与不饱和键
5. 摘要
什么是饱和键(saturated bonds)?
饱和键是单键。这些是共价化学键。在那里,两个原子通过sigma键相互结合,因此,没有π键-这种键包括两个电子;形成这种键的两个原子各有一个电子。这些电子是原子的价电子。这种类型的粘结强度相对较弱。两个共享的电子存在于原子之间,负电荷越大的原子将把电子吸引到自己身上。

图01:甲烷是一种饱和化合物,因为它有四个饱和键
此外,这种键具有旋转的能力。在那里,这个键充当旋转轴。当下列轨道相互重叠时,就会形成饱和键。
- 两个s轨道
- 两个pz轨道
- S和pz轨道
- 两个dz2轨道
- 杂化轨道的线性重叠。
什么是不饱和键(unsaturated bonds)?
不饱和键是两个原子之间的双键和三键。这些是共价键。因此,原子之间共享电子。此外,还有sigma键和pi键。在双键中,两个原子之间有一个σ键和一个π键。在三键中,有一个sigma键和两个π键。sigma键是由于原子轨道的线性重叠而形成的,而pi键是由于平行重叠而形成的。

图02:双键的形成
另外,双键在原子间有四个键电子,而三键在那里有六个电子。由于不饱和键合中原子间有大量电子,这些键往往更具活性。此外,与单一债券相比,这些债券更坚固、更短。
饱和的(saturated)和不饱和键(unsaturated bonds)的区别
饱和键是单键,不饱和键是两个原子之间的双键和三键。饱和键和不饱和键的关键区别在于饱和键没有π键,而非饱和键总是有π键。饱和键和不饱和键之间的另一个区别是饱和键中的两个原子之间有一个电子对,而在不饱和键中原子之间有两个或三个电子对。
此外,饱和键和不饱和键的一个重要区别是饱和键相对较弱、较长且反应性较小,而不饱和键则强、短、反应性强。此外,饱和键可以旋转,而不饱和键则不能。
下面的信息图是饱和键和不饱和键之间区别的比较总结。
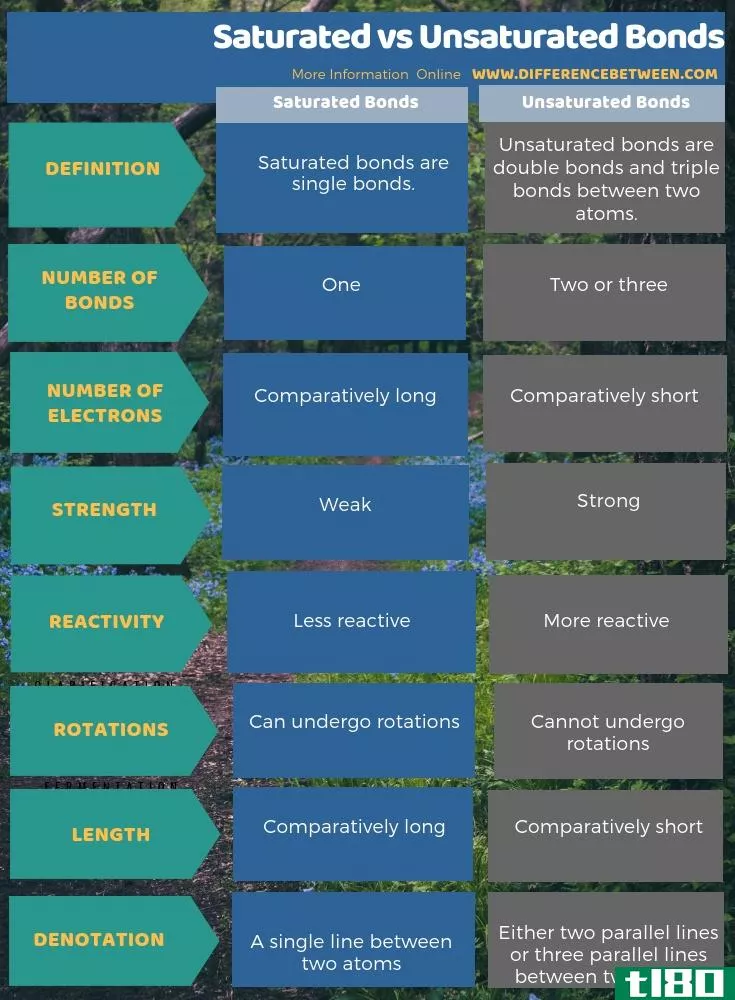
总结 - 饱和的(saturated) vs. 不饱和键(unsaturated bonds)
总之,饱和键是单共价键,而不饱和键是双键和三键。因此,饱和键和不饱和键的关键区别在于饱和键没有π键,而非饱和键总是有π键。
引用
1Helmenstine,Anne-Marie博士,“化学中的双键定义和示例”,ThoughtCo,2017年9月8日。这里有2个。大英百科全书的编辑。“三重债券”,《大英百科全书》,大英百科全书,2011年4月14日。此处提供
2大英百科全书的编辑。“三重债券”,《大英百科全书》,大英百科全书,2011年4月14日。