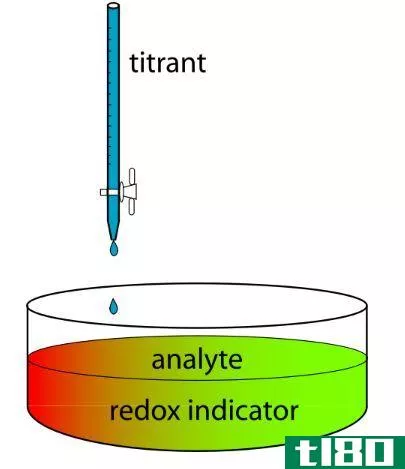
酸碱滴定曲线
强酸滴定曲线

第一条曲线显示强酸被强碱滴定。初始pH值缓慢上升,直到反应接近添加足够的碱中和所有初始酸的点。这一点称为等价点。对于强酸/强碱反应,这在pH=7时发生。当溶液通过等效点时,当溶液接近滴定溶液的pH值时,pH值的增加速度减慢。

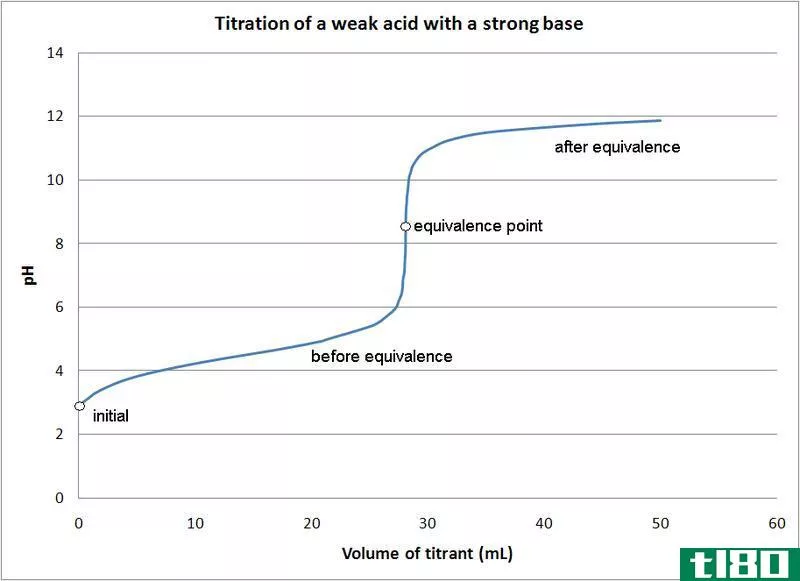
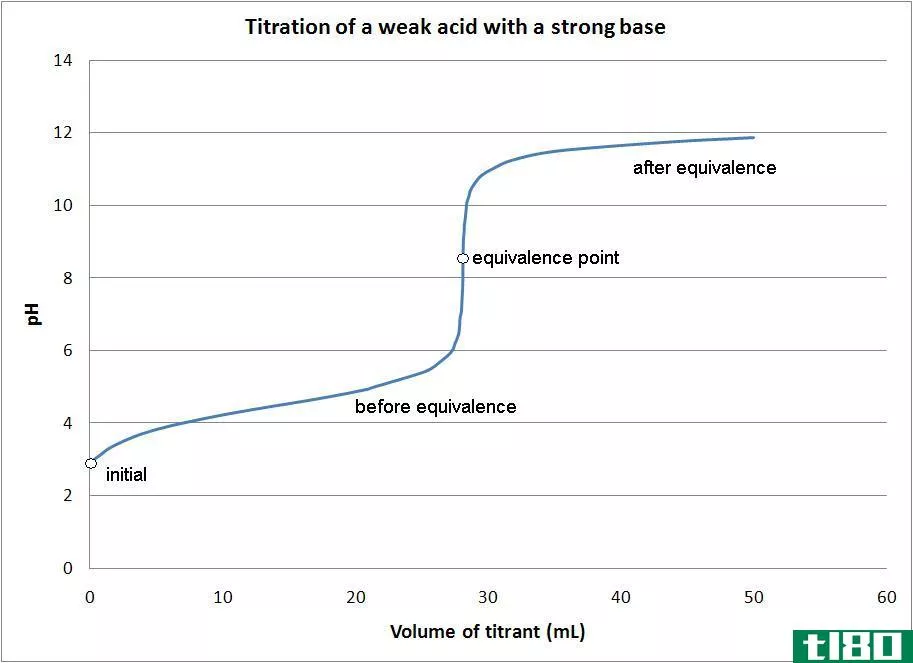
弱酸强碱

弱酸只与盐部分分离。一开始pH值会正常升高,但当它到达溶液似乎被缓冲的区域时,斜率会变平。在该区域之后,pH值通过其等效点急剧上升,并像强酸/强碱反应一样再次稳定下来。
关于这条曲线,有两点需要注意。
第一个是半等值点。这一点发生在缓冲区的中间,缓冲区的pH值在大部分时间内几乎没有变化基地补充。半当量点是当添加的碱刚好足以使一半的酸转化为共轭碱时。当这种情况发生时,H+离子的浓度等于酸的Ka值。更进一步,pH=pKa。
第二点是较高的等效点。一旦酸被中和,注意该点高于pH=7。当弱酸被中和时,剩下的溶液是碱性的,因为酸的共轭碱留在溶液中。
多元酸和强碱

第三张图是由含有一个以上H+离子的酸生成的。这些酸被称为多元酸。例如,硫酸(H2SO4)是一种二元酸。它有两个氢离子,它可以放弃。
第一个离子在水中会因离解而断裂
H2.所以4.→ H++hso4.-第二个H+来自HSO4-的分解
HSO4.-→ H++所以4.2-这基本上是一次滴定两种酸。该曲线显示了与弱酸滴定相同的趋势,其中pH值在一段时间内不会发生变化,会出现峰值并再次趋于稳定。当第二次酸反应发生时,差异就出现了。同样的曲线再次出现,pH值缓慢变化后出现峰值并趋于稳定。
每个“驼峰”都有自己的半等效点。第一个驼峰点出现在向溶液中添加足够的碱,以将第一次解离的一半H+离子转化为其共轭碱或其Ka值时。
第二个驼峰的半当量点出现在二次酸的一半转化为二次共轭碱或该酸的Ka值的点上。
在许多酸的Ka表中,这些将被列为K1和K2。其他表格仅列出解离过程中每种酸的Ka。
这张图显示了一种二元酸。对于含有更多氢离子的酸[例如,含有3个氢离子的柠檬酸(H3C6H5O7)],该图将有第三个驼峰,在pH=pK3时有半个等效点。
- 发表于 2021-09-25 03:11
- 阅读 ( 215 )
- 分类:科学
你可能感兴趣的文章
酸度(acidity)和水的碱度(alkalinity of water)的区别
水的酸碱性的关键区别在于,水的酸性是水中和碱的能力,而水的碱度决定了水中和酸的能力。 我们可以将水的酸性称为“碱中和能力”,将水的碱度称为“酸中和能力”。我们可以通过实验室实验来确定这两个参数。这对...
- 发布于 2020-09-15 13:04
- 阅读 ( 813 )
正态性因子(normality factor)和滴定误差(titration error)的区别
...度最简单的方法是使用溶液的摩尔浓度。例如,1M硫酸在酸碱反应中有2N当量,因为一个硫酸分子可以产生两摩尔氢离子。然后我们可以用摩尔浓度除以当量浓度来确定当量系数;例如,硫酸的当量系数是2。然而,确定正态性因...
- 发布于 2020-09-20 09:32
- 阅读 ( 396 )
半等价点(half equivalence point)和等效点(equivalence point)的区别
...1:指示等效点的滴定曲线 在NaOH和HCl的反应中,这是一个酸碱反应,我们可以用NaOH或HCl作为已知浓度的滴定剂。在这里,滴定剂被放置在滴定管中,我们可以慢慢地将其添加到滴定和/分析物中,直到反应混合物发生颜色变化。...
- 发布于 2020-09-22 11:49
- 阅读 ( 1174 )
酸碱度(ph)和可滴定酸度(titratable acidity)的区别
...比较——pH值与可滴定酸度的表格形式 5. 摘要 什么是酸碱度(ph)? pH值是溶液中游离质子(H+离子)浓度的测量值。这些质子是与酸分离的氢离子。因此,通过测量溶液的pH值,我们可以测量溶液的酸强度。这意味着我们可以测...
- 发布于 2020-09-30 01:01
- 阅读 ( 975 )
滴定法(titration)和中和(neutralization)的区别
...能得到pH值为7的中和溶液。其他反应产生的中和溶液由于酸碱的pH值变化而变化。 滴定法(titration)和中和(neutralization)的区别 滴定和中和是化学中非常重要的术语。滴定法是一种需要特定仪器的技术,它是在中和反应的基础上进...
- 发布于 2020-09-30 23:44
- 阅读 ( 560 )
酸碱滴定法(acid-base titration)和氧化还原滴定(redox titration)的区别
主要区别-酸碱滴定与氧化还原滴定 通常,滴定法用于测定未知溶液(分析物)的浓度。最常用的两种滴定方法是酸碱滴定法和氧化还原滴定法。酸碱滴定和氧化还原滴定的关键区别在于滴定过程中滴定剂和被分析物之间发生...
- 发布于 2020-10-06 00:15
- 阅读 ( 663 )
标准化(standardization)和滴定法(titration)的区别
...,我们使用一级标准溶液。这些溶液含有高纯度。 图01:酸碱滴定法 当我们用固体化合物配制溶液时。该溶液的最终浓度可能因化合物纯度、仪器误差、人为误差等几个因素而变化。例如,如果我们想制备1.0 molL-1的EDTA溶液,我...
- 发布于 2020-10-15 07:31
- 阅读 ( 1231 )
稀释(dilution)和滴度(titre)的区别
...最低条件。滴定是我们用来测定溶液浓度的过程。 图02:酸碱滴定装置 滴定试验采用酸碱中和反应。有许多物理现象,如颜色变化、pH值变化、电导率和沉淀等,它们标志着反应的终点或达到的浓度阈值。此外,动物脂肪的滴度...
- 发布于 2020-10-17 07:34
- 阅读 ( 777 )
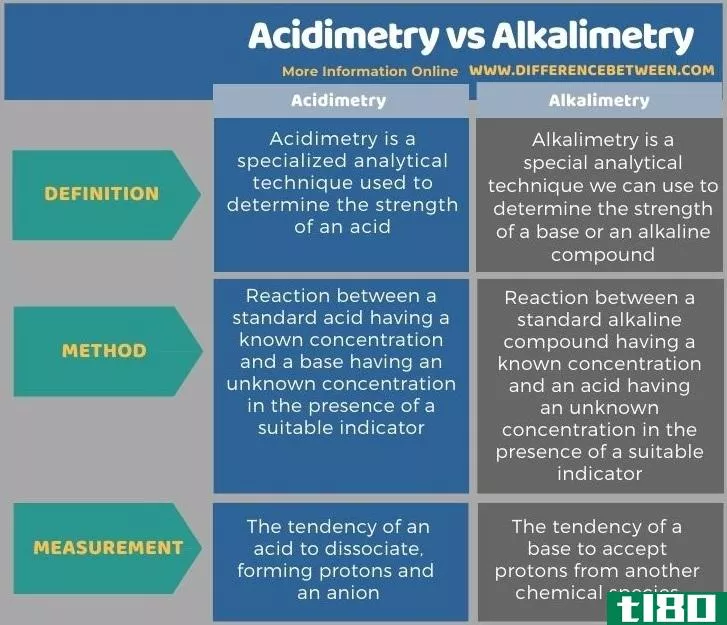
酸度测定法(acidimetry)和碱度测定法(alkalimetry)的区别
...是一种专门的分析技术,用于测定酸的强度。我们可以在酸碱滴定中使用这种技术来测定碱性或碱性物质的浓度。但是,我们需要使用标准酸溶液进行测定。它包括中和反应。这种反应技术在容量分析过程中很有用。 在酸度测...
- 发布于 2021-03-04 16:53
- 阅读 ( 260 )
酸碱滴定法(acid-base titration)和氧化还原滴定(redox titration)的区别
酸碱滴定法的主要区别(main difference acidbase titration) vs. 氧化还原滴定(redox titration) 滴定法是一种广泛应用的实验室技术,通过其浓度对化学分析物进行定量。这是用一套特殊仪器来完成的。一般来说,它是在两种液体溶...
- 发布于 2021-06-27 11:22
- 阅读 ( 345 )