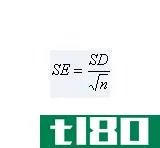正态性因子与滴定误差的关键区别在于,正态性因子给出了观测值与理论值的比值,而滴定误差给出了观测终点与实际终点之间的差值。
在分析化学中,正态系数和滴定误差是确定同一实验中观察结果与理论真实结果的偏差的重要因素。
目录
1. 概述和主要区别
2. 什么是正态系数
3. 什么是滴定误差
4. 并排比较-正态性系数与表格形式的滴定误差
5. 摘要
什么是正态因子(normality factor)?
正态系数是溶液制备过程中观测值与理论重量值的比值。换言之,正态性因子是指在制备已知正态性值的理想溶液时,溶质的观察重量与溶质理论重量之间的比率。
溶液的当量是指一公升溶液中溶质的克当量重量。因此,我们可以把它命名为当量浓度。常态的符号是“N”。通常,当量的计量单位是eq/L(相当于每升)。对于非常小的量,我们可以用meq/L(毫当量每升)的单位。
计算溶液当量浓度最简单的方法是使用溶液的摩尔浓度。例如,1M硫酸在酸碱反应中有2N当量,因为一个硫酸分子可以产生两摩尔氢离子。然后我们可以用摩尔浓度除以当量浓度来确定当量系数;例如,硫酸的当量系数是2。然而,确定正态性因子的最精确方法是计算溶液中存在的溶质的观测重量和理论重量。
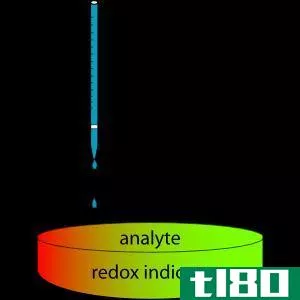
什么是滴定误差(titration error)?
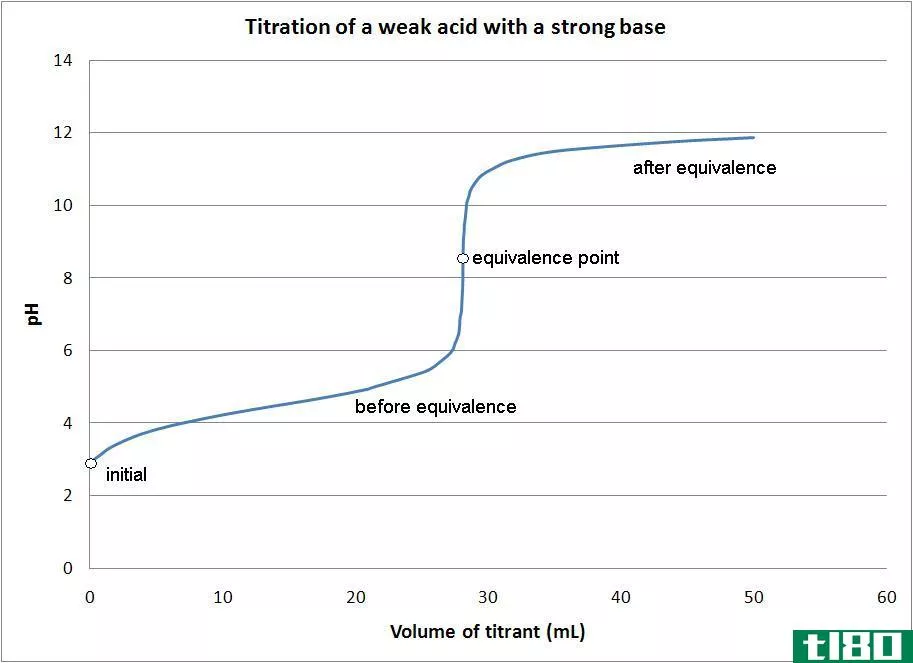
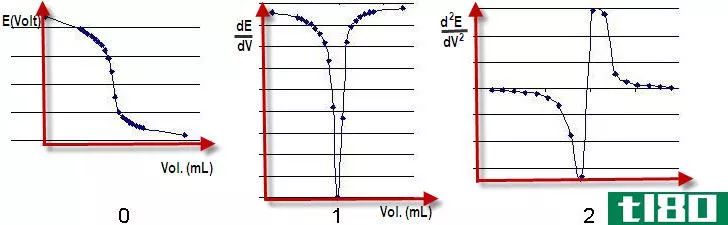
滴定误差是滴定终点与滴定当量点之间的差值。换句话说,滴定误差是指终点的体积高于或低于当量点。滴定终点是观察到的使颜色发生变化的反应的终点。
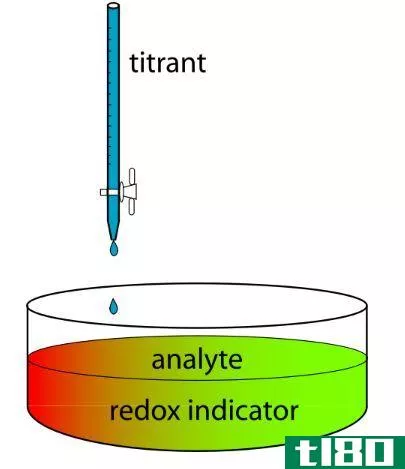
然而,当量点是滴定瓶中反应停止的确切体积。滴定终点是根据滴定中使用的指示剂,反应结束的点。
正态性因子(normality factor)和滴定误差(titration error)的区别
正态系数和滴定误差这两个术语描述了从特定实验获得的结果相对于理论计算结果的变化。正态性因子与滴定误差的关键区别在于,正态性因子给出了观测值与理论值的比值,而滴定误差给出了观测终点与实际终点之间的差值。
正态性因子是比值,而滴定误差是两个值之间的差值。
以下信息图总结了正态系数和滴定误差之间的差异。

总结 - 正态性因子(normality factor) vs. 滴定误差(titration error)
在分析化学中,正态系数和滴定误差是确定同一实验中观察结果与理论真实结果的偏差的重要因素。正态性因子与滴定误差的关键区别在于,正态性因子给出了观测值与理论值的比值,而滴定误差给出了观测终点与实际终点之间的差值。
引用
1赫尔曼斯汀,安妮·玛丽。“如何计算正态性(化学)。”ThoughtCo,2020年2月11日,