在滴定标准溶液中,我们加入的滴定量和标准溶液的量是相等的。
滴定法是我们主要在分析化学中用来测定样品中分析物含量的技术。这些分析物包括酸、碱、氧化剂、还原剂和金属离子。
目录
1. 概述和主要区别
2. 什么是滴定
3. 什么是返滴定法
4. 并列比较-以表格形式滴定与反滴定
5. 摘要
什么是滴定法(titration)?
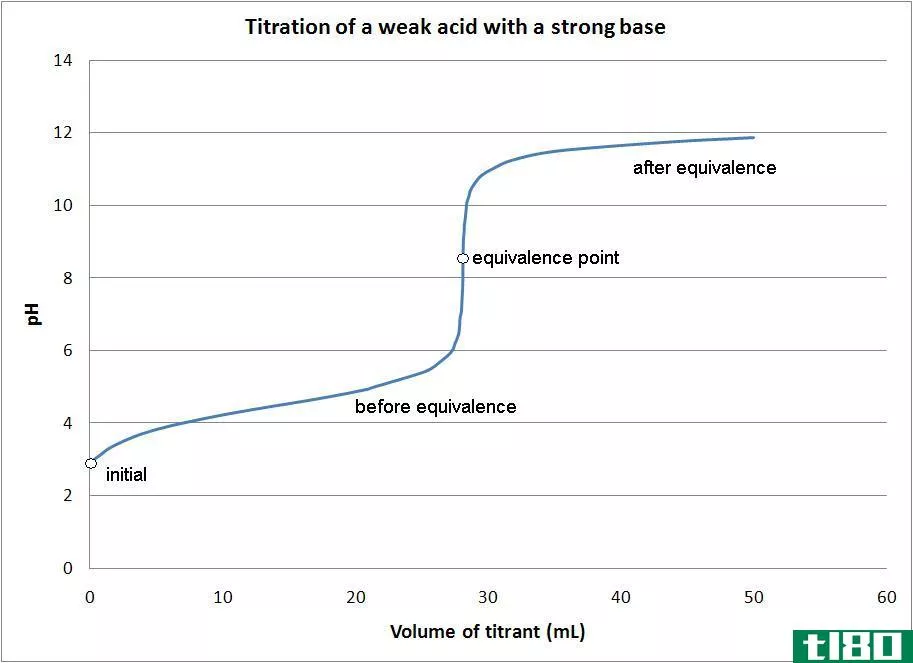
在滴定中,会发生已知的化学反应。在这里,分析物与标准试剂反应,我们称之为“滴定剂”。在滴定中应使用理想的标准溶液,它应具有化学稳定性和与被分析物迅速、完全反应的能力。
在滴定法中,有时我们使用一种高纯度和稳定的一级标准溶液作为参考物质。然后,如果我们能找到与分析物完全反应的滴定液的体积或质量,就可以确定被分析物的数量。

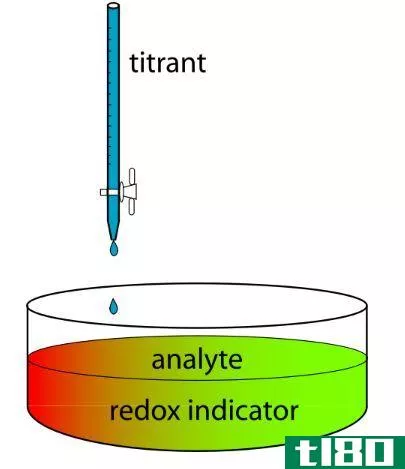
图01:滴定装置
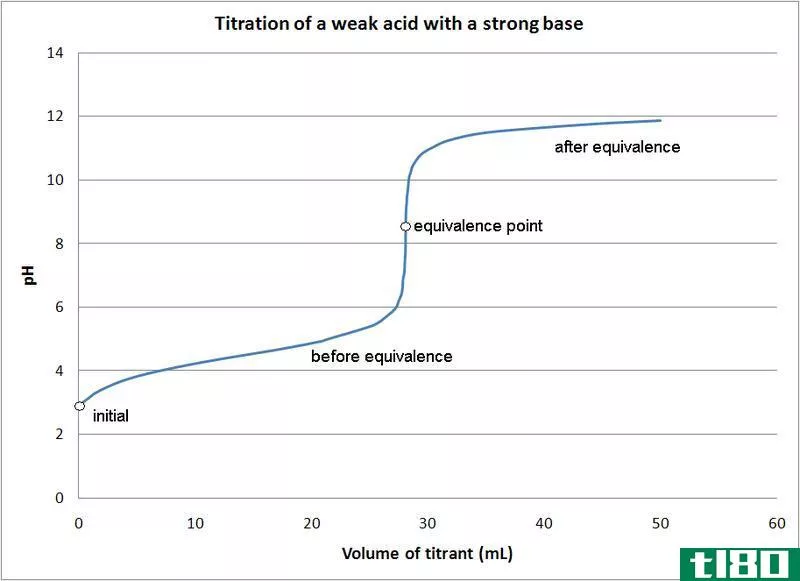
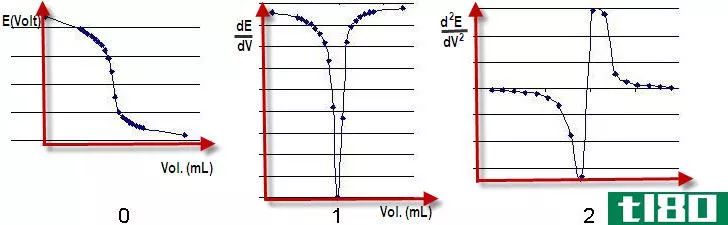
在滴定中,滴定剂在滴定管中,我们使用吸管将分析物添加到滴定瓶中。反应在滴定瓶中进行。在任何滴定中,反应完成的点(化学当量点)就是滴定的终点。我们可以用一个指示器来检测终点,它可以改变终点的颜色。或者我们可以利用仪器反应的变化来确定终点;例如,电位和电导率。
滴定也有一些错误。滴定中的当量点是指添加的滴定剂与样品中的分析物在化学上完全等效的点。然而,这是一个理论上的观点,我们不能准确地用实验来测量。我们只能观察终点。在理想情况下,终点并不完全等于当量点(滴定误差),但我们尽量使两者之间的差距最小化。也可能存在与此方法相关的人为错误。因此,为了减少这些,我们通常需要重复滴定至少三次。然后我们可以确定平均值。
什么是反滴定(back titration)?
在反滴定法中,我们向分析物中加入过量的标准滴定剂。然后,一定量的标准滴定液将与被分析物发生反应,过量的标准滴定液仍保留在样品中。在这里,我们可以用反滴定法测定标准试剂的剩余量。
例如,可以用这种方法测定样品中的磷酸盐含量。当我们在磷酸盐样品中加入过量的硝酸银时,两者都会反应生成固体磷酸银。然后用硫氰酸钾滴定过量的硝酸银。因此,添加的硝酸银总量等于磷酸盐离子的量和我们用于反滴定的硫氰酸盐的量。
滴定法(titration)和反滴定(back titration)的区别
滴定法是一种用于定量测定样品中被分析物含量的分析技术。另一方面,反滴定法是滴定技术的一种先进形式,它能使滴定结果更加准确。然而,滴定法和反滴定法的关键区别在于,在滴定法中,我们通常向分析物中添加等量的标准溶液,而在反滴定法中,我们向分析物中添加过量的标准溶液。
此外,在正常滴定的样品中,只有一种化学反应发生。然而,在反滴定法中,同一样品中会发生两种化学反应。因此,在常规滴定中,我们只需要一个步骤,而在反向滴定中,我们需要执行两个滴定程序。因此,这也是滴定和反滴定的重要区别。

总结 - 滴定法(titration) vs. 反滴定(back titration)
滴定是非常重要的分析技术。有不同类型的分析技术,如氧化还原滴定法、电位滴定法、电导滴定法等,反滴定法就是其中之一。在滴定法中,我们通常向被分析物中添加等量的标准溶液,而在反滴定法中,我们向分析物中添加过量的标准溶液。所以,这就是滴定和反滴定的关键区别。
引用
1“滴定法”,化学剧本,歌词,2019年6月3日,可在这里查阅。