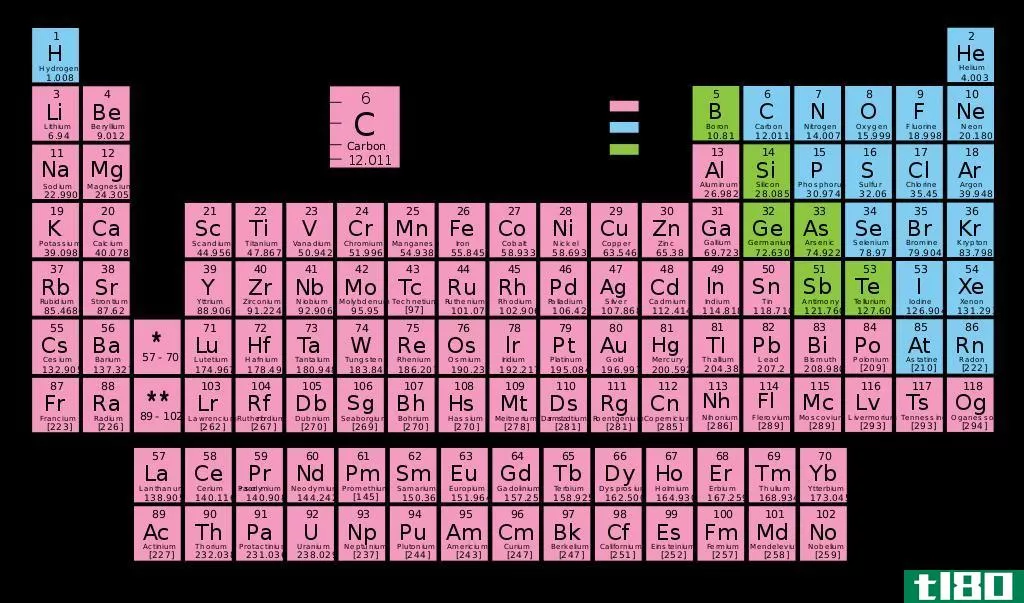
元素的价态化学表
你可以假设元素的价,原子与之结合或形成的电子数,是那些可以通过观察周期表的组(列)得到的。虽然这些是最常见的价态,但电子的真实行为却不那么简单。


这是一张元素价表。记住,通过填充、清空或半填充外壳,元素的电子云将变得更加稳定。此外,壳层不会整齐地堆叠在另一个之上,因此不要总是假设一种元素的价态是由其外壳中的电子数决定的。
元素价表
| 数字 | 要素 | 原子价 |
| 1. | 氢 | (-1), +1 |
| 2. | 氦 | 0 |
| 3. | 锂 | +1 |
| 4. | 铍 | +2 |
| 5. | 硼 | -3, +3 |
| 6. | 碳 | (+2), +4 |
| 7. | 氮 | -3, -2, -1, (+1), +2, +3, +4, +5 |
| 8. | 氧气 | -2 |
| 9 | 氟 | -1, (+1) |
| 10 | 霓虹的 | 0 |
| 11 | 钠 | +1 |
| 12 | 镁 | +2 |
| 13 | 铝 | +3 |
| 14 | 硅 | -4, (+2), +4 |
| 15 | 磷 | -3, +1, +3, +5 |
| 16 | 硫黄 | -2, +2, +4, +6 |
| 17 | 氯 | -1, +1, (+2), +3, (+4), +5, +7 |
| 18 | 氩 | 0 |
| 19 | 钾 | +1 |
| 20 | 钙 | +2 |
| 21 | 钪 | +3 |
| 22 | 钛 | +2, +3, +4 |
| 23 | 钒 | +2, +3, +4, +5 |
| 24 | 铬 | +2, +3, +6 |
| 25 | 锰 | +2, (+3), +4, (+6), +7 |
| 26 | 铁 | +2, +3, (+4), (+6) |
| 27 | 钴 | +2, +3, (+4) |
| 28 | 镍 | (+1), +2, (+3), (+4) |
| 29 | 铜 | +1, +2, (+3) |
| 30 | 锌 | +2 |
| 31 | 镓 | (+2). +3. |
| 32 | 锗 | -4, +2, +4 |
| 33 | 砷 | -3, (+2), +3, +5 |
| 34 | 硒 | -2, (+2), +4, +6 |
| 35 | 溴 | -1, +1, (+3), (+4), +5 |
| 36 | 氪 | 0 |
| 37 | 铷 | +1 |
| 38 | 锶 | +2 |
| 39 | 钇 | +3 |
| 40 | 锆 | (+2), (+3), +4 |
| 41 | 铌 | (+2), +3, (+4), +5 |
| 42 | 钼 | (+2), +3, (+4), (+5), +6 |
| 43 | 锝 | +6 |
| 44 | 钌 | (+2), +3, +4, (+6), (+7), +8 |
| 45 | 铑 | (+2), (+3), +4, (+6) |
| 46 | 钯 | +2, +4, (+6) |
| 47 | 银 | +1, (+2), (+3) |
| 48 | 镉 | (+1), +2 |
| 49 | 铟 | (+1), (+2), +3 |
| 50 | 锡 | +2, +4 |
| 51 | 锑 | -3, +3, (+4), +5 |
| 52 | 碲 | -2, (+2), +4, +6 |
| 53 | 碘 | -1, +1, (+3), (+4), +5, +7 |
| 54 | 氙气 | 0 |
| 55 | 铯 | +1 |
| 56 | 钡剂 | +2 |
| 57 | 镧 | +3 |
| 58 | 铈 | +3, +4 |
| 59 | 镨 | +3 |
| 60 | 钕 | +3, +4 |
| 61 | 镨 | +3 |
| 62 | 钐 | (+2), +3 |
| 63 | 铕 | (+2), +3 |
| 64 | 钆 | +3 |
| 65 | 铽 | +3, +4 |
| 66 | 镝 | +3 |
| 67 | 钬 | +3 |
| 68 | 铒 | +3 |
| 69 | 铥 | (+2), +3 |
| 70 | 镱 | (+2), +3 |
| 71 | 镥 | +3 |
| 72 | 铪 | +4 |
| 73 | 钽 | (+3), (+4), +5 |
| 74 | 钨 | (+2), (+3), (+4), (+5), +6 |
| 75 | 铼 | (-1), (+1), +2, (+3), +4, (+5), +6, +7 |
| 76 | 锇 | (+2), +3, +4, +6, +8 |
| 77 | 铱 | (+1), (+2), +3, +4, +6 |
| 78 | 铂金 | (+1), +2, (+3), +4, +6 |
| 79 | 金 | +1, (+2), +3 |
| 80 | 水星 | +1, +2 |
| 81 | 铊 | +1, (+2), +3 |
| 82 | 领导 | +2, +4 |
| 83 | 铋 | (-3), (+2), +3, (+4), (+5) |
| 84 | 钋 | (-2), +2, +4, (+6) |
| 85 | 虾青素 | ? |
| 86 | 氡 | 0 |
| 87 | 弗朗西姆 | ? |
| 88 | 镭 | +2 |
| 89 | 锕 | +3 |
| 90 | 钍 | +4 |
| 91 | 精锕 | +5 |
| 92 | 铀 | (+2), +3, +4, (+5), +6 |
来源
- 布朗,I.大卫。“无机化学中的化学键:键价模型”,第二版,国际结晶学联合会。牛津:牛津科学出版社,2016年。
- 兰格化学手册,第8版,手册出版商,1952年。
- O'Dwyer,M.F.,J.E.Kent和R.D.Brown。《瓦伦西》,纽约:斯普林格·维拉格,1978年。
- 斯马特,莱斯利E.和伊莱恩A.摩尔。《固体化学导论》,第四版。博卡拉顿:华润出版社,2016年。
- 发表于 2021-10-14 06:35
- 阅读 ( 153 )
- 分类:数学
你可能感兴趣的文章
一价(monovalent)和二价(divalent)的区别
一价元素和二价元素之间的关键区别在于,一价元素可以移除或获得一个电子以达到稳定,而二价元素可以移除或获得两个电子以达到稳定。 一价和二价这两个术语可以描述化学元素的价态。这两个术语描述了一个原子为了...
- 发布于 2020-09-15 10:14
- 阅读 ( 285 )
连锁(catenation)和四价(tetravalency)的区别
链结和四价的关键区别在于,链结包括同一化学元素的原子结合形成链状或环状结构,而四价是指形成四个共价键的能力。 由于化学元素碳的特性,它和化学元素碳同时使用链式和四价。碳可以通过共价键与许多碳原子结合...
- 发布于 2020-09-27 17:55
- 阅读 ( 242 )
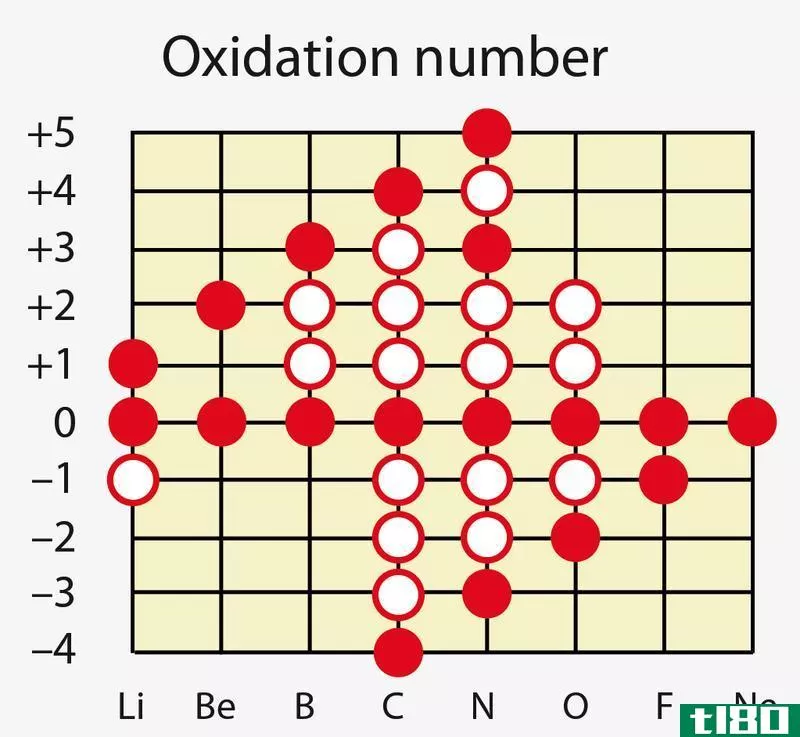
价(valency)和氧化值(oxidation number)的区别
...。 很自然,惰性气体原子有这种电子构型。因此,其他元素需要丢失、获得或共享电子来遵守八位元规则。在这种稳定过程中,一个原子需要失去、获得或分享的最大电子数就是该原子的价态。 例如,让我们考虑一下硅。硅的...
- 发布于 2020-10-15 12:44
- 阅读 ( 316 )
激进的(radical)和价(valency)的区别
...子的化学物种,而价是一个化学概念,它描述了一种化学元素与另一种化学元素结合的能力。 自由基是一种非常活泼的化学物质,因为它有一个不成对的电子。价是一种元素的结合力,特别是用它能置换或结合的氢原子数来衡...
- 发布于 2020-10-17 02:38
- 阅读 ( 418 )
氧化物(oxide)和二氧化物(dioxide)的区别
...于氧化物是任何一种含有一个或多个氧原子与另一种化学元素结合的化合物,而二氧化物是一种分子中含有两个氧原子的氧化物。 氧化物是描述化合物中氧原子存在的一般术语。在这里,氧原子与另一种化学元素(主要是金属...
- 发布于 2020-10-17 09:02
- 阅读 ( 657 )
价(valency)和指控(charge)的区别
价态与电荷的关键区别在于,价态表示一种化学元素与另一种化学元素结合的能力,而电荷则表示一种化学元素获得或移除的电子数。 价和电荷是密切相关的术语,因为这两个术语都描述了化学元素的反应性。价是一种元素...
- 发布于 2020-10-23 02:08
- 阅读 ( 364 )
价(valency)和价电子(valence electrons)的区别
...的关键区别在它们的定义中得到了最好的解释;价电子是元素最外层壳层中的电子,而价电子是为了达到最接近的目的而应该接受或移除的电子数惰性气体配置。正是最外层的电子通常有助于形成化学键。在某些原子中,价电子...
- 发布于 2020-10-24 18:09
- 阅读 ( 1010 )
配价(valency)和价电子(valence electrons)的区别
...在化学中的文学意义是与容量有关的。用化学术语来说,元素的价态是它能形成的键的数目。价电子就是可以参与成键的电子。因此,价电子和价电子之间的主要区别在于,价电子是一个原子或元素能形成的键的数目,而价电子...
- 发布于 2021-06-27 10:49
- 阅读 ( 634 )
配价(valency)和共价性(covalency)的区别
...道上的电子称为价电子。有时,价电子的数目被认为是该元素的价。例如,氢的价态(H)是1,因为氢原子可以通过失去或获得1个电子而稳定。氯原子在最外层轨道上有7个电子(价电子数为7),但再获得1个电子,就可以得到更...
- 发布于 2021-06-29 08:25
- 阅读 ( 377 )
原子价(valence)和配价(valency)的区别
主差价(main difference valence) vs. 配价(valency) 原子的价态和价态是根据原子中存在的电子来描述的。众所周知,电子位于原子核周围的壳层或轨道中。因此,根据这些电子和原子核之间的吸引力的强度,电子可以从原子中丢...
- 发布于 2021-06-29 08:34
- 阅读 ( 405 )