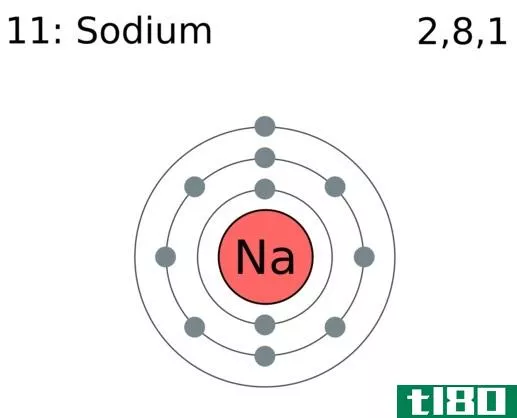
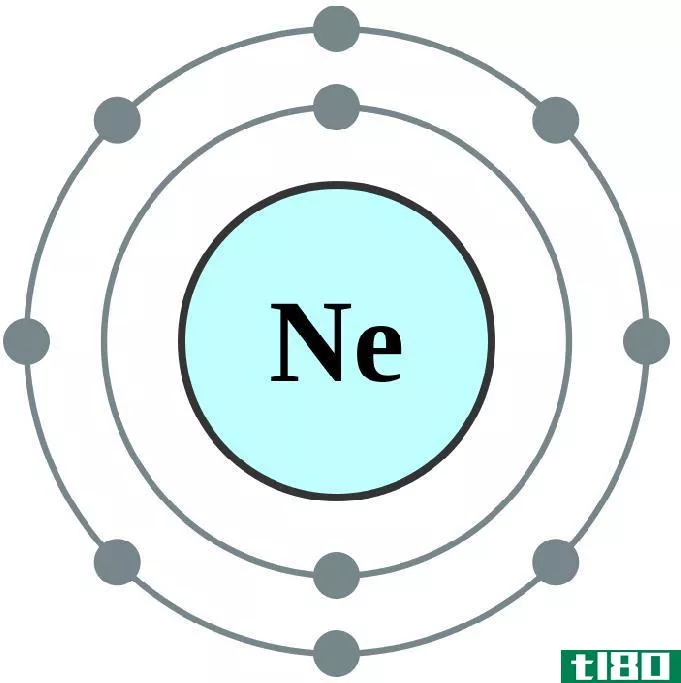
价态与电荷的关键区别在于,价态表示一种化学元素与另一种化学元素结合的能力,而电荷则表示一种化学元素获得或移除的电子数。
价和电荷是密切相关的术语,因为这两个术语都描述了化学元素的反应性。价是一种元素的结合力,特别是用它能置换或结合的氢原子数来衡量的。另一方面,原子的电荷是质子数减去原子中的电子数。
目录
1. 概述和主要区别
2. 什么是价
3. 什么是电荷
4. 并列比较-以表格形式表示的价与电荷
5. 摘要
什么是价(valency)?
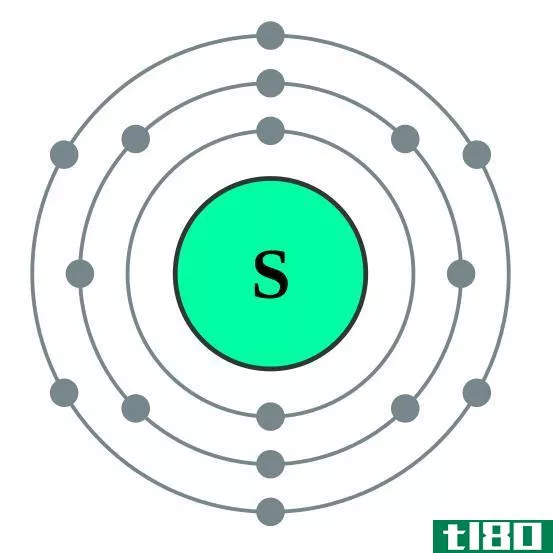
价是一种元素的结合力,特别是用它能置换或结合的氢原子数来衡量的。它是化学元素反应性的量度。然而,它只描述原子的连接性,而不描述化合物的几何结构。
我们可以通过观察元素在周期表中的位置来确定价态。周期表根据原子最外层的电子数排列了化学元素。最外层的电子数也决定了原子的价态。例如,周期表中的第1组元素有一个最外层的电子。因此,它们有一个电子来代替或与氢原子结合。因此,价是1。
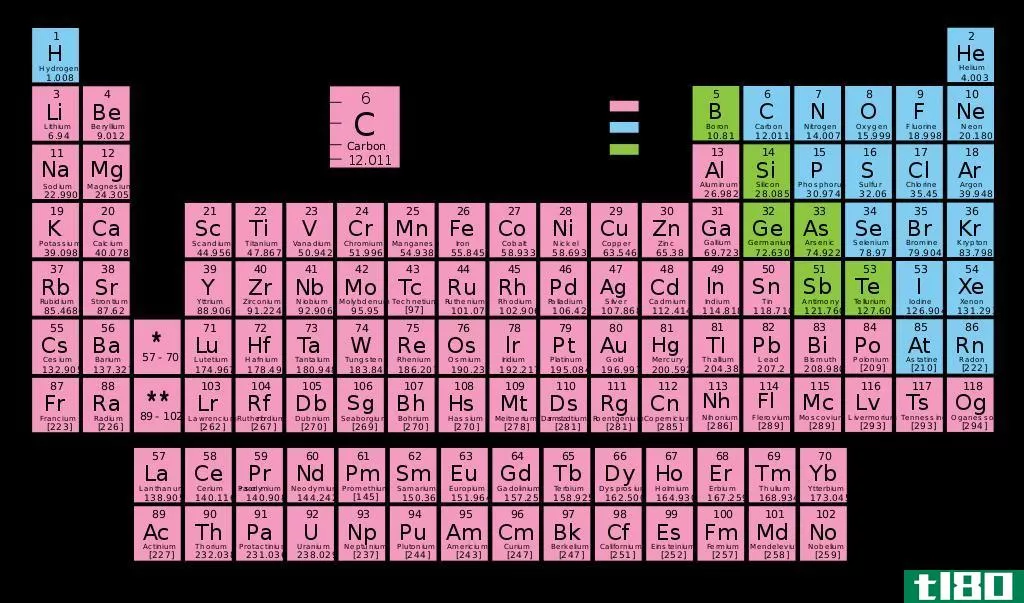
图01:元素周期表
同样,我们可以用化合物的化学式来确定其价态。这种方法的基础是八位规则。根据八位元规则,原子趋向于用电子填满壳层或移除多余的电子来完成最外层的壳层。例如,如果我们考虑化合物NaCl,Na的价是1,因为它可以除去最外层壳层中的一个电子。同样,Cl的价也是1,因为它倾向于获得一个电子来完成它的八位态。
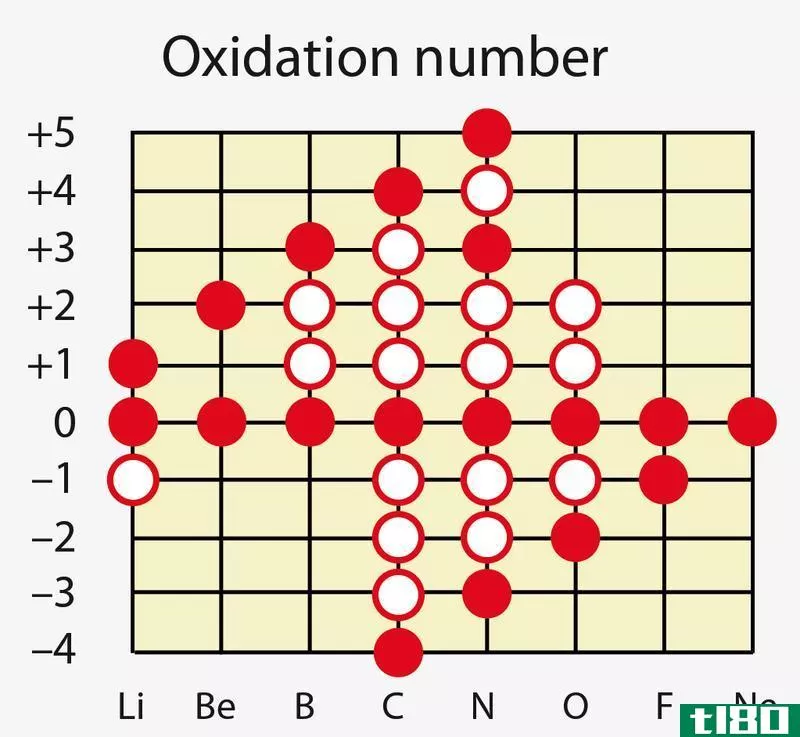
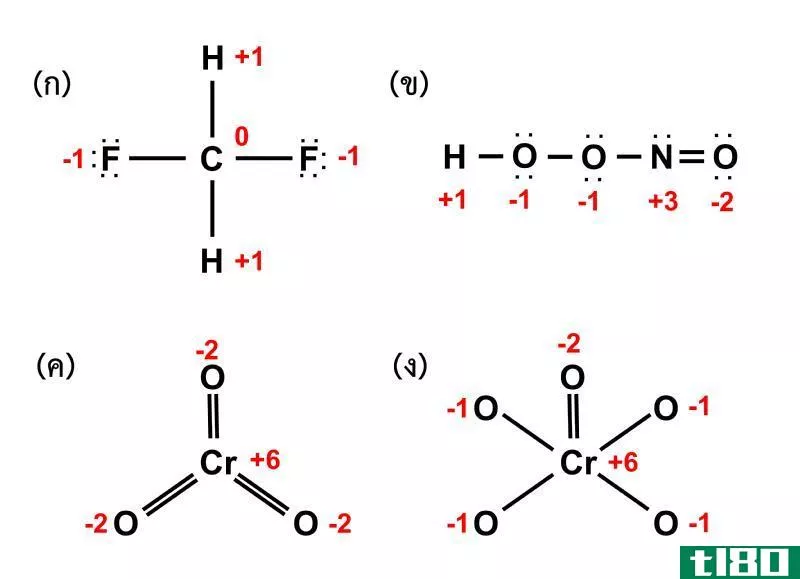
但是,我们不应该与氧化数和价相混淆,因为氧化数描述了原子可以携带的电荷。例如,氮的价态是3,但氧化数可以在-3到+5之间变化。
什么是指控(charge)?
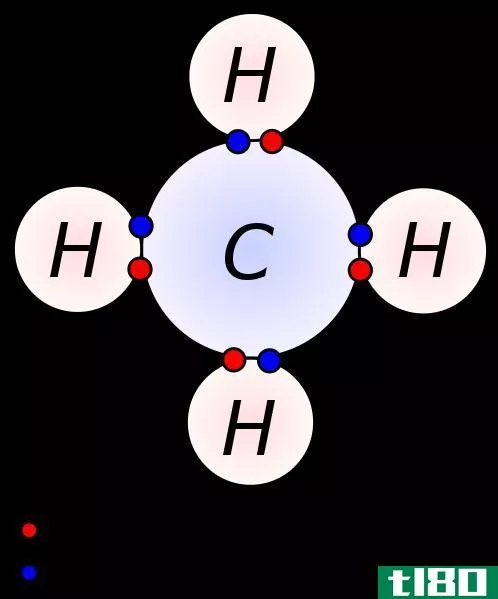
电荷是原子中质子数减去电子数。通常,这两个数相等,原子以中性形式出现。
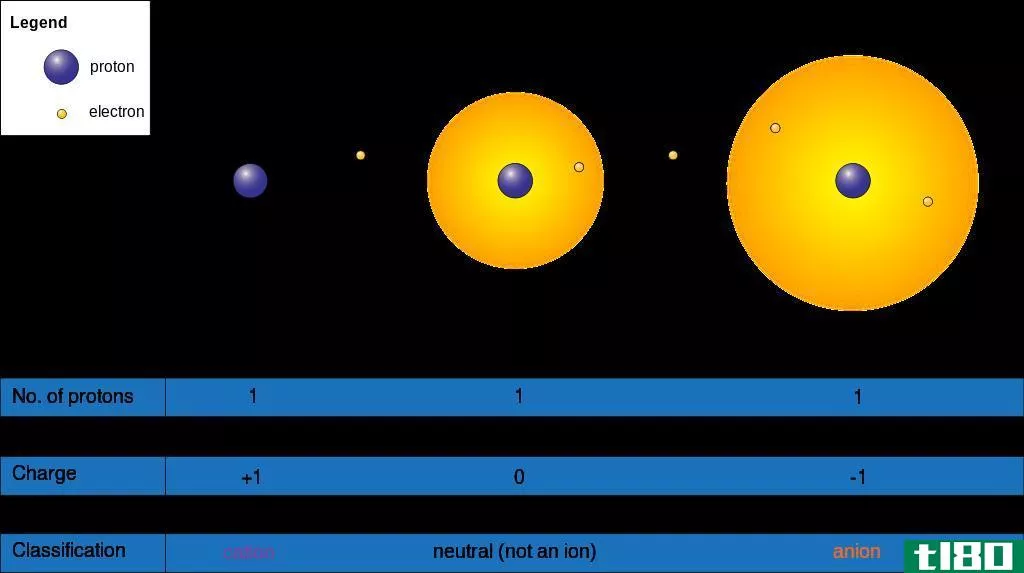
图02:氢原子的电荷
然而,如果一个原子有一个不稳定的电子构型,那么它就倾向于通过获得或移除电子来形成离子。在这里,如果一个原子获得了电子,那么它就得到了一个负电荷,因为一个电子有一个负电荷。当一个原子获得一个电子时,原子中没有足够的质子来平衡这个电荷;因此,原子的电荷是-1。但是,如果原子除去一个电子,那么就有一个额外的质子;因此,原子得到+1电荷。
价(valency)和指控(charge)的区别
价表示原子的反应性,而电荷则表示原子如何反应。因此,价态和电荷的关键区别在于,价态表示一种化学元素与另一种化学元素结合的能力,而电荷则表示一种化学元素获得或移除的电子数。
此外,价的值没有正负号,而如果离子是通过除去电子而形成的,则电荷有加号;如果原子获得了电子,则电荷有负号。
下面的信息图总结了价态和电荷之间的区别。

总结 - 价(valency) vs. 指控(charge)
价表示原子的反应性,而电荷则描述原子如何反应。总之,价态和电荷的关键区别在于,价态表示一种化学元素与另一种化学元素结合的能力,而电荷则表示一种化学元素获得或移除的电子数。
引用
1赫尔曼斯汀,安妮·玛丽。“什么是价或价?“ThoughtCo,2019年3月21日,可在此处获取。