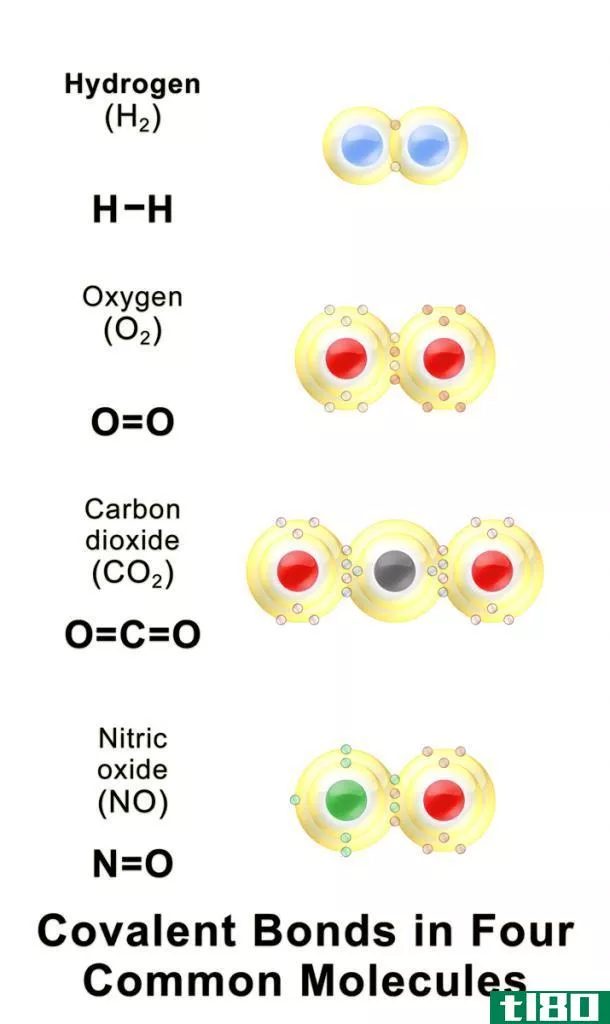
形式电荷和氧化态的关键区别在于,形式电荷是分子中一个原子的电荷,我们假设化学键中的电子在原子之间平均分配,而氧化态是一个原子失去或获得或与另一个原子共享的电子数。
形式电荷和氧化态是不同的,尽管我们通常假设它们是相同的。形式电荷决定了分子中原子周围出现的电子数,氧化态决定了分子形成过程中原子间交换的电子数。
目录
1. 概述和主要区别
2. 什么是正式收费
3. 什么是氧化状态
4. 并列比较-表格形式的形式电荷与氧化状态
5. 摘要
什么是正式指控(formal charge)?
形式电荷是分子中原子的电荷,我们假设化学键中的电子在原子之间平均分配。因此,当我们比较原子周围的电子数时,我们比较原子周围的电子数。在确定形式电荷时,我们必须把分子的电子分配给单个原子。在这里,我们还需要考虑以下要求:;
- 我们必须把非键电子分配给产生非键电子的原子
- 我们必须在共享原子之间平均分配成键电子
数学关系如下:
形式电荷=(中性原子价电子数)-(孤对电子数)—({1/2}*键对电子数)

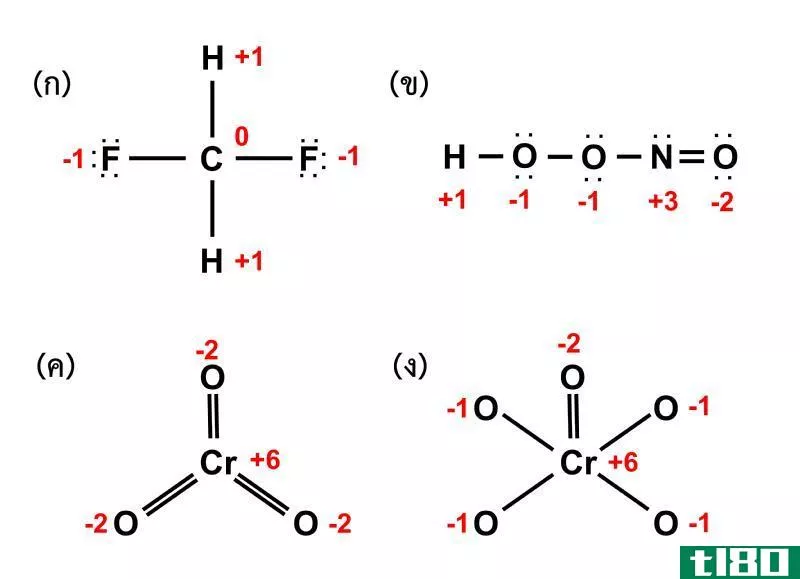
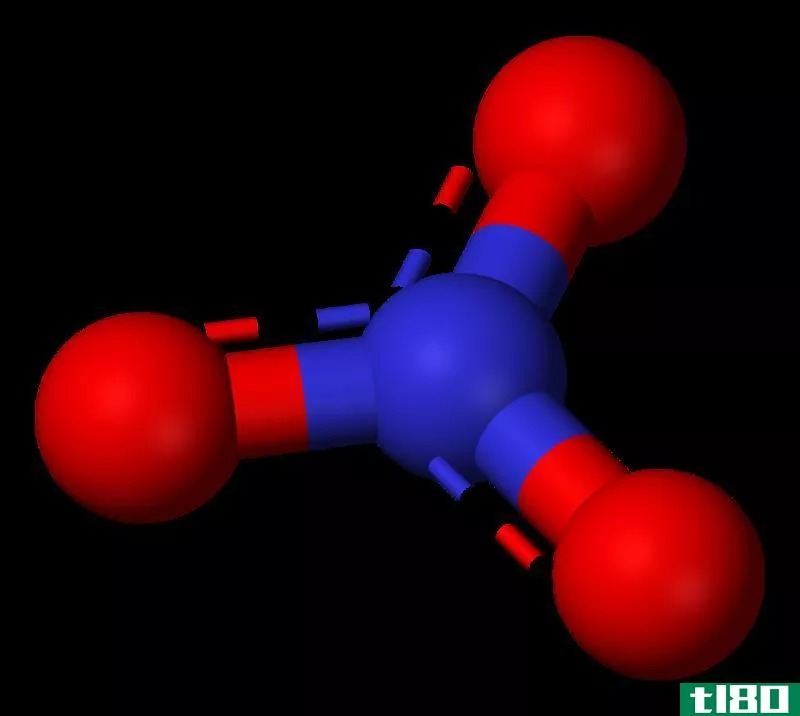
图1:臭氧和硝酸根阴离子的形式电荷
让我们考虑一个例子来理解这种现象。对于氨分子,氮原子上有三个N-H键和一个孤电子对。那么什么时候可以计算出以下各项:;
N=5-2{1/2}*6=0的形式电荷
H=1–0–{1/2}*2=0的形式电荷
什么是氧化态(oxidation state)?
氧化态是一个特定原子可以失去、获得或与另一个原子共享的电子数。这个术语适用于分子中的任何化学元素(氧化数这个术语主要用于配位络合物的中心金属原子,尽管我们可以互换使用这些术语)。氧化态实际上给出了化合物中原子的氧化程度。在印度教中,我们应该给出一个完整的原子数。例如,铁在FeO中的氧化态为+2。
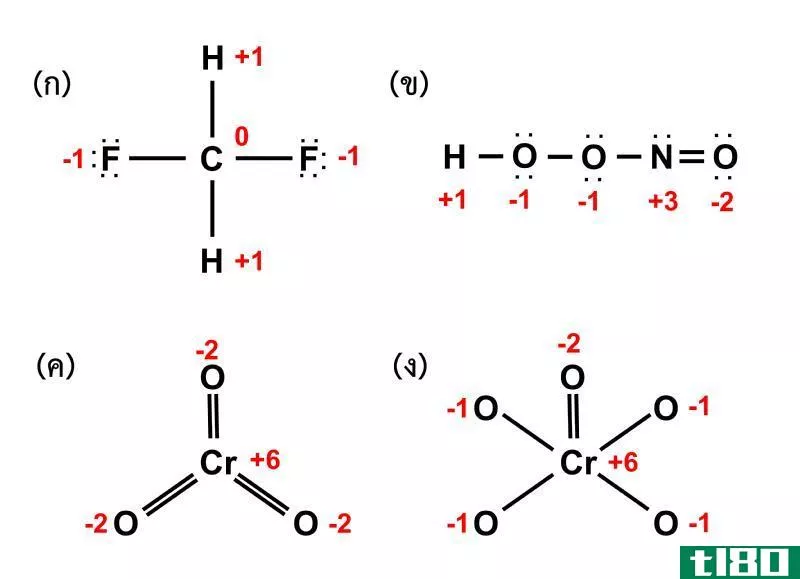
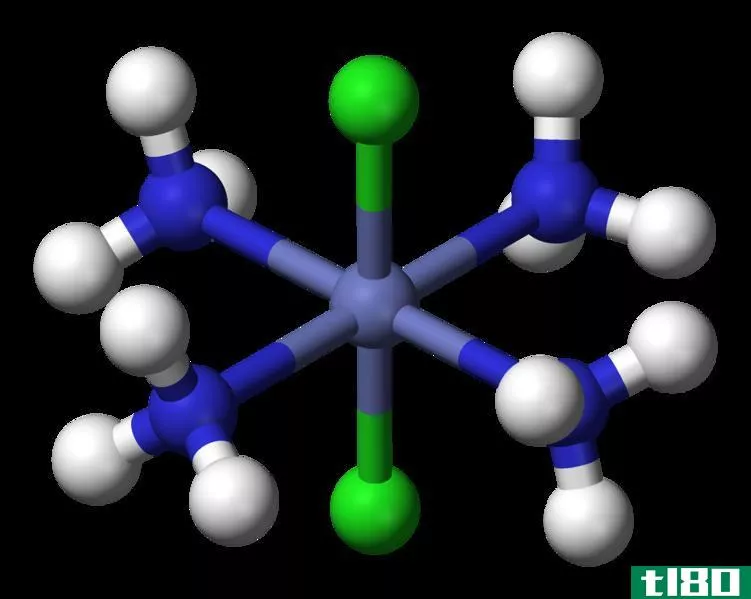
图02:不同分子中原子的氧化态
测定氧化状态的提示:
- 单个元素的氧化状态为零(这也包括由单个元素组成的分子)。
- 分子或离子的总电荷是每个原子的电荷之和。
- 碱金属的氧化态总是+1,碱土金属的氧化态为+2。
- 同时,氟的氧化态始终为-1。
- 此外,氢的氧化态通常为+1。但有时它是-1(当与碱金属或碱土金属结合时)
- 而且,一般来说,氧的氧化状态是-2(但在过氧化物和超级氧化物中可能会有所不同)。
- 分子中最负电荷的原子带负电荷,另一个原子带正电荷。
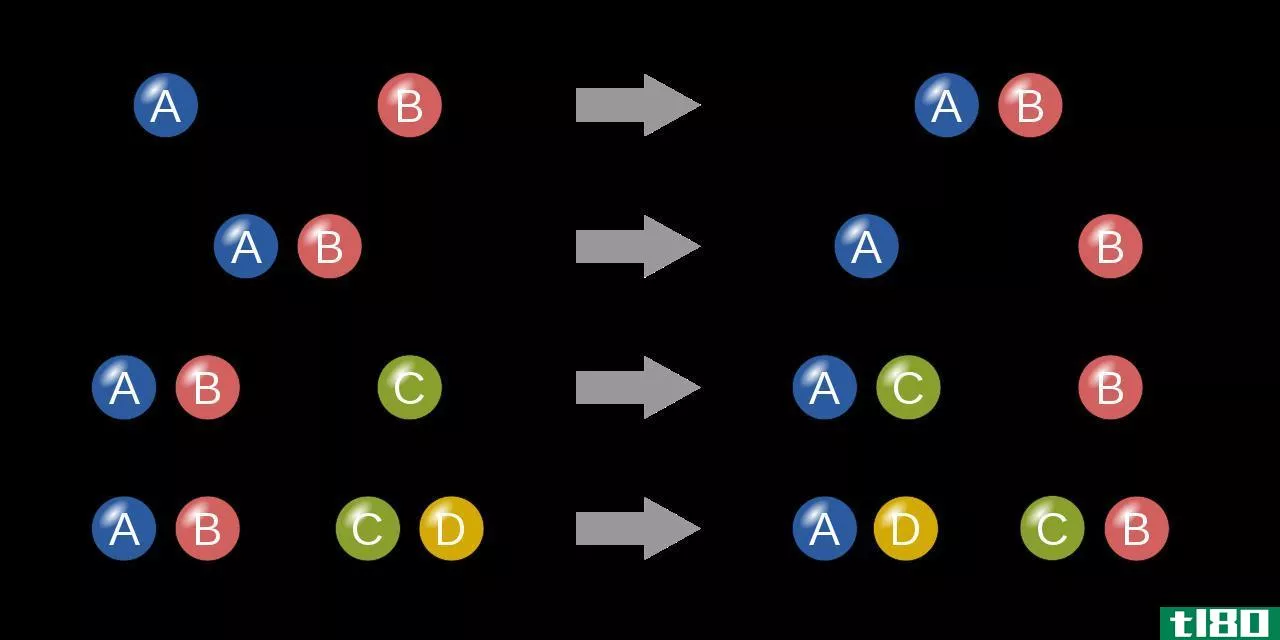
氧化态对氧化还原反应产物的测定非常有用。氧化还原反应是包括原子间电子交换的化学反应。在氧化还原反应中,两个半反应同时发生。一种是氧化反应,另一种是还原反应。氧化反应涉及到原子氧化状态的增加,而还原反应涉及到原子氧化状态的降低。
正式指控(formal charge)和氧化态(oxidation state)的区别
形式电荷和氧化态之间的关键区别在于,形式电荷是分子中一个原子的电荷,我们假设化学键中的电子在原子之间平均分配,而氧化态是一个原子失去、获得或与另一个原子共享的电子数。例如,氨分子中氮原子的形式电荷为0,而氧化态为+3。
下面的信息图总结了形式电荷和氧化状态之间的区别。

总结 - 正式指控(formal charge) vs. 氧化(oxidation)
形式电荷和氧化态是不同的术语,尽管有些人认为它们是相同的。形式电荷和氧化态之间的关键区别在于,形式电荷是分子中一个原子的电荷,我们假设化学键中的电子在原子之间平均分配,而氧化态是一个原子失去、获得或与另一个原子共享的电子数。
引用
1“2.3:正式指控。”化学剧本,歌词,2019年7月25日,可在这里查阅。