金属氧化物和非金属氧化物的主要区别在于金属氧化物是碱性化合物,而非金属氧化物是酸性化合物。
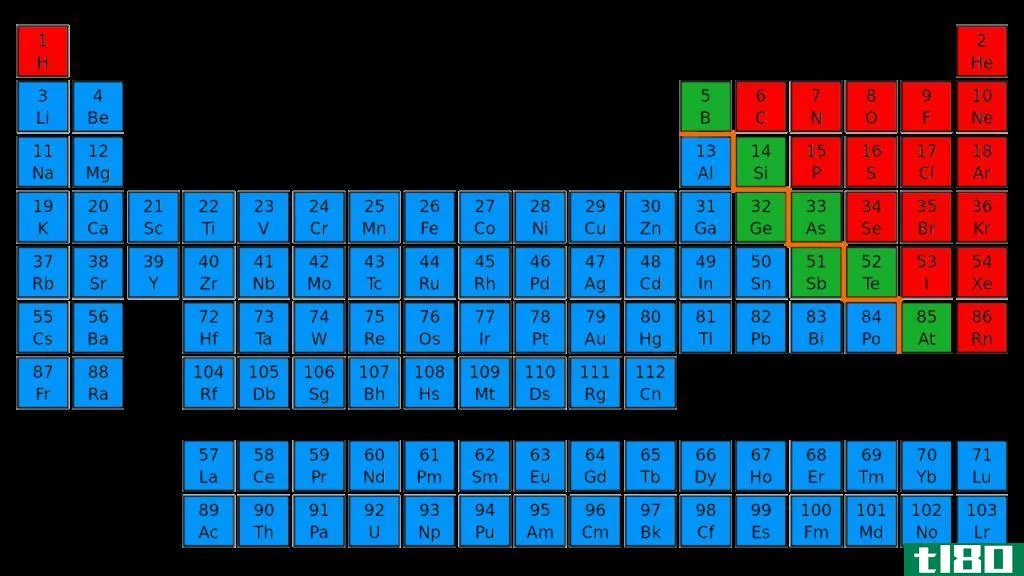
“氧化物”是一大类化合物,其化学元素基本上与氧原子结合。然而,惰性气体由于其惰性和较高的稳定性而不形成这些化合物。大多数金属和非金属形成具有不同氧化状态的氧化物,而其他一些化学元素形成具有固定氧化状态的氧化物;例如,镁仅形成化学式为MgO的氧化镁,而钒形成各种氧化物,如V2O3和V2O5。
目录
1. 概述和主要区别
2. 什么是金属氧化物
3. 什么是非金属氧化物
4. 并列比较-表格形式的金属氧化物与非金属氧化物
5. 摘要
什么是金属氧化物(metal oxides)?
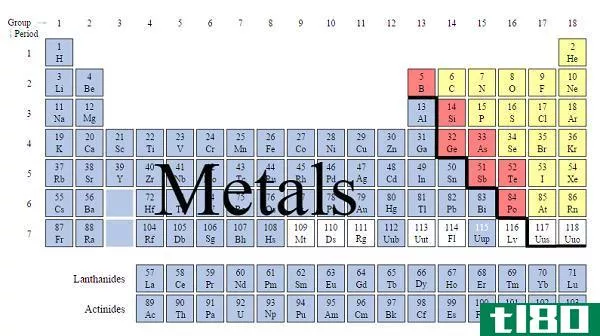
金属氧化物是无机化合物,含有基本上与氧原子结合的金属。在这些化合物中,氧本质上是具有-2氧化状态的化合物的阴离子。因此,金属的阳离子是化合物。形成氧化物的金属包括碱金属族(1族元素)、碱土金属(2族元素)和包括过渡金属在内的d块元素。它们形成离子氧化物,也就是说,它们形成的氧化物化合物具有离子性质。但有些化学元素形成具有共价性质的氧化物,特别是表现出较高氧化状态的化学元素。

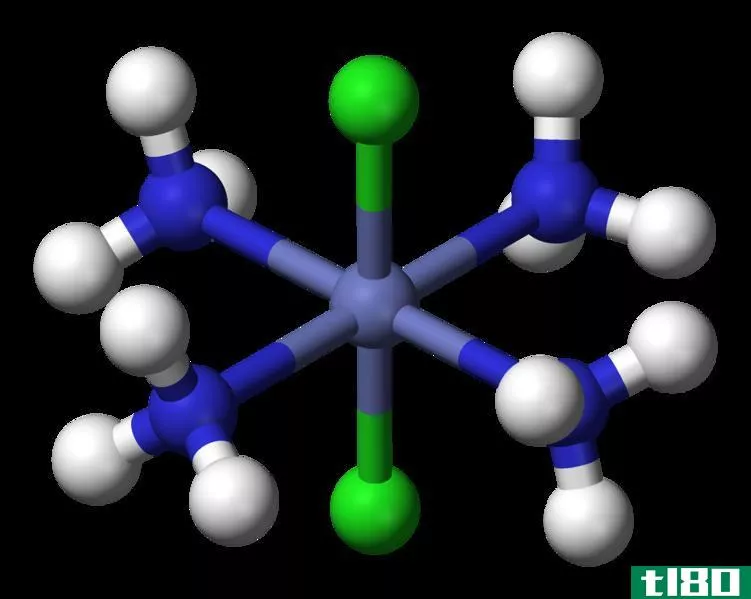
图01:氧化银(II)
大多数时候,金属氧化物是晶体固体,通常是碱性化合物。因此,它们能与水反应生成碱性溶液。此外,它们还可以与酸反应,通过中和反应生成盐。虽然几乎所有的氧化物都有-2氧化态的氧,但也有-1和-1/2氧化态的氧化物,我们分别称之为过氧化物和超氧化物。化合物中氧原子的数量取决于金属的氧化状态。
金属氧化物示例:
- 氧化钠(Na2O)
- 氧化镁(MgO)
- 五氧化二钒(V2O5)
- 氧化银(AgO)
什么是非金属氧化物(nonmetal oxides)?
非金属氧化物是含有基本上与氧原子结合的非金属的无机化合物。因此,这些化合物主要含有p嵌段元素,因为p嵌段元素是我们所拥有的非金属元素。几乎所有的非金属氧化物都是共价化合物,因为它们倾向于与其他原子共用电子,这里是氧原子。
这些都是酸性化合物,因此当它们溶解在水中时会形成酸。由于同样的原因,它们可以通过中和反应与碱反应生成盐。此外,在水介质中可以形成氧化丹。

图02:夸脱或二氧化硅是一种非金属氧化物
非金属氧化物示例:
- 二氧化硫(SO2)和三氧化硫(SO3)
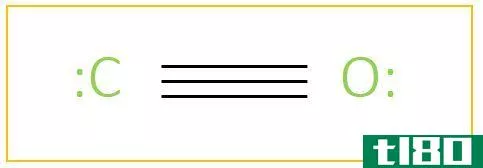
- 二氧化碳(CO2)和一氧化碳(CO)
- 二氧化硅(SiO2)
- 氮氧化物(N2O、NO2、N2O5)
金属(metal)和非金属氧化物(nonmetal oxides)的区别
金属氧化物是含有基本上与氧原子结合的金属的无机化合物,而非金属氧化物是含有基本上与氧原子结合的非金属的无机化合物。这就是金属氧化物和非金属氧化物的根本区别。此外,这些化合物因其化学性质而不同。因此,金属氧化物和非金属氧化物的关键区别在于金属氧化物是碱性化合物,而非金属氧化物是酸性化合物。
此外,金属氧化物和非金属氧化物在化学结构上也存在一些差异。大多数情况下,金属氧化物是离子化合物,而非金属氧化物是共价化合物。此外,金属氧化物倾向于与水反应形成碱性溶液,而非金属氧化物倾向于与水反应形成酸性溶液。这是金属氧化物和非金属氧化物之间的另一个显著区别。此外,金属氧化物与酸反应生成盐,而非金属氧化物与碱反应生成盐。
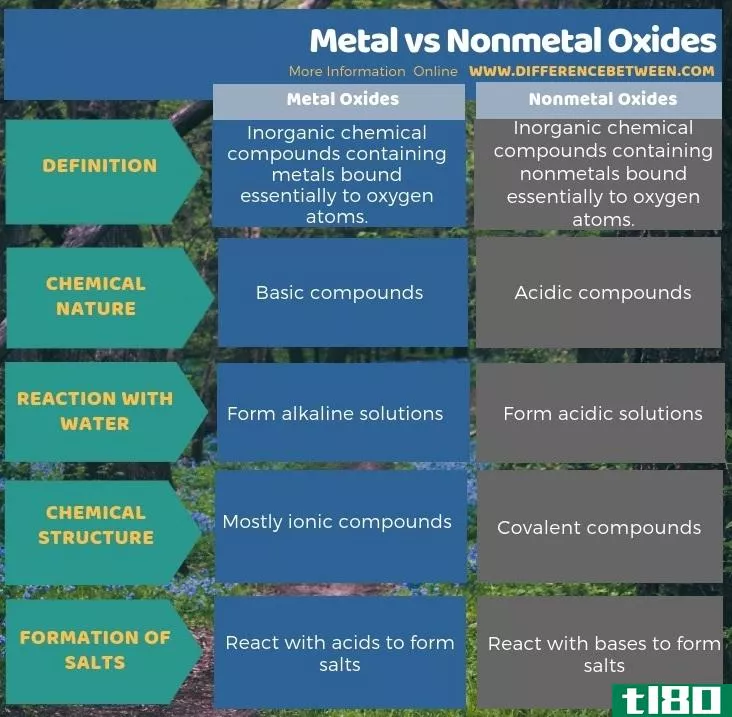
总结 - 金属(metal) vs. 非金属氧化物(nonmetal oxides)
氧化物是一种由金属或非金属与一个或多个氧原子结合的化合物。金属氧化物和非金属氧化物的主要区别在于金属氧化物是碱性化合物,而非金属氧化物是酸性化合物。
引用
1Zumdahl,Steven S.“氧化物”,《大英百科全书》,2018年5月7日。此处提供