价电子和核心电子之间的关键区别在于,价电子参与化学键的形成,而核心电子不参与化学键的形成。
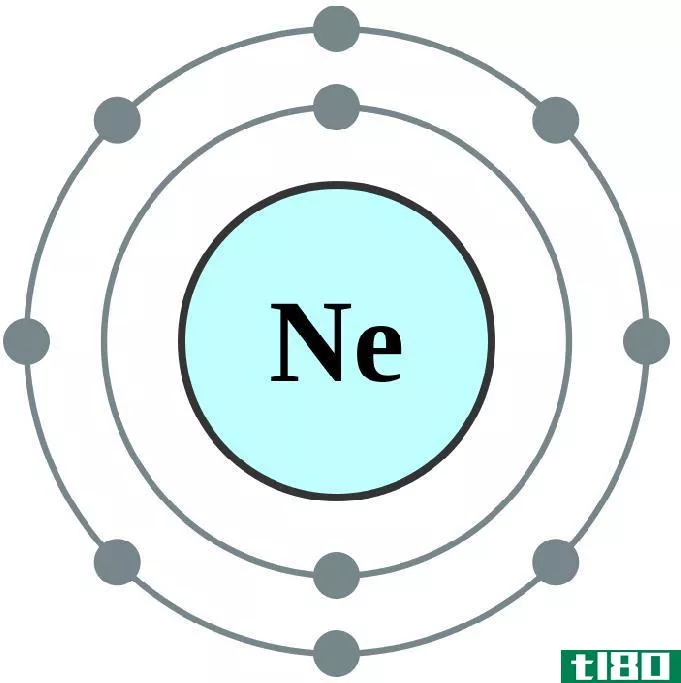
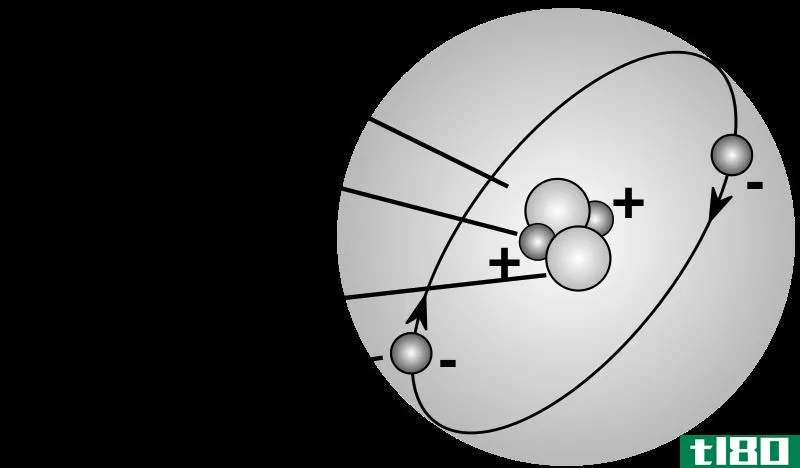
原子是所有现存物质的组成部分。它们太小了,我们甚至不能用肉眼观察它们。一般来说,原子在埃范围内。原子是由原子核组成的,原子核有质子和中子。有电子绕着原子核绕轨道旋转。原子中的大部分空间是空的。带正电的原子核(质子带正电荷)和带负电的电子之间的吸引力维持着原子的形状。电子以成对原子的形式存在于轨道上,它们有相反的自旋。此外,有两种类型的电子,即价电子和核心电子。
目录
1. 概述和主要区别
2. 什么是价电子
3. 什么是核心电子
4. 并列比较-价电子与核心电子的表格形式
5. 摘要
什么是价电子(valence electr***)?
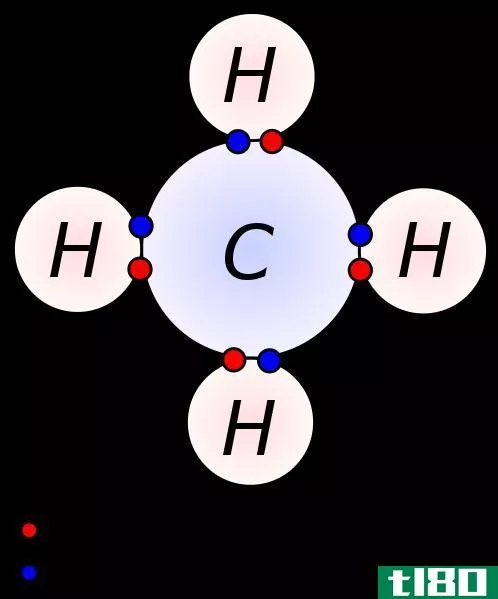
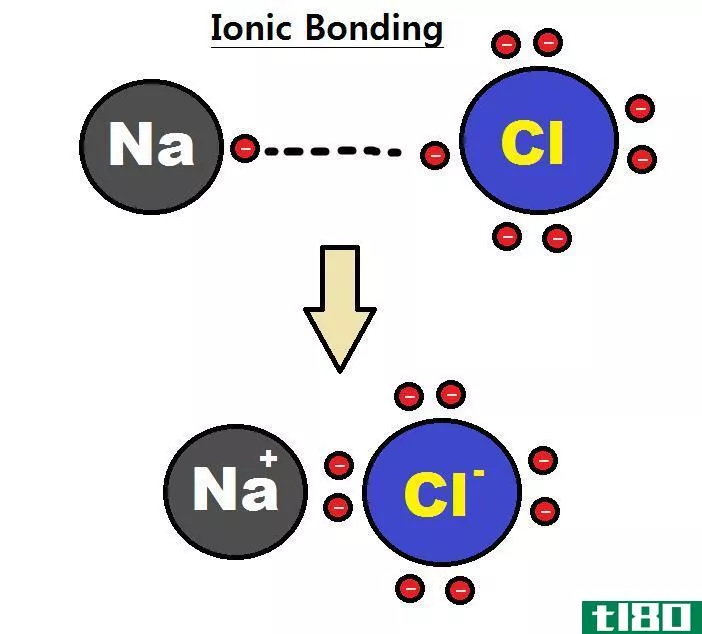
价电子是原子中参与化学键形成的电子。当化学键形成时,原子既可以获得电子,也可以贡献电子,也可以共享电子。捐赠、获得或分享这些电子的能力取决于它们拥有的价电子的数量。例如,当一个氢分子形成时,一个氢原子给共价键一个电子。因此,两个原子共用两个电子。因此,氢原子有一个价电子。在氯化钠的形成过程中,一个钠原子放出一个电子,而氯原子得到一个电子。它发生的目的是在它们的价轨道上填充一个八位元。在那里,钠只有一个价电子,氯有七个价电子。因此,通过观察价电子,我们可以确定原子的化学反应性。
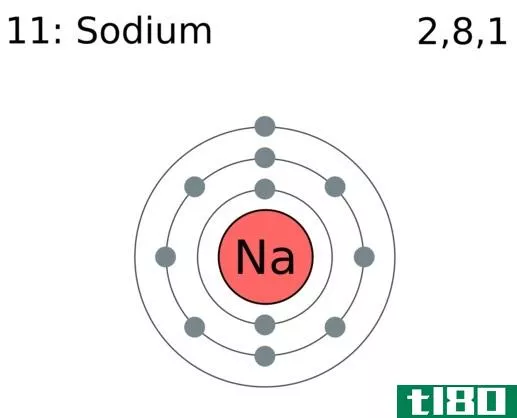
图01:钠原子有一个价电子
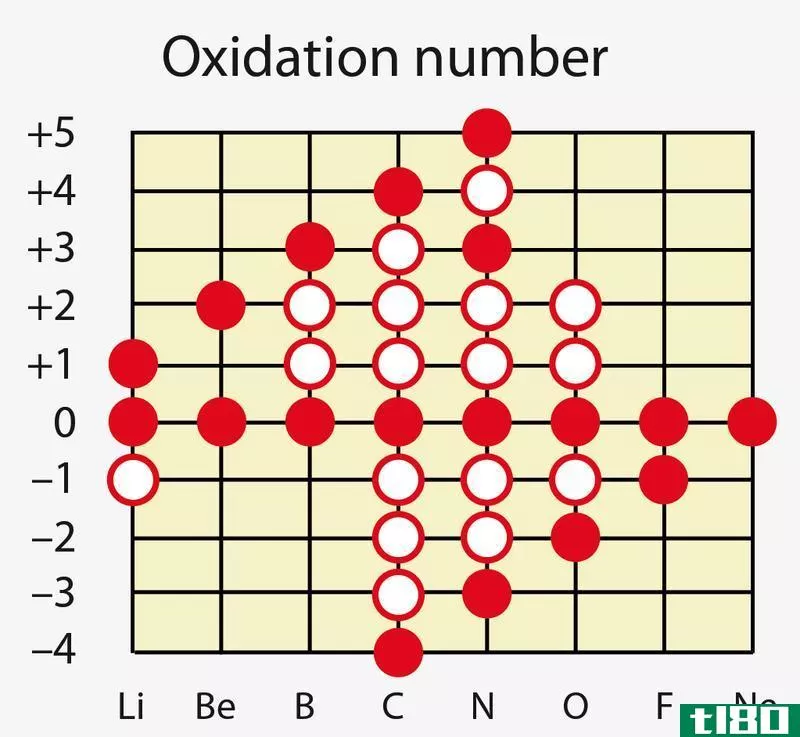
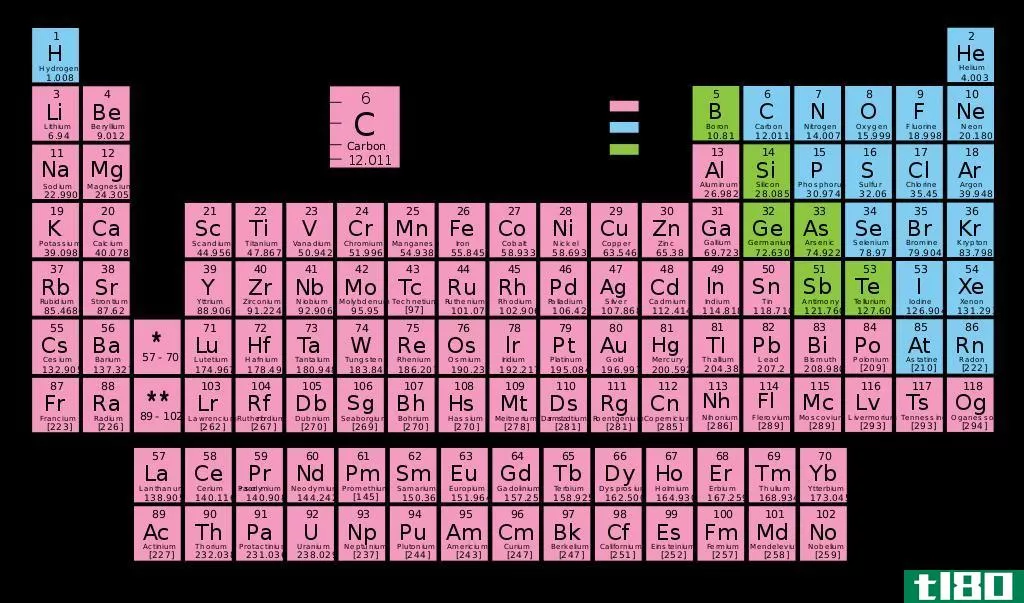
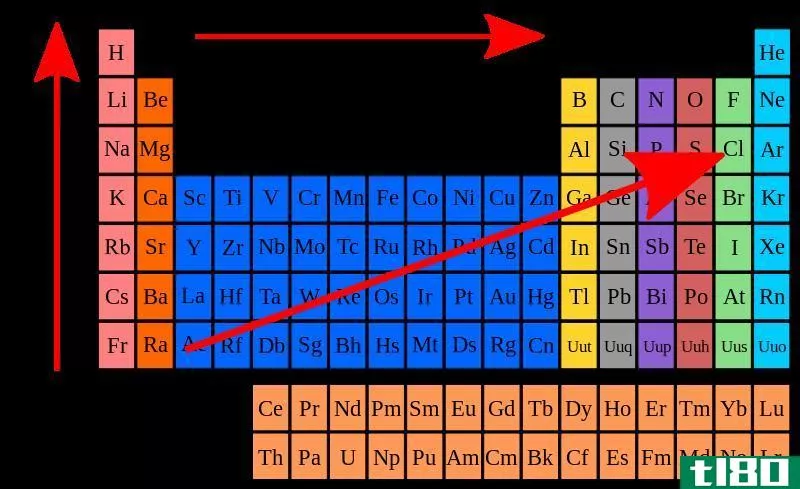
主族元素(I、II、III族等)最外层有价电子。价电子的数目等于它们的群数。惰性原子已经完成了价电子数目最多的壳层。对于过渡金属,一些内部电子也充当价电子。价电子的数目可以通过观察原子的电子构型来确定。例如,氮的电子构型是1s2 2s2 2p3。第二层壳层中的电子(在这种情况下是最高主量子数)被视为价电子。因此,氮有五个价电子。除了参与键合之外,价电子也是元素导热和导电的原因。
什么是核心电子(core electr***)?
核心电子是原子的价电子以外的电子。由于这些电子位于原子内部,所以核心电子不参与键的形成。它们存在于原子的内壳层中。例如,在氮原子(1s2 2s2 2p3)中,七个电子中有五个是价电子,而两个1s电子是核心电子。
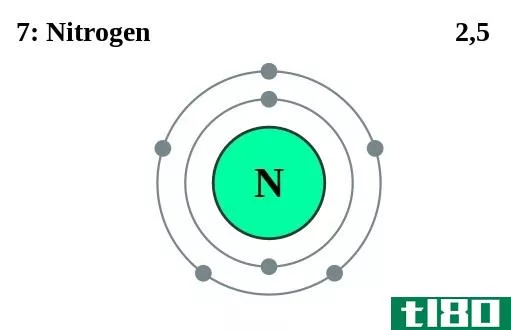
图02:氮有两个核心电子
此外,从原子中移除核心电子所需的能量远高于价电子所需的能量。
原子价(valence)和核心电子(core electr***)的区别
价电子和核心电子都围绕原子核运动。价电子位于最外层的电子壳层,而核心电子则位于内层壳层。例如,根据电子构型,氮原子有5个价电子和2个核心电子;1s2 2s2 2p3。首先,价电子与核心电子的关键区别在于价电子参与化学键的形成,而核心电子不参与化学键的形成。
此外,价电子和核心电子之间的另一个显著区别是,与去除价电子所需的能量相比,去除核心电子所需的能量非常高。
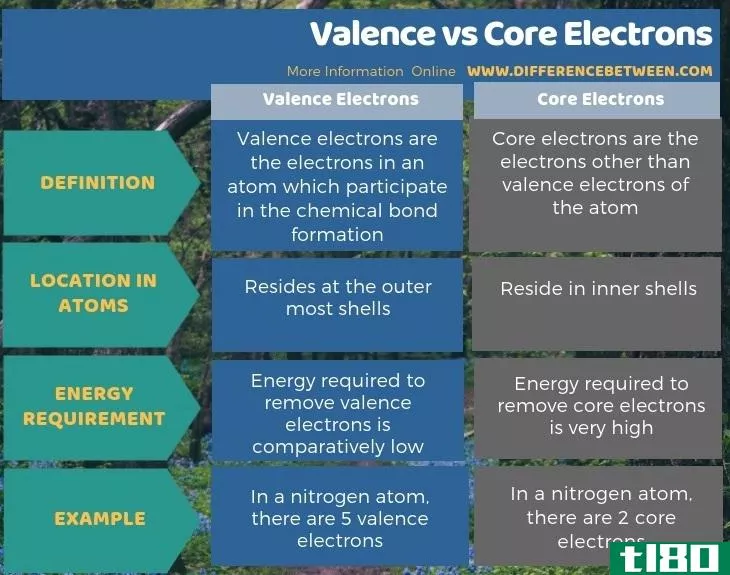
总结 - 原子价(valence) vs. 核心电子(core electr***)
原子中有两种类型的电子,即价电子和核心电子。价电子位于最外层,而核心电子在内层。价电子与核心电子的关键区别在于价电子参与化学键的形成,而核心电子不参与化学键的形成。
引用
1“1.3:价电子和开放价。”化学图书馆,图书馆,2019年4月23日,可在这里查阅。“1.9B:价电子和核心电子。”化学图书馆,图书馆,2019年5月2日,可在这里查阅。
2“1.9B:价电子和核心电子”,《化学歌词》,歌词,2019年5月2日,