惰性对效应与屏蔽效应的关键区别在于,惰性对效应是过渡后金属化合物中最外层电子壳层中的一对电子保持不变的能力,而屏蔽效应则是原子中电子与原子核之间吸引力的降低。
惰性对效应和屏蔽效应是化学中讨论的两种不同的现象。这两个术语都描述了电子和原子核之间的吸引力。
目录
1. 概述和主要区别
2. 什么是惰性对效应
3. 什么是屏蔽效应
4. 并列比较-惰性对效应与屏蔽效应的表格形式
5. 摘要
什么是惰性电子对效应(inert pair effect)?
惰性对效应是原子中最外层的电子在形成化合物时保持不变的趋势。它主要发生在s原子轨道上最外层的电子,我们可以在过渡后金属中观察到。这些电子在形成化合物时保持不共享或联合,因为这些最外层的s电子与原子核结合得更紧密。此外,该术语主要用于较重的元素,如第13、14、15和16组中的元素。另外,这一关于惰性对效应的理论是由科学家内维尔·西奇威克在1927年首次提出的。

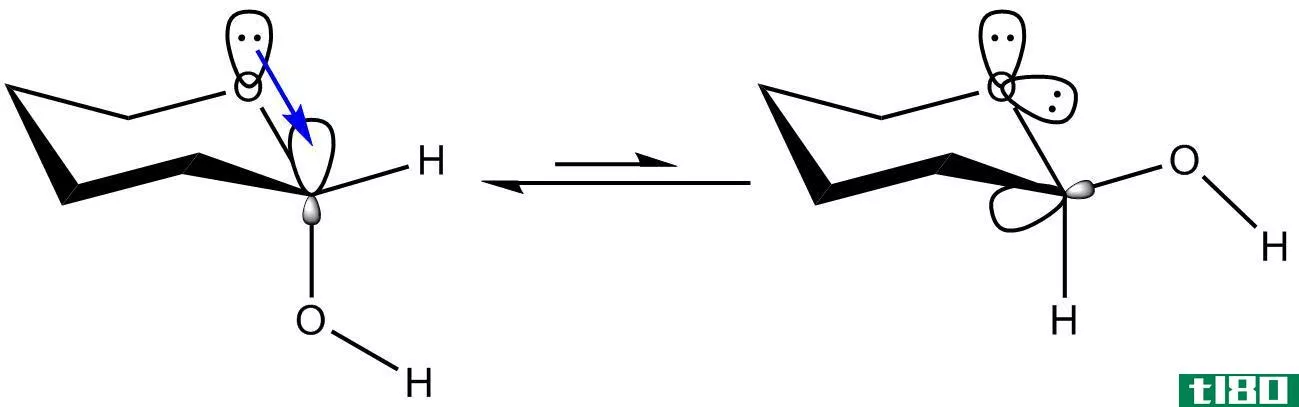
图01:原子半径影响惰性对效应
例如,让我们考虑组13中的化学元素铊。该化学元素的+1氧化态是稳定的,+3氧化态是不稳定的和稀有的。当考虑同一基团中其他化学元素的+1氧化态的稳定性时,由于这种惰性对效应,铊的稳定性最高。
什么是屏蔽效应(shielding effect)?
屏蔽效应是指原子中电子与原子核之间的吸引力减小,从而降低有效核电荷。这个术语的同义词是原子屏蔽和电子屏蔽。它描述了含有一个以上电子的原子中电子和原子核之间的吸引力。因此,它是电子场屏蔽的一个特例。
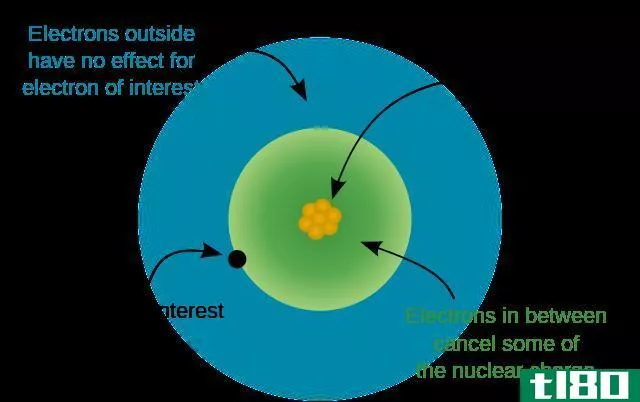
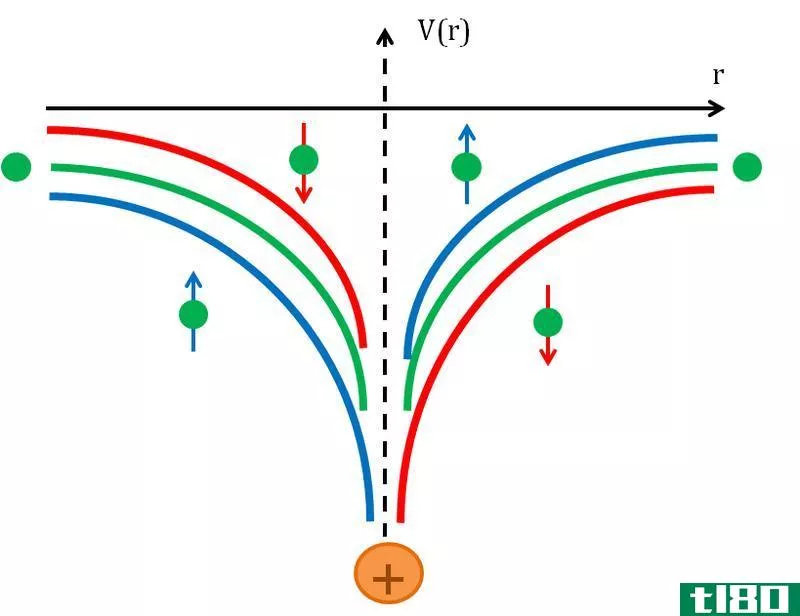
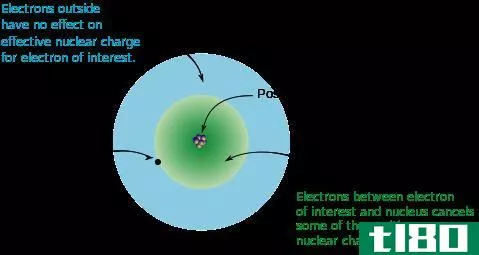
图02:有效核电荷
根据这种屏蔽效应理论,电子壳层在空间中越宽,电子与原子核之间的吸引力就越弱。
惰性电子对效应(inert pair effect)和屏蔽效应(shielding effect)的区别
惰性对效应和屏蔽效应是化学中讨论的两种不同现象。惰性对效应与屏蔽效应的关键区别在于,惰性对效应是最外层电子壳中的一对电子在过渡后金属化合物中保持不变的能力,而屏蔽效应指的是原子中电子与原子核之间的吸引力的减小。
此外,惰性对效应和屏蔽效应的另一个区别是,惰性对效应发生在较重的化学元素中,如第13、14、15和16族元素中,而屏蔽效应发生在电子较多的化学元素中。

总结 - 惰性电子对效应(inert pair effect) vs. 屏蔽效应(shielding effect)
惰性对效应和屏蔽效应是化学中讨论的两种不同的现象。惰性对效应与屏蔽效应的关键区别在于,惰性对效应是指过渡后金属化合物中最外层电子壳层中的一对电子保持不变的能力,而屏蔽效应是指原子中电子与原子核之间引力的降低。
引用
1“惰性对效应”,维基百科,维基媒体基金会,2020年1月24日,可在这里查阅。莫特,瓦莱丽。“化学导论——屏蔽效应和有效核电荷。”Lumen,可在这里找到。
2莫特,瓦莱丽。《化学导论——屏蔽效应和有效核电荷》,Lumen,