屏蔽(shielding)和屏蔽效应(screening effect)的区别
屏蔽效应是由于原子核中电子的吸引力不同,电子云上的有效核电荷减少。换言之,这是由于内壳层电子的存在,原子核和最外层电子之间的吸引力降低。屏蔽效应和屏蔽效应的含义是一样的。屏蔽效果和屏蔽效果没有区别。
目录
1. 概述和主要区别
2. 什么是屏蔽效应
3. 什么是筛选效果
4. 屏蔽与屏蔽效应
5. 摘要
什么是屏蔽效应(shielding effect)?
屏蔽效应是由于电子和原子核之间引力的不同,电子云上有效核电荷的减少。这个术语描述了电子和原子核之间的引力,原子核有一个以上的电子。它也被称为原子屏蔽。
屏蔽效应降低了原子核和含有许多电子的原子中最外层电子之间的吸引力。有效核电荷是原子最外层电子壳层中的电子(价电子)所经历的净正电荷。当有许多内壳层电子存在时,原子核对原子核的吸引力较小。那是因为原子核被电子屏蔽了。内部电子的数量越多,屏蔽效应就越大。增加屏蔽效果的顺序如下。
S轨道>p轨道>d轨道>f轨道
屏蔽效应有周期性的趋势。氢原子是存在一个电子的最小原子。由于没有屏蔽电子,因此该电子上的有效核电荷不会减少。因此,没有屏蔽作用。但是当在周期表中穿过一个周期(从左到右),原子中存在的电子数量会增加。这样屏蔽效果也就增强了。
原子的电离能主要由屏蔽效应决定。电离能是从原子或离子中除去最外层电子所需的能量。如果屏蔽效应很高,那么原子最外层的电子就不会被原子核吸引,换句话说,最外层的电子很容易被移除。因此,屏蔽效应越大,电离能越小。
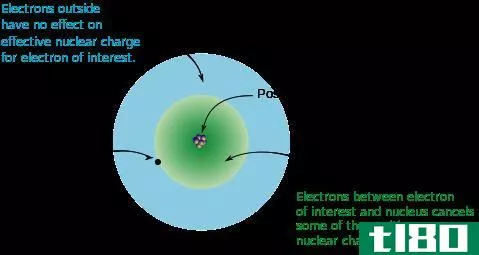
图01:电子的屏蔽效应
然而,在周期表的一个周期内,电离能值也有一些例外。例如,镁的电离能高于铝的电离能。但铝中的电子数高于镁。这是因为铝原子有3p轨道上最外层的电子,而这个电子是不成对的。这个电子被两个3s电子屏蔽。在Mg中,最外层的电子是在同一轨道上成对的两个3s电子。因此,Al价电子上的有效核电荷小于Mg价电子上的有效核电荷。因此,它很容易从铝原子中被除去,从而使电离能比镁少。
什么是屏蔽效应(screening effect)?
屏蔽效应也称为屏蔽效应。它是由于内壳层电子的存在,原子核和最外层电子之间的吸引力降低的结果。这是因为内层电子屏蔽了原子核。
屏蔽(shielding)和屏蔽效应(screening effect)的区别
- 屏蔽效应是由于电子和原子核之间引力的不同,电子云上有效核电荷的减少。屏蔽效应也称为屏蔽效应。因此,这两个术语之间没有区别。它们的意思基本相同。
总结
屏蔽效应或屏蔽效应是由于内壳层电子的存在,原子核和最外层电子之间的吸引力降低。屏蔽效应使电子上的有效核电荷减少。价电子受这种效应的影响。屏蔽效应和倾斜效应没有区别。
引用
1.“6.17:电子屏蔽”,《化学歌词》,歌词,2017年8月23日。此处提供2.“屏蔽效应”。屏蔽效应|定义|趋势|图托尔维斯塔。此处提供3.“屏蔽效应”,维基百科,维基媒体基金会,2018年3月5日。此处提供
2.“屏蔽效应。”屏蔽效应|定义|趋势|图托尔维斯塔。
3.“屏蔽效应”,维基百科,维基媒体基金会,2018年3月5日。