潜热与显热
当系统的能量因系统与周围环境的温差而变化时,我们说能量被作为热(q)传递。传热是由高温到低温,这是根据温度梯度而变化的。
潜热
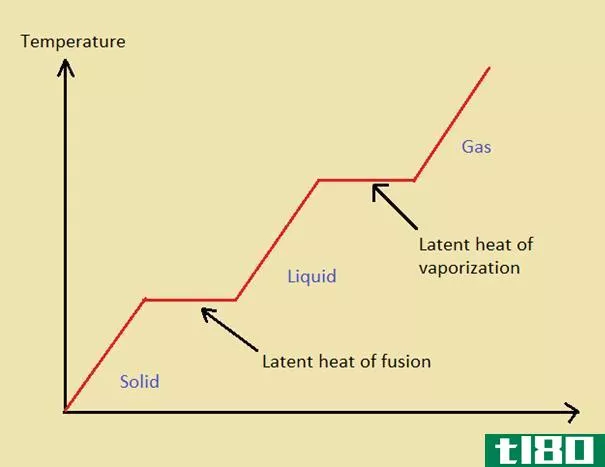
当物质发生相变时,能量以热的形式被吸收或释放。潜热是物质在相变过程中吸收或释放的热量。这种热变化在吸收或释放时不会引起温度变化。相变是指固体变为气相,液体变为固相,反之亦然。它是一种自发的转化,发生在给定压力的特征温度下。所以潜热的两种形式是熔化潜热和汽化潜热。熔化潜热发生在熔化或冻结过程中。汽化潜热发生在沸腾或冷凝过程中。在将气体转化为液体或液体转化为固体时,相变会释放热量(放热)。当从固体变为液体或液体变为气体时,相变吸收能量/热量(吸热)。例如,在蒸汽状态下,水分子的能量很高。而且没有分子间的引力。它们以单个水分子的形式运动。与此相比,液态水分子的能量较低。然而,如果一些水分子具有较高的动能,它们能够逃逸到蒸气状态。在常温下,汽态和液态水分子之间会有平衡。但是,当加热到沸点时,大部分水分子会释放到蒸汽状态。所以,当水分子蒸发时,水分子之间的氢键必须被打破。为此,需要能量,这种能量被称为汽化潜热。对于水,这种相变发生在100°C(水的沸点)下。然而,当这种相变发生在这个温度下时,热能被水分子吸收,使键断裂,但它不会使温度升高更多。
比热是指将一个相完全转化为一个物质单位质量的另一个相所需的热能。
显热
显热是热力学反应过程中能量传递的一种形式,它使温度发生变化。物质的显热可用下列公式计算。
Q=mc∆T
Q=显热
M=物质质量
C=比热容
∆T=热能引起的温度变化
| 潜热和显热有什么区别?•潜热不影响物质的温度,而显热影响温度并使其升高或降低。•潜热在相变时被吸收或释放。显热是指除相变以外的任何热力学过程中释放或吸收的热量。•例如,当将水加热到25°C至100°C时,所提供的能量会导致温度升高。因此,这种热被称为显热。但当水在100℃蒸发时,不会引起温度升高。此时吸收的热量称为潜热。 |