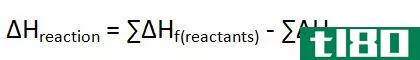热容与比热的关键区别在于,热容与物质的量有关,而比热容与物质的量无关。
当我们加热一种物质时,它的温度升高,当我们冷却它时,它的温度降低。这种温差与供给的热量成正比。热容和比热是与温度变化和热量有关的两个比例常数。
目录
1. 概述和主要区别
2. 热容是多少
3. 什么是比热
4. 并列比较-热容与比热的表格形式
5. 摘要
什么是热容(heat capacity)?
在热力学中,系统的总能量是内能。内能指的是系统中分子的总动能和势能。我们可以通过对系统做功或加热来改变系统的内能。物质的内能随着温度的升高而增加。增加量取决于加热的条件。在这里,我们需要热量来提高温度。
一种物质的热容(C)是“使一种物质的温度升高一摄氏度(或一开尔文)所需的热量。”热容因物质而异。物质的量与热容成正比。也就是说,通过使物质的质量加倍,热容就会加倍。我们需要把一种物质的温度从t1升高到t2所需要的热量可以用下面的等式来计算。
q=C x∆tq=所需热量∆t=t1-t2
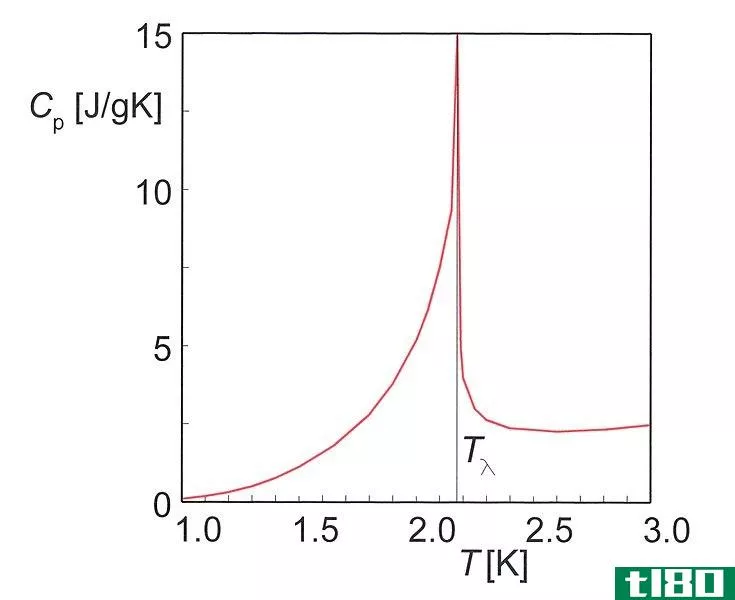
图01:氦的热容
热容单位为JºC-1或JK-1。热力学中定义了两种热容:恒压热容和定容热容。
什么是比热(specific heat)?
热容取决于物质的量。比热或比热容是与物质量无关的热容。我们可以把它定义为“在恒定压力下使一克物质的温度升高一摄氏度(或一开尔文)所需的热量。”
比热单位为Jg-1oC-1。水的比热很高,为4.186jg-1oC-1。这意味着,要使1g水的温度升高1℃,我们需要4.186j的热能。这个高值说明了水在热调节中的作用。为了求出使一定质量的物质的温度从t1升高到t2所需的热量,可以使用以下方程式。
q=m x s x∆tq=所需热量m=物质质量∆t=t1-t2
但是,如果反应涉及相变,则上述方程式不适用;例如,当水变成气相(在沸点处),或当水结冰形成冰(在熔点处)。这是因为在相变过程中添加或去除的热量不会改变温度。
热容(heat capacity)和比热(specific heat)的区别
热容与比热的关键区别在于,热容与物质的量有关,而比热容与物质的量无关。此外,当考虑该理论时,使物质温度改变1°C或1K所需热量的热容,而比热是使1g物质温度改变1°C或1K所需的热量。

总结 - 热容(heat capacity) vs. 比热(specific heat)
热容和比热是热力学中的重要术语。热容与比热的关键区别在于,热容与物质的量有关,而比热容与物质的量无关。
引用
1赫尔曼斯汀,安妮·玛丽。“化学比热容”,ThoughtCo,2019年3月21日,可在此处查阅。