sp2与sp3的主要区别在于sp杂化轨道具有50%s轨道特性,sp2杂化轨道具有33%s轨道特性,而sp3杂化轨道具有25%s轨道特性。
术语sp,sp2和sp3,是指轨道的不同杂交导致形成杂化轨道。轨道是一个原子核周围的假想区域,其中包含该原子的电子。这些轨道可以通过杂交形成新的杂化轨道,从而形成共价化学键。根据参与杂交过程的原子轨道,有几种形式的杂交。Sp,sp2和sp3是一些常见的杂化,涉及到原子的s和p轨道。
目录
1. 概述和主要区别
2. 什么是sp
3. 什么是sp2
4. 什么是sp3
5. 并列比较——以表格形式显示的sp与sp2与sp3
6. 摘要
什么是服务提供商(sp)?
Sp杂交是最简单的杂交形式,其中s轨道与p轨道重叠形成两个新的Sp轨道。一个电子壳层包含三个p轨道。在这种杂交中,这三个p轨道中的一个与同一个原子的s轨道混合。因此,在这些原子中还有两个未杂化的p轨道。
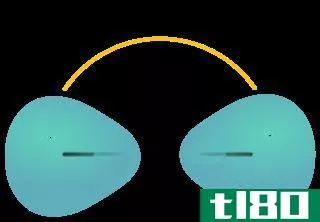
图01:sp杂化轨道的空间排列
两个原子轨道的混合比为1:1(s:p)。因此,新的混合轨道具有50%的s轨道特性和50%的p轨道特性。s和p原子轨道的这种混合形成了两个新的混合轨道。这两个轨道呈线性空间排列;将每个原子轨道指向相反的方向。这种排列使得两个轨道之间的应变最小。因此,粘结角为180°。
什么是sp2型(sp2)?
Sp2杂化是一种轨道杂交,其中一个s轨道与两个p轨道重叠形成三个新的杂交轨道。由于一个原子中有三个p原子轨道,这种杂化留下一个未杂化的p轨道。与sp杂交不同,在这种杂交形式中,每个sp2杂化轨道的s特性为33%,而p轨道特性为66%。

图02:sp2轨道的空间排列
然而,这些仅仅是近似值,因为这三个原子轨道之间的比率是s:p=1:2。
则s特性等于100/3=33.33%
p特性等于(100/3)x2=66.66%
这三个新的杂化轨道得到了三角形的平面布置,以使轨道之间的应变最小。此外,这些轨道之间的键角为120°。
什么是sp3级(sp3)?
Sp3杂交是一种轨道杂交,其中一个s轨道与三个p轨道重叠。因此,不存在未杂交的p轨道,因为所有的p轨道都参与了杂交过程。

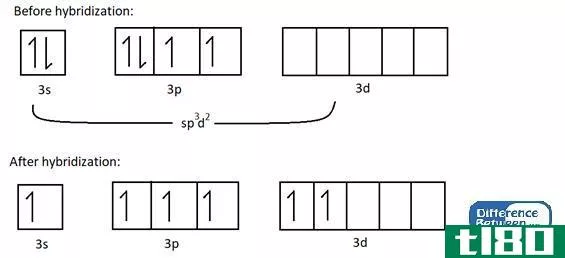
图03:sp3杂化轨道的空间排列
因此,这就产生了4个新的杂化轨道。由于s轨道与p轨道之比为1:3,因此每个杂化轨道的s特性为25%,而p轨道特性为75%。这些新的杂化轨道以109.5°键角四面体排列。
sp sp2(sp sp2)和sp3级(sp3)的区别
Sp杂交是最简单的杂交形式,其中s轨道与p轨道重叠形成两个新的Sp轨道,Sp2杂化是一种轨道杂交,其中一个s轨道与两个p轨道重叠形成三个新的杂交轨道,而Sp3杂化是一种轨道杂交,其中一个s轨道与三个p轨道重叠。这就是sp2和sp3杂化轨道的根本区别。此外,在这三种杂交形式中形成的每个新的杂化轨道都具有不同的s轨道特性,因为s轨道与不同数量的p轨道混合在一起。因此它们也有不同的p轨道特性。
然而,根据这些杂化轨道的s特性,我们可以强调sp2和sp3杂化的主要区别:sp杂化轨道具有50%s轨道特性,sp2杂化轨道具有33%s轨道特性,而sp3杂化轨道具有25%s轨道特性。此外,每次杂交都会留下不同数量的未杂交轨道。例如,sp杂化只涉及1p原子轨道。因此,它留下两个未杂化的p原子轨道。
下面的信息图显示了sp2和sp3杂交的差异的详细并排比较。
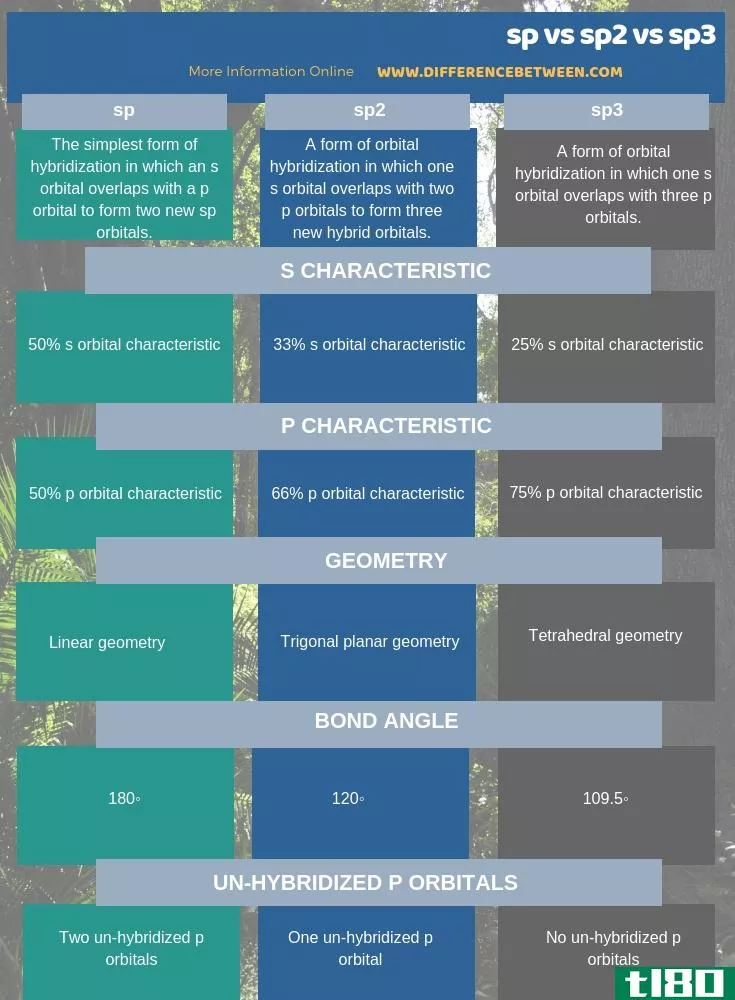
总结 - sp sp2(sp sp2) vs. sp3级(sp3)
杂化是原子轨道相互混合形成新的杂化轨道的过程,这种杂化轨道可以进行共价化学键合。原子轨道杂化最简单的形式是sp,sp2和sp3杂化。sp2与sp3的主要区别在于sp杂化轨道具有50%s轨道特性,sp2杂化轨道具有33%s轨道特性,而sp3杂化轨道具有25%s轨道特性。
引用
1“轨道杂交”,维基百科,维基媒体基金会,2018年9月13日。这里有2个。歌词。“杂交”,化学剧本,歌词,2016年7月21日。此处提供
2歌词。“杂交”,化学剧本,歌词,2016年7月21日。