价键理论(valence bond theory)和分子轨道理论(molecular orbital theory)的区别
主差价键理论(main difference valence bond theory) vs. 分子轨道理论(molecular orbital theory)
原子由电子所在的轨道组成。这些原子轨道可以在不同的形状和不同的能级上找到。当一个原子与其他原子结合在分子中时,这些轨道以不同的方式排列。这些轨道的排列将决定分子的化学键和形状或几何。为了解释这些轨道的排列,我们可以使用价键理论或分子轨道理论。价键理论与分子轨道理论的主要区别在于价键理论解释了轨道的杂化,而分子轨道理论没有详细说明轨道的杂化。
覆盖的关键领域
1.什么是价键理论-定义、理论、实例2.什么是分子轨道理论-定义、理论、实例3.价键理论和分子轨道理论的区别是什么-主要区别的比较
Key Terms: Antibonding Molecular Orbitals, Bonding Molecular Orbitals, Hybridization, Hybrid Orbitals, Molecular Orbital Theory, Pi Bond, Sigma Bond, sp Orbital, sp2 Orbital, sp3 Orbital, sp3d1 Orbital, Valence Bond Theory
什么是价键理论(valence bond theory)?
价键理论是用来解释分子中原子化学键的基本理论。价键理论通过轨道的重叠来解释电子的配对。原子轨道主要有s轨道、p轨道和d轨道。根据价键理论,两个s轨道的重叠或p轨道的头对头重叠将形成sigma键。两个平行p轨道的重叠将形成π键。因此,单键将只包含一个sigma键,而双键将包含一个sigma键和一个pi键。三键可以包含一个sigma键和两个pi键。
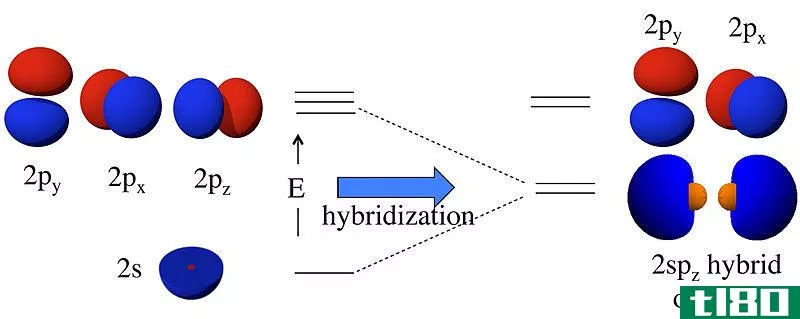
简单的分子,例如H2,由于氢(H)原子只由s轨道组成,所以仅仅通过轨道的重叠就形成了sigma键。但是对于由s和p轨道组成的原子,它们有着不成对的电子,价键理论有一个称为“杂化”的概念。
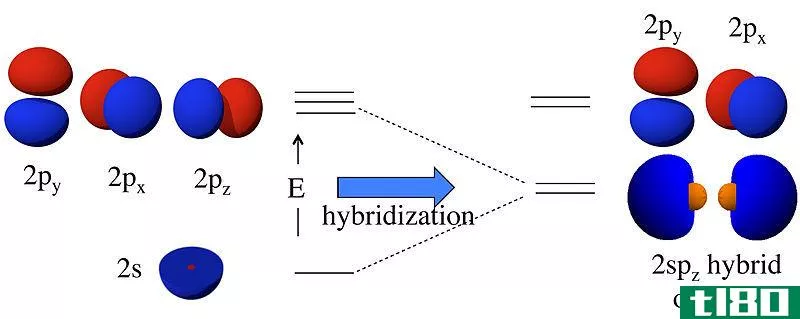
杂化轨道导致杂化轨道。这些杂化轨道的排列方式使得这些轨道之间的斥力最小化。下面是一些混合轨道。
sp轨道
这个杂化轨道是s轨道与p轨道杂化后形成的。因此,sp轨道具有50%的s轨道特性和50%的p轨道特性。由sp杂化轨道组成的原子有两个未杂化的p轨道。因此,这两个p轨道可以平行重叠形成两个π键。杂化轨道的最终排列是线性的。
sp2轨道
这个杂化轨道是由一个s轨道和两个p轨道杂化而成的。因此,这个sp2杂化轨道包含约33%的s轨道性质和约67%的p轨道性质。经过这种杂交的原子由一个未杂交的p轨道组成。杂化轨道的最终排列是三角平面的。
sp3轨道
这种混合轨道是由s轨道与三个p轨道杂交而成。因此,sp3杂化轨道包含约25%的s轨道性质和大约75%的p轨道性质。经过这种杂交的原子没有未杂交的p轨道。混合轨道的最终排列是四面体。
sp3d1轨道
这种杂化包括一个s轨道,三个p轨道和一个d轨道。
这些杂化轨道将决定分子的最终几何形状或形状。

Figure 1: Geometry of CH4 is tetrahedral
上图显示了CH4分子的几何结构。它是四面体的。灰色轨道是碳原子的sp3杂化轨道,而蓝色轨道是氢原子的s轨道,与形成共价键的碳原子杂化轨道重叠。
什么是分子轨道理论(molecular orbital theory)?
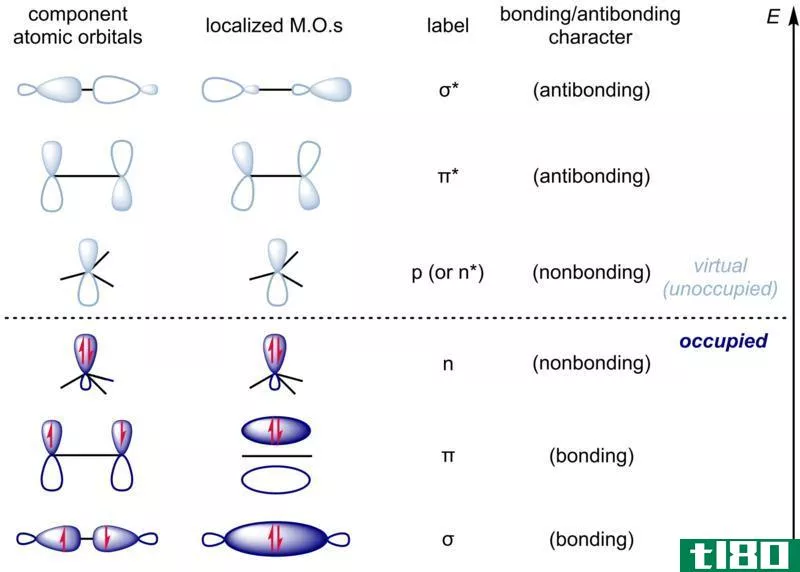
分子轨道理论用假设的分子轨道解释了分子的化学键。它还描述了当原子轨道重叠(混合)时,分子轨道是如何形成的。根据这个理论,一个分子轨道最多可以容纳两个电子。这些电子有相反的自旋,以尽量减少它们之间的排斥。这些电子称为键电子对。正如这个理论所解释的,分子轨道可以有两种类型:成键分子轨道和反键分子轨道。
成键分子轨道
成键分子轨道的能量低于原子轨道(参与分子轨道形成的原子轨道)。因此,键合轨道是稳定的。键合分子轨道用符号表示σ.
反键分子轨道
反键分子轨道的能量比原子轨道高。因此,这些反键轨道与键合轨道和原子轨道相比是不稳定的。给出了反键分子轨道的符号σ*.
成键分子轨道导致化学键的形成。这种化学键可以是sigma键或pi键。反键轨道与化学键的形成无关。他们居住在债券之外。当头与头重叠时形成sigma键。π键是在轨道的内侧和外侧重叠处形成的。

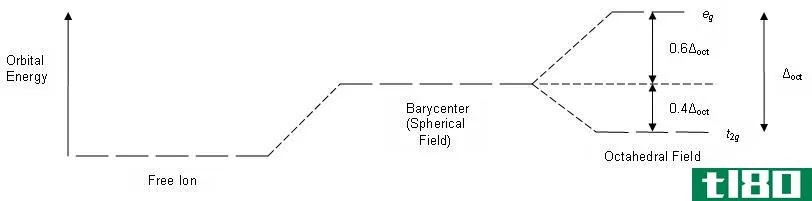
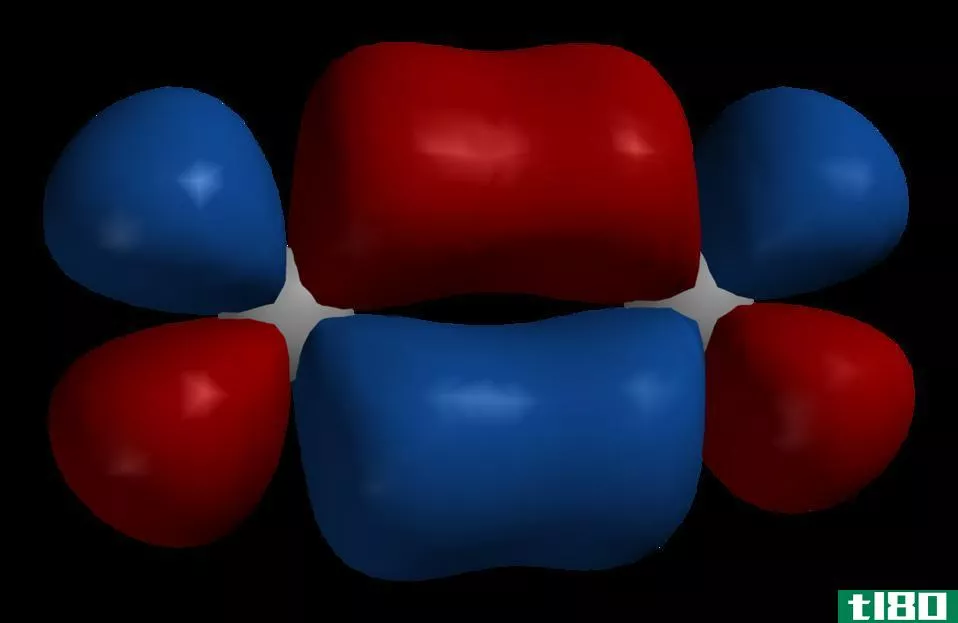
Figure 2: Molecular orbital diagram for the bonding in oxygen molecule
在上图中,两个氧原子的原子轨道显示在左边和右边。在中间,氧分子的分子轨道表现为成键轨道和反键轨道。
价键理论(valence bond theory)和分子轨道理论(molecular orbital theory)的区别
定义
价键理论:价键理论是用来解释分子中原子化学键的基本理论。
分子轨道理论:分子轨道理论用假想的分子轨道解释分子的化学键。
分子轨道
价键理论:价键理论没有给出分子轨道的细节。它解释了原子轨道的键合。
分子轨道理论:分子轨道理论是在分子轨道的基础上发展起来的。
轨道类型
价键理论:价键理论描述杂化轨道。
分子轨道理论:分子轨道理论描述成键分子轨道和反键分子轨道。
杂交
价键理论:价键理论解释了分子轨道的杂化。
分子轨道理论:分子轨道理论不能解释轨道的杂化。
结论
用价键理论和分子轨道理论解释了分子中原子间的化学键。然而,价键理论不能用来解释复杂分子中的键合。它非常适合于双原子分子。但是分子轨道理论可以用来解释任何分子中的成键。因此,它比价键理论有许多先进的应用。这就是价键理论和分子轨道理论的区别。
引用
1.《分子轨道理论》化学libretext。Libretexts,2016年7月21日,网络。这里有。2017年8月9日。 2.《价键理论与混合原子轨道〉价键理论与混合原子轨道。N.p.,N.d.网站。这里有。2017年8月9日。 2.《价键理论与混合原子轨道〉价键理论与混合原子轨道。N.p.,N.d.网站。
- 发表于 2021-06-29 10:32
- 阅读 ( 400 )
- 分类:科学
你可能感兴趣的文章
分子轨道理论(molecular orbital theory)和杂交理论(hybridization theory)的区别
...-分子轨道理论与杂交理论 5. 摘要 什么是分子轨道理论(molecular orbital theory)? 分子轨道理论是用量子力学描述分子电子结构的技术。这是解释分子中化学键的最有效的方法。让我们详细讨论一下这个理论。 首先,我们需要知道...
- 发布于 2020-10-15 22:50
- 阅读 ( 835 )
反键合(antibonding)和非键合(nonbonding)的区别
...示为σ*。 什么是非键合(nonbonding)? Nonbonding orbital is the molecular orbital in which addition or removal of electr*** neither increases or decreases the bond order between atoms. We often designate this orbital by “n”. These orbitals resemble the lone electron pairs in Lewis struc...
- 发布于 2020-10-16 03:12
- 阅读 ( 1264 )
碰撞理论(collision theory)和过渡态理论(transition state theory)的区别
关键区别-碰撞理论与过渡状态理论 碰撞理论和过渡态理论是在分子水平上解释不同化学反应速率的两种理论。碰撞理论描述了气相化学反应中气体分子的碰撞。过渡态理论通过假设过渡态中间化合物的形成来解释反应速率。...
- 发布于 2020-10-16 12:41
- 阅读 ( 680 )
混合的(hybrid)和简并轨道(degenerate orbitals)的区别
...。 图01:Sp杂交 杂化的概念首先被讨论是因为科学家发现价键理论不能正确地预测某些分子如CH4的结构。虽然根据碳原子的电子构型,碳原子只有两个不成对的电子,但它可以形成四个共价键。为了形成四个键,必须有四个不成...
- 发布于 2020-10-16 17:47
- 阅读 ( 895 )
经典理论(classical theory)和量子理论(quantum theory)的区别
...间的电子跃迁 此外,这个理论对于确定原子如何通过共价键相互结合很重要。此外,量子理论应用的领域还包括电子学、密码学、量子计算等。 经典理论(classical theory)和量子理论(quantum theory)的区别 经典力学理论是描述宏观物...
- 发布于 2020-10-17 07:17
- 阅读 ( 428 )
vbt公司(vbt)和cft公司(cft)的区别
关键区别——vbt与cft VBT一词代表价键理论。它是一种用来描述原子间不同化学键形成的理论。这个理论解释了原子轨道的重叠或混合形成化学键。CFT一词代表晶体场理论。它是一个用来解释电子轨道(通常是d或f轨道)的简...
- 发布于 2020-10-19 11:35
- 阅读 ( 462 )
物质的粒子模型(particle model of matter)和分子动力学理论(kinetic molecular theory)的区别
...的粒子模型(particle model of matter)和分子动力学理论(kinetic molecular theory)的区别 物质的粒子模型是用来解释存在于任何物质中的原子、分子或离子排列的模型。分子动力学理论是用来解释气体物理性质的理论。物质的粒子模型和动...
- 发布于 2020-10-23 17:56
- 阅读 ( 685 )
晶体场理论(crystal field theory)和配位场理论(ligand field theory)的区别
...作用。配体场理论(LFT)将金属与配体的相互作用视为共价键的相互作用,并依赖于金属与配体上d-轨道的取向和重叠。这是晶体场理论和配体场理论的关键区别。 什么是晶体场理论(crystal field theory)? 晶体场理论(CFT)由物理...
- 发布于 2020-10-24 03:34
- 阅读 ( 742 )
分子轨道(molecular orbital)和原子轨道(atomic orbital)的区别
...子轨道和原子轨道的表格形式 5. 摘要 什么是分子轨道(a molecular orbital)? 原子结合在一起形成分子。当两个原子靠得更近形成一个分子时,原子轨道重叠并结合成分子轨道。新形成的分子轨道数等于组合原子轨道数。此外,分子...
- 发布于 2020-10-24 07:58
- 阅读 ( 558 )
道尔顿原子理论(dalton’s atomic theory)和现代原子理论(modern atomic theory)的区别
道尔顿原子理论(dalton’s atomic theory)和现代原子理论(modern atomic theory)的区别 道尔顿的原子理论是关于原子的最古老的理论。1808年,约翰道尔顿(johndalton)发表了他的理论,该理论由几个基于他的实验和化学结合定律建立的...
- 发布于 2020-10-25 03:59
- 阅读 ( 804 )