分子轨道理论和杂化理论的主要区别在于分子轨道理论描述了成键轨道和反键轨道的形成,而杂交理论描述了杂化轨道的形成。
有不同的理论发展来确定分子的电子结构和轨道结构。VSEPR理论、Lewis理论、价键理论、杂化理论和分子轨道理论是这些重要的理论。其中最能被接受的理论是分子轨道理论。
目录
1. 概述和主要区别
2. 什么是分子轨道理论
3. 什么是杂交理论
4. 并列比较-分子轨道理论与杂交理论
5. 摘要
什么是分子轨道理论(molecular orbital theory)?
分子轨道理论是用量子力学描述分子电子结构的技术。这是解释分子中化学键的最有效的方法。让我们详细讨论一下这个理论。
首先,我们需要知道什么是分子轨道。当两个原子核之间的净吸引力和原子核之间的电子之间的净吸引力超过两个原子核之间的静电斥力时,两个原子之间就形成了化学键。基本上,这意味着,两个原子之间的吸引力应该大于这两个原子之间的排斥力。在这里,电子必须存在于一个叫做“结合区”的区域,才能形成这种化学键。否则,电子将处于“反束缚区”,这将有助于原子间的排斥力。
然而,如果满足了这些要求并且两个原子之间形成了化学键,那么与键合有关的相应轨道称为分子轨道。在这里,我们可以从两个原子的两个轨道开始,到属于两个原子的一个轨道(分子轨道)结束。
根据量子力学,原子轨道不能如我们所愿出现或消失。当轨道相互作用时,它们往往会相应地改变形状。但根据量子力学,它们可以自由改变形状,但需要有相同数量的轨道。然后我们需要找到丢失的轨道。在这里,两个原子轨道的同相结合形成成键轨道,而异相结合形成反键轨道。

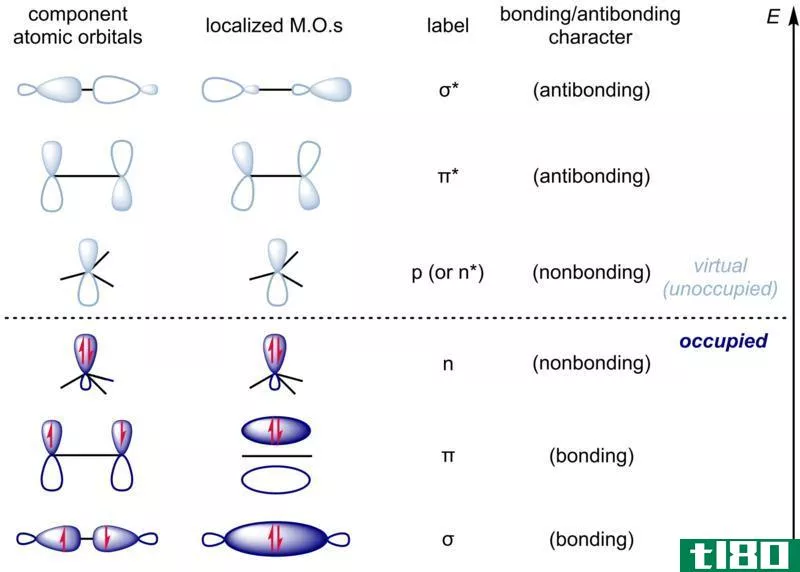
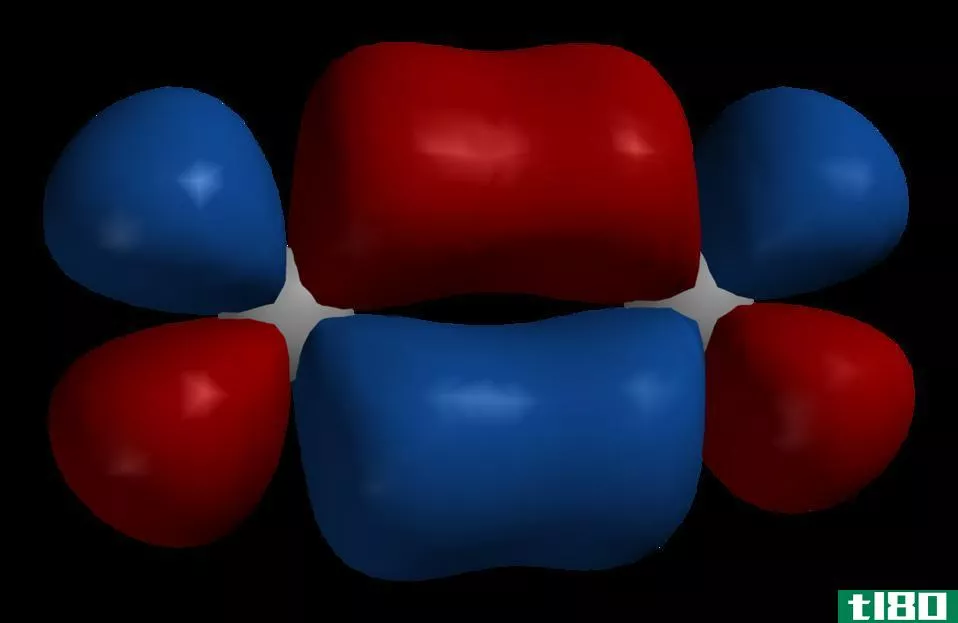
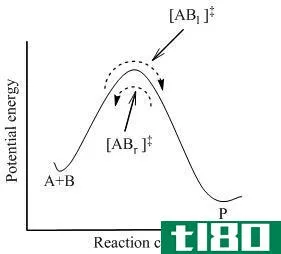
图01:分子轨道图
成键电子占据成键轨道,而反键轨道上的电子不参与成键。相反,这些电子积极地反对化学键的形成。成键轨道的势能比反键轨道低。如果我们考虑σ键,键轨道的表示是σ,反键轨道是σ*。我们可以用这个理论来描述复杂分子的结构,来解释为什么有些分子不存在(如He2)和分子的键序。因此,这一描述简要地解释了分子轨道理论的基础。
什么是杂交理论(hybridization theory)?
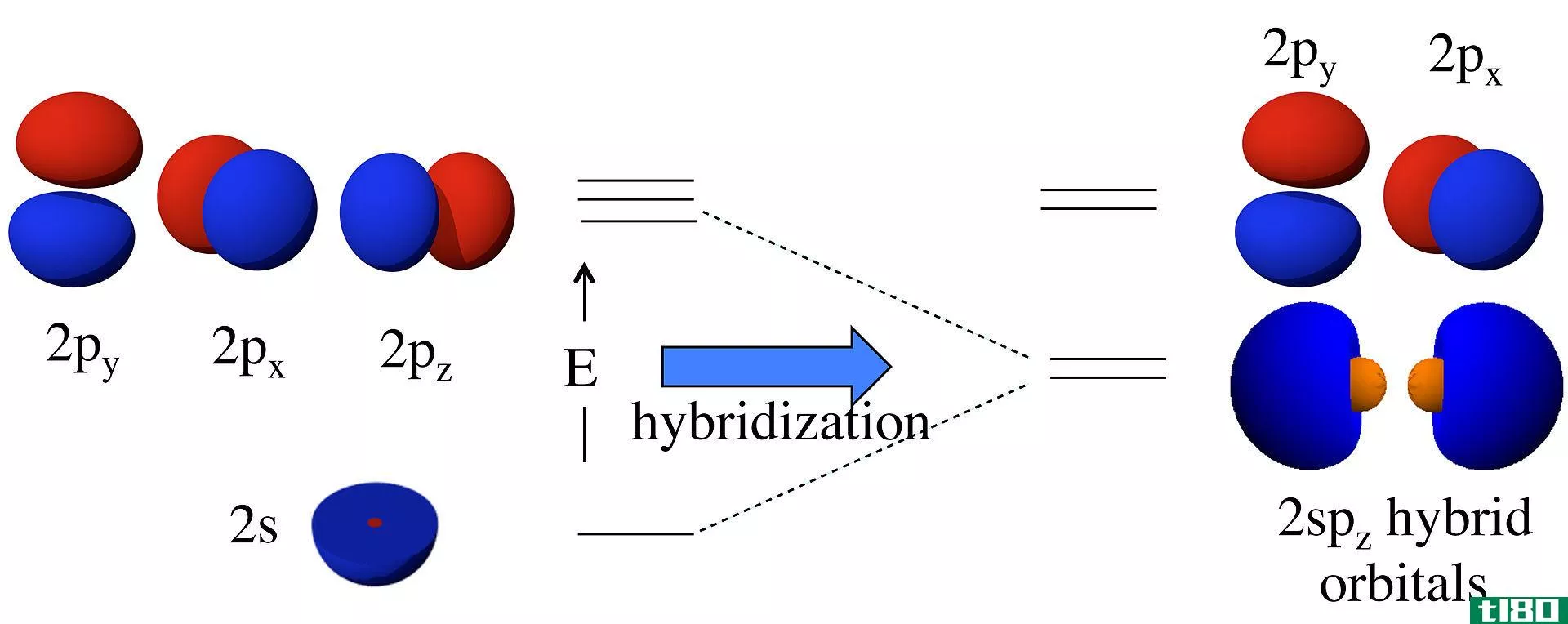
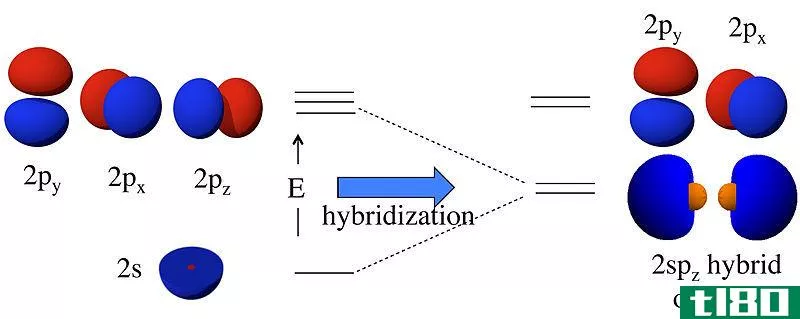
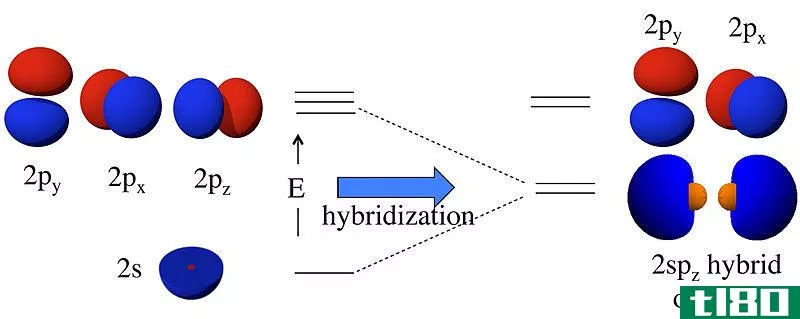
杂化理论是我们用来描述分子轨道结构的一种技术。杂化是通过混合两个或多个原子轨道而形成的杂化轨道。这些轨道的方向决定了分子的几何形状。它是价键理论的扩展。
在原子轨道形成之前,它们具有不同的能量,但在形成之后,所有的轨道都具有相同的能量。例如,一个s原子轨道和一个p原子轨道可以组合成两个sp轨道。s和p原子轨道具有不同的能量(s的能量<p的能量)。但是在杂化之后,它形成了两个具有相同能量的sp轨道,这个能量介于单个s和p原子轨道的能量之间。此外,这个sp杂化轨道具有50%s轨道特性和50%p轨道特性。
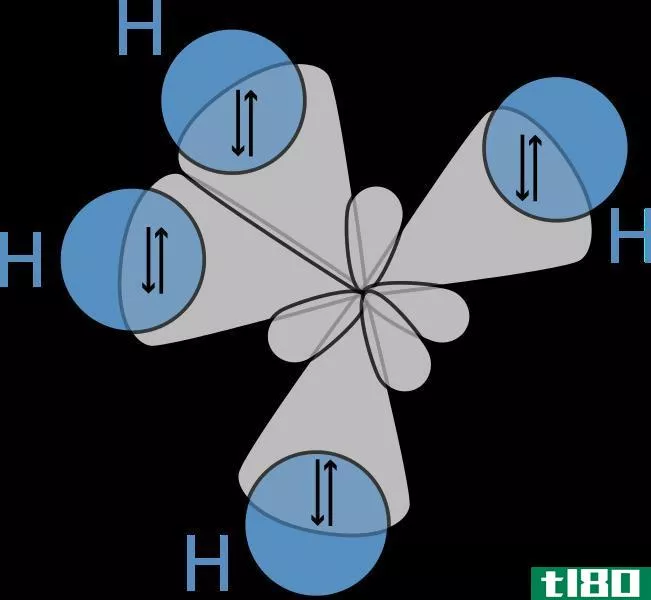
图02:碳原子杂化轨道和氢原子s轨道之间的键
杂化的想法首先进入讨论,因为科学家观察到价键理论未能正确预测某些分子(如CH4)的结构。在这里,虽然碳原子根据其电子构型只有两个不成对的电子,但它可以形成四个共价键。要形成四个键,必须有四个不成对的电子。
他们解释这种现象的唯一方法是认为碳原子的s轨道和p轨道相互融合,形成新的轨道,称为杂化轨道,它们具有相同的能量。这里,一个s+3p给出了4个sp3轨道。因此,电子均匀地填充了这些杂化轨道(每个杂化轨道一个电子),遵循Hund规则。然后有四个电子与四个氢原子形成四个共价键。
分子轨道理论(molecular orbital theory)和杂交理论(hybridization theory)的区别
分子轨道理论是用量子力学描述分子电子结构的技术。杂化理论是我们用来描述分子轨道结构的一种技术。因此,分子轨道理论和杂化理论的关键区别在于分子轨道理论描述成键和反键轨道的形成,而杂交理论描述杂化轨道的形成。
此外,根据分子轨道理论,新的轨道形式来自于两个原子的原子轨道的混合;而在杂化理论中,新的轨道形式是同一个原子的原子轨道的混合。因此,这是分子轨道理论和杂交理论的另一个区别。
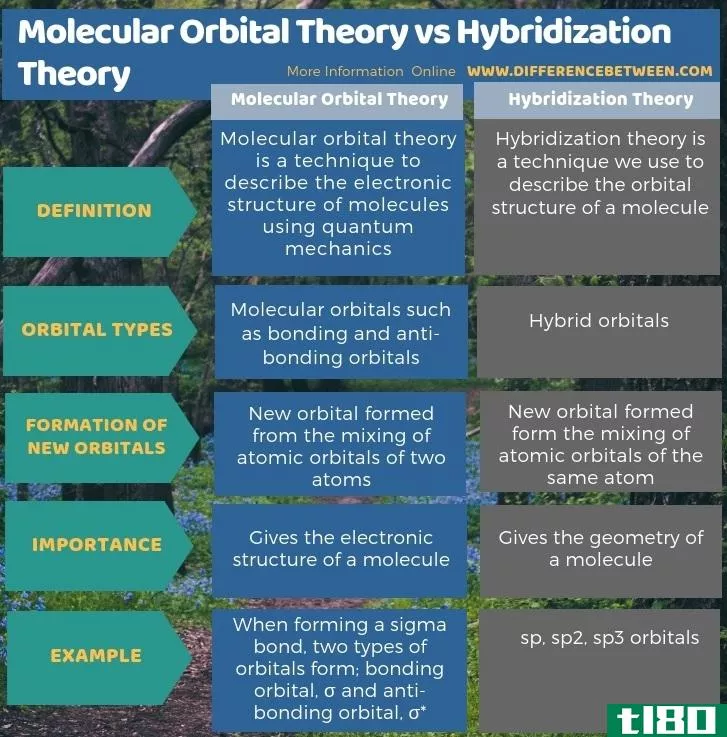
总结 - 分子轨道理论(molecular orbital theory) vs. 杂交理论(hybridization theory)
分子轨道理论和杂化理论都是决定分子结构的重要理论。分子轨道理论和杂化理论的主要区别在于分子轨道理论描述了成键轨道和反键轨道的形成,而杂交理论描述了杂化轨道的形成。
引用
1.“杂交。”化学剧本,剧本,2019年6月5日,可在这里查阅。