纯轨道和杂化轨道的关键区别在于,纯轨道是原始原子轨道,而杂化轨道是由两个或多个原子轨道混合而成。
在简单分子的化学键形成过程中,我们可以简单地考虑原子轨道的重叠。但是如果我们要讨论复杂分子中的化学键,我们需要知道什么是轨道杂交。轨道杂化是描述原子轨道混合形成新杂化轨道的化学概念。这些轨道涉及共价化学键的形成。
目录
1. 概述和主要区别
2. 什么是纯轨道
3. 什么是杂化轨道
4. 并列比较-纯轨道与混合轨道的表格形式
5. 摘要
什么是纯轨道(pure orbitals)?
纯原子轨道包含纯原子轨道。这些轨道不是像混合轨道那样的混合轨道。轨道给出了原子中电子最可能的位置,因为电子在原子核周围连续运动。这不是一个固定的位置,而是一个电子在某个特定时间出现的区域。
纯原子轨道以球形、哑铃形等多种形式存在。根据量子力学的一个名字,我们用了一个量子力学的名字。这组数字包括n(主量子数)、l(角动量量子数)、m(磁量子数)和s(自旋量子数)。每个轨道最多占据两个电子。根据角动量量子数,已知的原子轨道有四种:s轨道(球形)、p轨道(哑铃形)、d轨道(同一平面上的两个哑铃)和f轨道(一种复杂的结构)。
什么是杂化轨道(hybrid orbitals)?
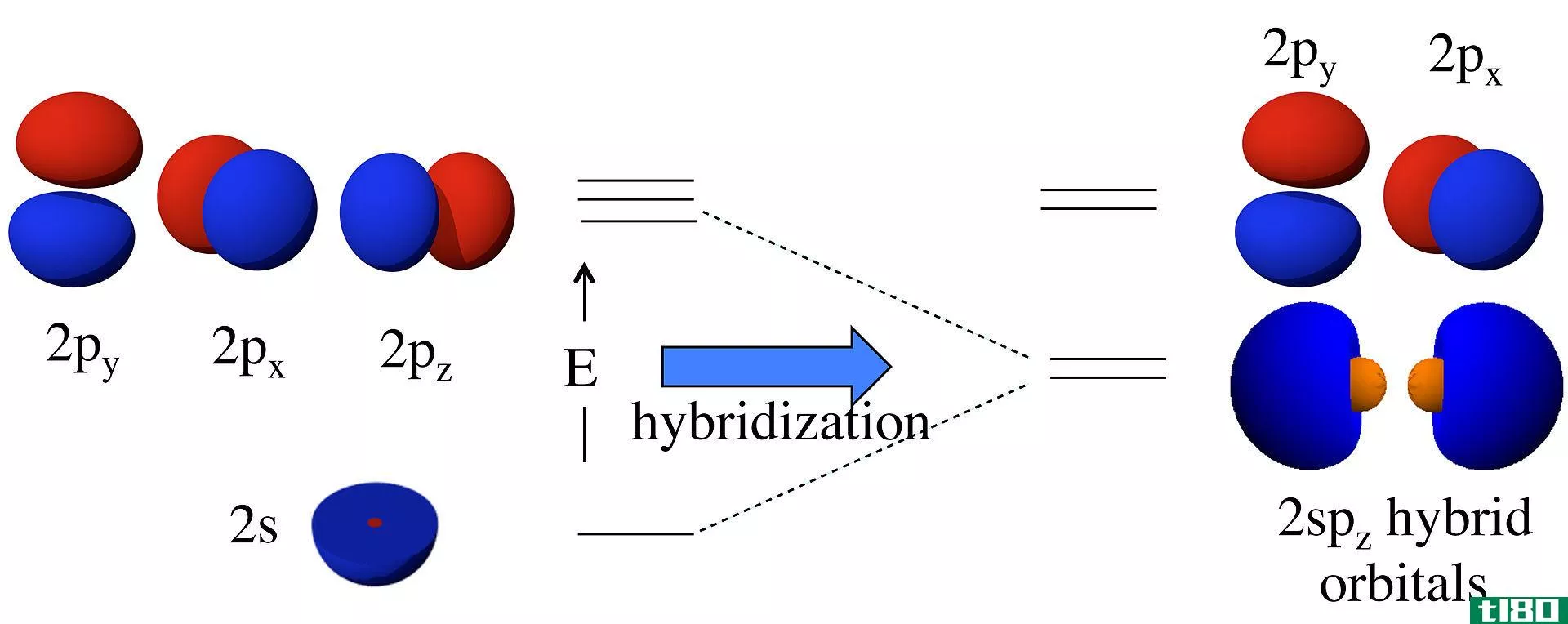
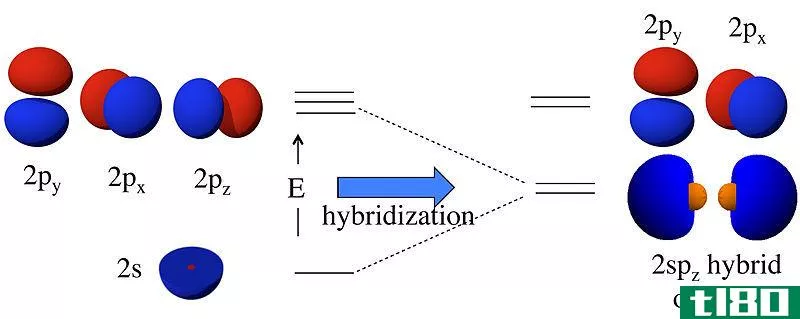
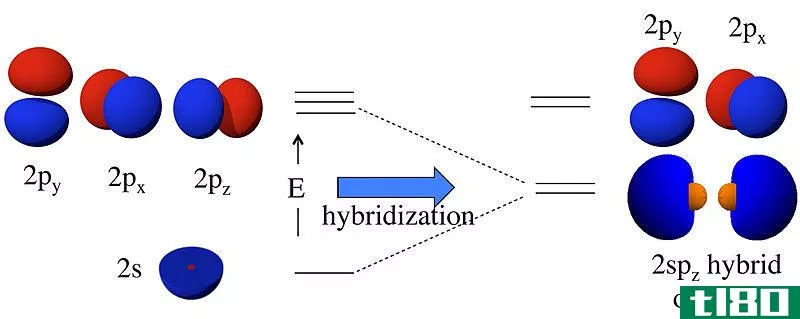
杂化轨道是由原子轨道混合而成的分子轨道。这些是假设的轨道。混合发生在同一个原子的原子轨道之间。这种混合是为了与另一个原子形成共价化学键。这种混合的过程是“轨道杂交”,产生杂交轨道。我们根据经过杂交的原子轨道来命名这些轨道。

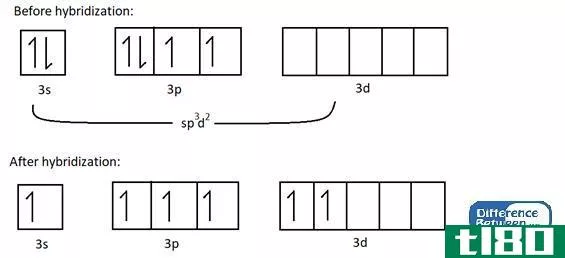
图01:sp3杂交
因此,杂化轨道的三种主要形式是:
- sp hybrid orbital – this forms due to the hybridization of s and p atomic orbitals. Therefore the resulting hybrid orbital has 50% s characteristics and 50% p orbital characteristics. This hybrid orbital has a linear spatial arrangement.
- sp2 hybrid orbital – this forms due to the hybridization of one s and two p orbitals. Therefore the resulting hybrid orbital has 33% of s orbital characteristics and 66% of p orbital characteristic. The spatial arrangement is trigonal planar.
- sp3 hybrid orbital – this forms due to the hybridization of one s and three p orbitals. Hence the resulting hybrid orbital has 25% s characteristics and 75% p characteristics. The spatial arrangement of these hybrid orbitals is tetrahedral.
纯净的(pure)和杂化轨道(hybrid orbitals)的区别
纯轨道是包含原子电子的原子轨道,而混合轨道是由原子轨道混合而成的分子轨道。这就是纯轨道和混合轨道之间的关键区别。此外,杂化轨道是通过轨道杂交形成的,但纯轨道不是杂化的。此外,杂化轨道的形成在通过共价化学键形成复杂化合物的过程中起着重要作用。在考虑轨道的命名时,我们将纯轨道命名为s、p、d和f轨道,而将混合轨道命名为sp、sp2、sp3等。
下面的信息图表列出了纯轨道和混合轨道之间的差异,以便快速参考。

总结 - 纯净的(pure) vs. 杂化轨道(hybrid orbitals)
原子轨道是原子中电子存在的区域。在这篇文章中,我们描述了纯轨道和混合轨道两种类型。纯轨道和杂化轨道的关键区别在于,纯轨道是原始的原子轨道,而杂化轨道则是由两个或多个原子轨道混合而成。
引用
1歌词。“杂化轨道”,化学剧本,歌词,2016年7月21日。此处提供
Image Courtesy: