杂化与重叠的关键区别在于,杂化是指通过原子轨道的重叠形成新的杂化轨道,而重叠则是指原子轨道的混合。
轨道是可以充满电子的假想结构。根据不同的发现,科学家们提出了这些轨道的不同形状。轨道主要有三种类型:原子轨道、分子轨道和杂化轨道。杂交轨道是通过杂交过程形成的。杂化和重叠是两个相关的化学概念。原子轨道的重叠发生在杂交过程中。
目录
1. 概述和主要区别
2. 什么是杂交
3. 什么是重叠
4. 并列比较-杂交与表格形式的重叠
5. 摘要
什么是杂交(hybridization)?
杂化是由原子轨道的混合形成杂化轨道的化学过程。杂化理论是我们用来描述分子轨道结构的一种技术。基本上,杂化是通过混合两个或多个原子轨道来形成杂化轨道。这些轨道的方向决定了分子的几何形状。它是价键理论的扩展。
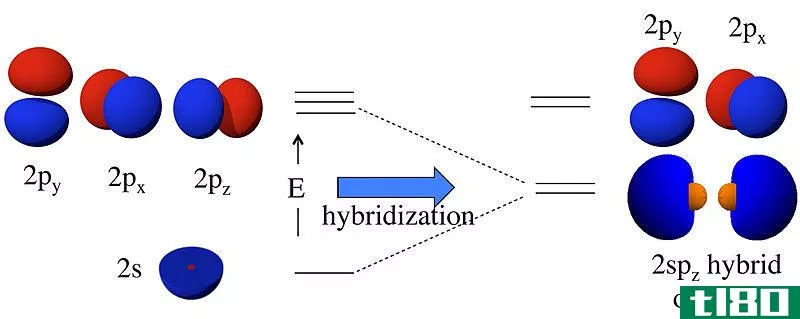
在原子轨道形成之前,它们具有不同的能量,但在形成之后,所有的轨道都具有相同的能量。例如,一个s原子轨道和一个p原子轨道可以组合成两个sp轨道。s和p原子轨道具有不同的能量(s的能量<p的能量)。但是,杂化后,它形成了两个具有相同能量的sp轨道,这个能量介于单个s和p原子轨道的能量之间。此外,这个sp杂化轨道具有50%s轨道特性和50%p轨道特性。
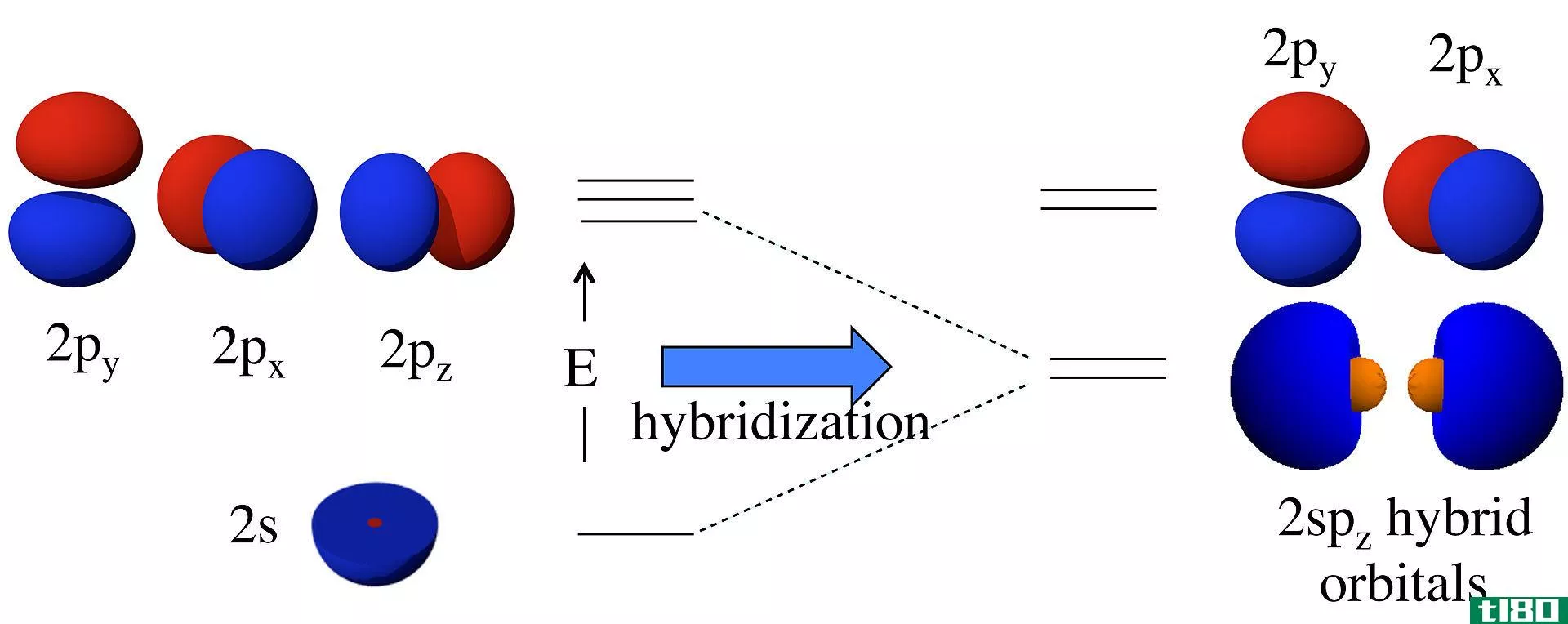
图01:杂化轨道的形成
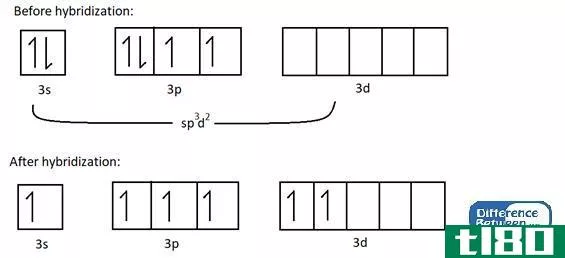
杂化的概念首次被讨论是因为价键理论未能正确预测某些分子如CH4的结构。尽管CH4中的碳原子根据其电子构型只有两个不成对电子,但它可以形成四个共价键。要形成四个键,必须有四个不成对的电子。
解释这一现象的唯一方法是认为碳原子的s轨道和p轨道相互融合,形成新的轨道,称为杂化轨道,它们具有相同的能量。这里,一个s+3p给出了4个sp3轨道。因此,电子均匀地填充了这些杂化轨道(每个杂化轨道一个电子),遵循Hund规则。因此,有四个电子与四个氢原子形成四个共价键。
什么是重叠(overlapping)?
重叠是原子轨道相互重叠的化学过程。换言之,是不同原子间轨道的集中,导致化学键的形成。Linus Pauling首先提出了轨道重叠的理论。他解释了不同分子的分子键角,这个概念是杂化理论的基础。
杂交(hybridization)和重叠(overlapping)的区别
杂化和重叠是两个相关的化学概念。杂化和重叠的关键区别在于杂化是通过原子轨道的重叠形成新的杂化轨道,而重叠则是原子轨道的混合。此外,在杂化过程中,相同原子的轨道重叠形成杂化轨道,而在重叠过程中,同一原子的轨道重叠形成杂化轨道,不同原子的轨道重叠形成化学键。
下面的信息图提供了更多关于杂交和重叠之间区别的事实。

总结 - 杂交(hybridization) vs. 重叠(overlapping)
杂化和重叠是两个相关的化学概念。杂化的关键是杂化和杂化轨道的重叠,而杂化的关键是杂化轨道的重叠。
引用
1赫尔曼斯汀,安妮·玛丽。“混合轨道定义”,ThoughtCo,2018年6月22日,可在这里查阅。