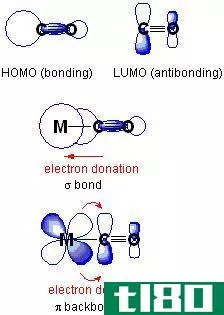
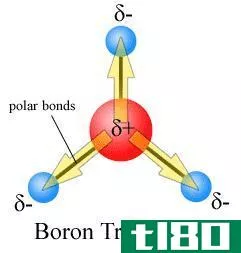
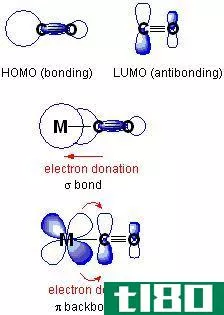
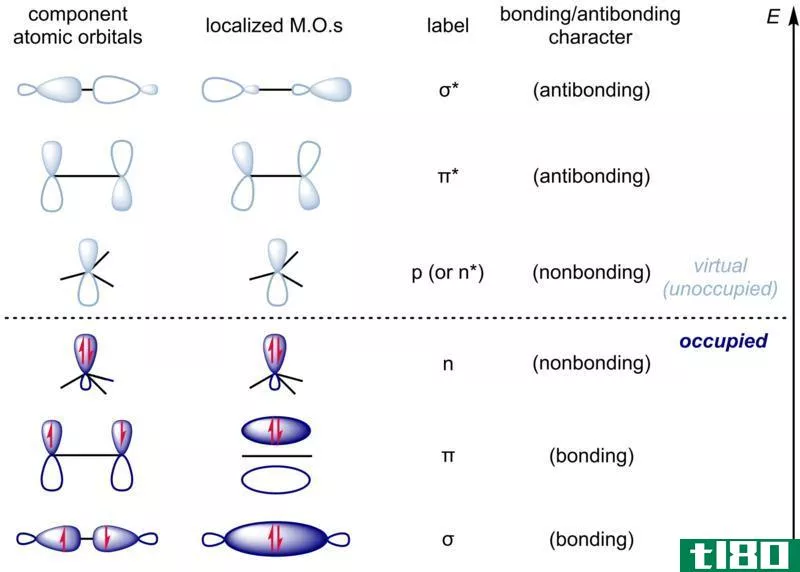
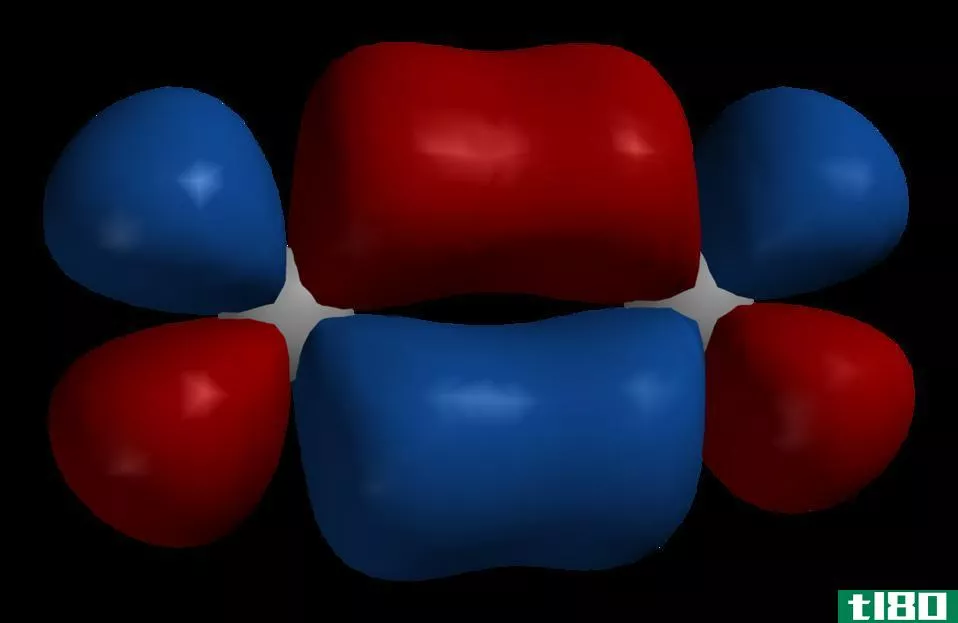
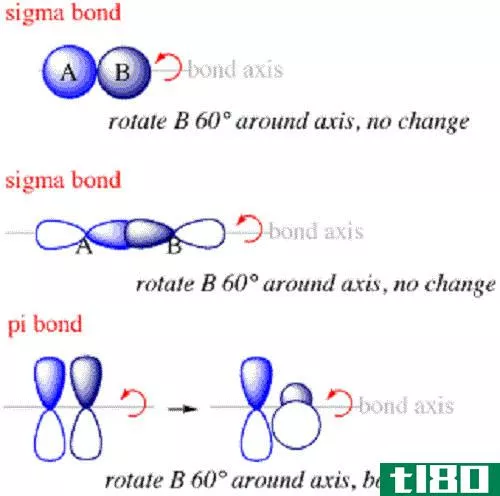
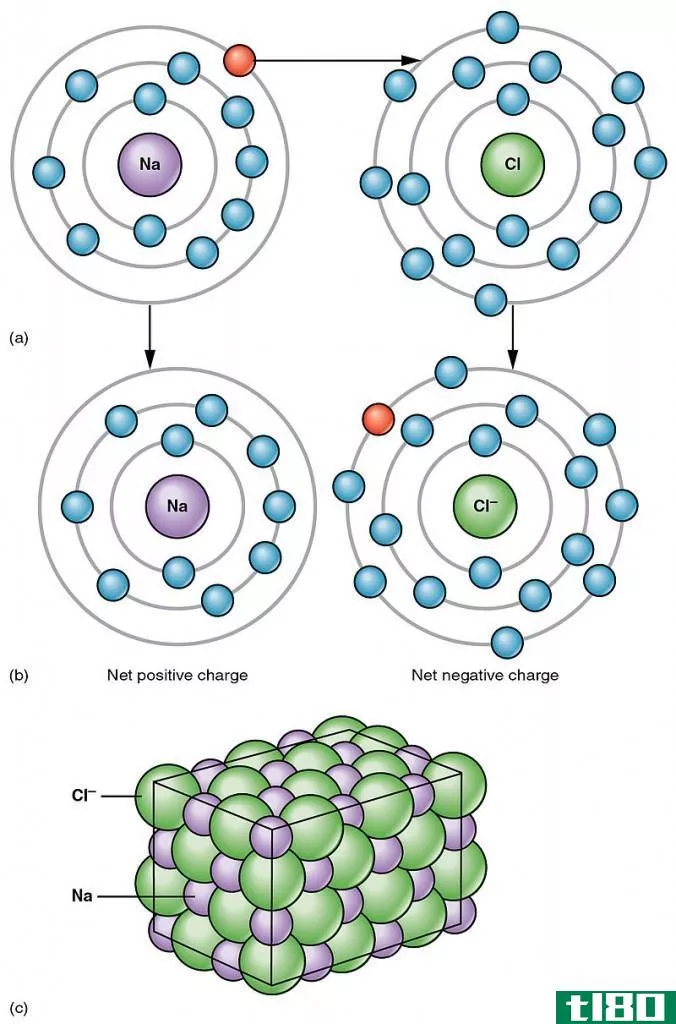
成键与反键分子轨道
这两种分子轨道间的化学键可以用化学键和分子轨道键的不同来解释。键和反键分子轨道之间最显著的区别是它们相对于母原子轨道的能级。这种能级差异导致了两个分子轨道之间的其他差异。
成键和反键分子轨道是由线性组合原子轨道形成的。为了理解成键和反键分子轨道之间的区别,以下几个关键概念非常重要。
Aufbau原理-能量最低的轨道首先被填满。
泡利不相容原理——占据一个轨道的最大电子数(自旋相反)是两个。
亨德定律——当有几个能量相等的分子轨道时,电子一次占据一个分子轨道,两个电子占据同一个分子轨道。
什么是键合分子轨道(bonding molecular orbitals)?
键合分子轨道是由原子轨道通过原子轨道的同相结合而形成的。它增加了键合原子之间的电子密度。它们的能量低于原子轨道。电子首先被填充到键合分子轨道上,它们稳定了分子,因为它们比母体原子中的电子结合的能量少。

氢的分子轨道图
什么是反键分子轨道(antibonding molecular orbitals)?
反键分子轨道是由原子轨道的异相结合形成的,它降低了两个原子之间的电子密度。在反键分子轨道中,能量高于形成它们的原子轨道。由于这个事实,当电子被填充到反键分子轨道中时,它会破坏两个原子之间的键。
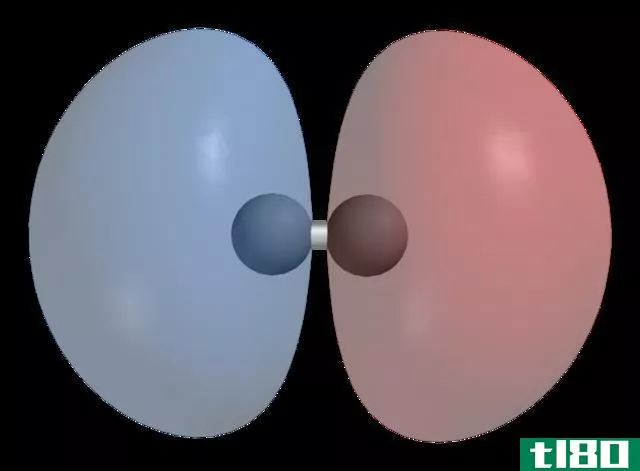
h21sσ*反键分子轨道
键合分子轨道(bonding molecular orbitals)和反键分子轨道(antibonding molecular orbitals)的区别
•能源:
能量键合分子轨道>;能键分子轨道
•与母原子轨道相比,键合分子轨道的能量更低。
•反键分子轨道比母体原子轨道具有更高的能量。
•一般来说,电子首先被填充到较低的能级。因此,电子首先填充到成键分子轨道,然后填充到反键分子轨道。
•稳定性:
•成键分子轨道比反键分子轨道和母体原子轨道更稳定。
•反键分子轨道比键合分子轨道和母体原子轨道都不稳定。
•稳定性差异的主要原因是能级差异。能量越高,稳定性越差。能量越低,稳定性越强。
•电子可用性:
•在键合分子轨道中找到电子的概率非常高。
•在反键分子轨道中找到一个电子是最低限度的。
•对分子形状的贡献:
•键合分子轨道直接影响分子的形状。
•反键分子轨道不会影响分子的形状。
- 用CCoil测氢钼图(CC by-SA 3.0)
- 利用Wikicomm***(公共领域)研究H2 1sσ*反键分子轨道