dπ-dπ键与δ键的主要区别在于dπ-dπ键是在填充d原子轨道和空d原子轨道之间形成的,而δ键是在一个原子轨道的四个波瓣和另一个原子轨道的四个波瓣之间形成的。
dπ-dπ键和δ键都是通过原子轨道的重叠形成的。dπ-dπ键形成过程中轨道的重叠形成了一个配位键,而δ键形成过程中的重叠形成了共价化学键。
目录
1. 概述和主要区别
2.什么是dπ-dπ键
3. 什么是三角洲债券
4. 并列比较-dπ-dπ键与δ键的表格形式
5. 摘要
什么是dπ-dπ键(dπ-dπ bond)?
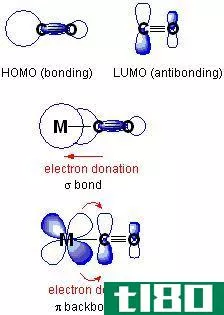
dπ-dπ键是一种共价化学键,金属通过d轨道的重叠与配体结合。换言之,这种共价化学键是在过渡金属的填充d轨道向配体的空d轨道捐赠一些电子形成配位化学键时形成的。因此,这些化合物被称为配位配合物。
图01:配位共价化合物
与类似于dπ-dπ键结构的δ键不同,dπ-dπ键发生在填充d轨道和空d轨道之间。另外,任何两个原子之间都可以形成δ键,而dπ-dπ键则发生在具有d电子构型的过渡金属和d电子壳层中具有空轨道的配体之间。
什么是三角洲债券(a delta bond)?
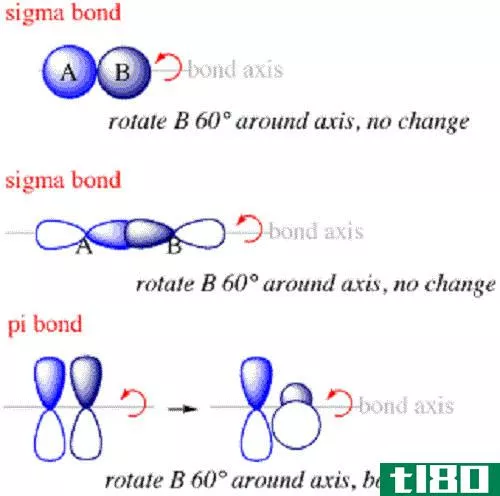
δ键是一种化学键,其中一个参与的原子轨道的四个波瓣往往与另一个参与的原子轨道的四个波瓣重叠,形成这种键。这种类型的轨道重叠导致形成一个分子轨道(键合),它由两个包含核间轴的节面组成,并穿过两个原子。三角洲符号“”的希腊字母用于表示三角洲债券。
图02:三角洲化学键的形成
一般来说,考虑键轴时,δ键的轨道对称性与通常的d原子轨道相似。在占据d原子轨道的原子中,我们可以观察到这种类型的化学键合,而d原子轨道含有低能量参与共价化学键合。例如,有机金属化学物种中的过渡金属表现出δ键;某些金属的化合物,如铼、钼和铬含有四重键。四键由一个σ键,两个π键和一个δ键组成。
当考虑δ键的轨道对称性时,我们可以观察到它与π反键轨道的对称性不同。π反键轨道包含一个由核间轴组成的节面和另一个垂直于原子间轴的节面。
科学家罗伯特·穆利肯在1931年介绍了三角洲符号。他首先用化学化合物八氯二苯甲酸钾(III)鉴定了这种键。
dπ-dπ键(dπ-dπ bond)和三角洲债券(delta bond)的区别
dπ-dπ键和δ键是两类共价化学键。dπ-dπ键与δ键的主要区别在于dπ-dπ键是在填充d原子轨道和空d原子轨道之间形成的,而δ键是在一个原子轨道的四个波瓣和另一个原子轨道的四个波瓣之间形成的。
在infographic之前,以表格形式总结了dπ-dπ键和delta键的区别。
总结 - dπdπ键(dπdπ bond) vs. 三角洲债券(delta bond)
dπ-dπ键和δ键是两类共价化学键。dπ-dπ键与δ键的主要区别在于dπ-dπ键是在填充d原子轨道和空d原子轨道之间形成的,而δ键是在一个原子轨道的四个波瓣和另一个原子轨道的四个波瓣之间形成的。