原子中成对的电子在轨道上以成对的形式出现,但未成对的电子不会以电子对或成对的形式出现。成对电子和未成对电子之间的关键区别在于,成对电子引起原子的抗磁性,而未成对电子引起原子的顺磁性或铁磁性。
电子是原子中的亚原子粒子。每个原子至少包含一个电子。在原子的中性态,电子的数目等于原子核中的质子数。但是当它有电荷时,这些数字是不相等的(这导致了电荷)。我们可以写出原子的电子构型,它给出了电子在不同能级上的排列。这种电子构型揭示了原子中成对和不成对的电子。现在让我们来讨论这两种形式是什么。
目录
1. 概述和主要区别
2. 什么是成对电子
3. 什么是未成对电子
4. 并列比较-成对电子与未配对电子的表格形式
5. 摘要
什么是成对电子(paired electr***)?
成对电子是原子中成对出现在轨道上的电子。轨道是一个电子在原子中的位置;它不是一个特定的位置,而是一个电子围绕原子核运动的区域,因为电子在原子核周围连续运动。根据现代理论,电子是以轨道存在的。一个最简单的轨道最多能容纳两个电子。当一个轨道上有两个电子时,我们说有一对电子。这些是原子中的成对电子。有些化学元素的电子全部配对,非常稳定。但有些是反应性的。稳定性取决于原子的电子构型。
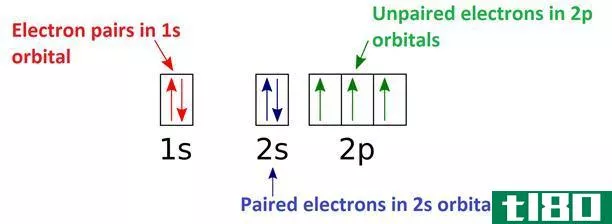
图01:氮原子轨道上的电子排列
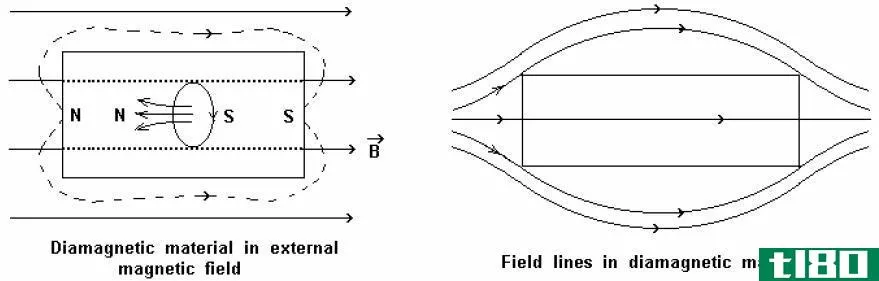
此外,如果我们考虑化学元素的磁性,可以有三种主要的磁性类型,即抗磁元素、顺磁性元素和铁磁性元素。这种磁性主要取决于未成对电子的数量。因此,成对电子对磁性没有贡献。然后我们可以把所有电子配对的化学元素命名为抗磁性化学元素;抗磁性意味着它不吸引磁场。
什么是未成对电子(unpaired electr***)?
不成对电子是原子中单独出现在轨道上的电子。这意味着这些电子不是成对的或以电子对的形式出现。我们只需写下原子的电子构型,就可以很容易地确定原子中是否存在未成对电子。拥有这些电子的原子表现出顺磁性或铁磁性。
顺磁性材料中的电子比未磁化的材料吸引的电子要高,而顺磁性材料的电子比空气中的电子要高。当一个原子或分子有这种类型的电子时,我们称之为自由基。含有这些电子的化学元素具有高度的反应性。这是因为它们倾向于把所有的电子配对以变得稳定;拥有一个不成对的电子是不稳定的。
成对的(paired)和未成对电子(unpaired electr***)的区别
成对电子是原子中成对出现在轨道上的电子,而不成对电子是原子中单独出现在轨道上的电子。因此,在轨道上,成对电子总是以一对电子的形式出现,而不成对的电子则以单个电子的形式出现。这就是成对电子和未成对电子之间的根本区别。此外,成对电子引起原子的抗磁性,而不成对的电子引起原子的顺磁性或铁磁性。我们可以说这是成对电子和未成对电子之间的关键区别。
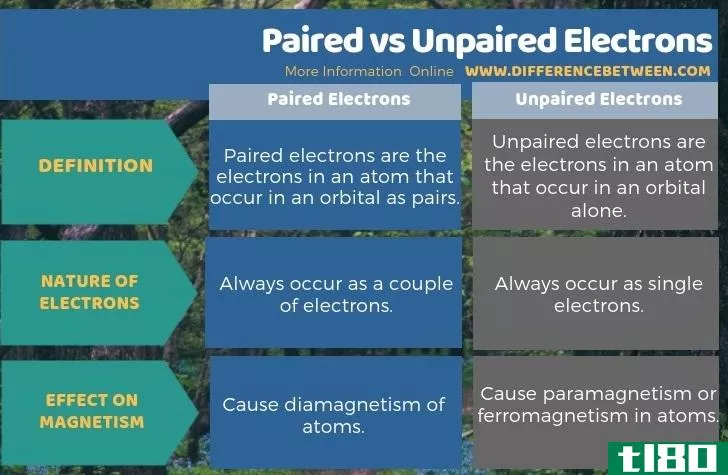
总结 - 成对的(paired) vs. 未成对电子(unpaired electr***)
电子出现在原子轨道上。它们在原子核周围****。这些电子可能以成对或不成对两种形式出现。成对电子和未成对电子的区别在于,成对电子引起原子的抗磁性,而不成对电子引起原子的顺磁性或铁磁性。