主要区别
热力学第一定律和热力学第二定律的主要区别在于,热力学第一定律讨论了能量既不能产生也不能被破坏,但它可以改变其形式,而根据热力学第二定律,系统的熵总是增加的。
热力学第一定律(first law of thermodynamics) vs. 热力学第二定律(second law of thermodynamics)
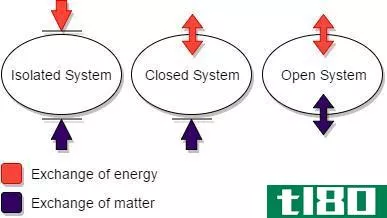
“热力学”一词是希腊语单词的派生词,其中“Thermo”代表热量,“dynamics”表示功率。因此,它是对存在于不同形式的能量的研究,如热、光、电和化学能。热力学有四种不同的定律,即第零定律、第一定律、第二定律和第三定律。但最重要的是热力学第一定律和第二定律。热力学第一定律讨论了能量既不能产生也不能被破坏,但它只能改变它的形式,而热力学第二定律则指出,系统的熵从不减少,而是总是增加。在讨论这些规律时,有两个术语是非常重要的,即制度和环境。我们所处理的任何一个项目或一组项目,无论是小的像细胞,还是大的像生态系统,都被称为系统。系统周围的一切都被称为周围环境。
比较图
什么是热力学第一定律(the first law of thermodynamics)?
热力学第一定律,也叫能量守恒定律,讨论了宇宙中的总能量。它指出,总能量保持不变。根据这个定律,能量可以改变它的形式,但它不能被创造或毁灭。
示例
- 在光合作用过程中,植物利用阳光,即太阳能,并将其转化为化学能,即葡萄糖。
- 当我们在饭后散步、呼吸或跑步等时,我们正在将食物中的化学能转化为动能。
- 变亮的电灯泡把电能转换成光能。
方程式
ΔE=q+w这是一个系统的内能变化等于流入系统的总热量和周围环境对系统做功的总和。如果其他两个量已知,它可以用来计算一个值。
什么是热力学第二定律(the second law of thermodynamics)?
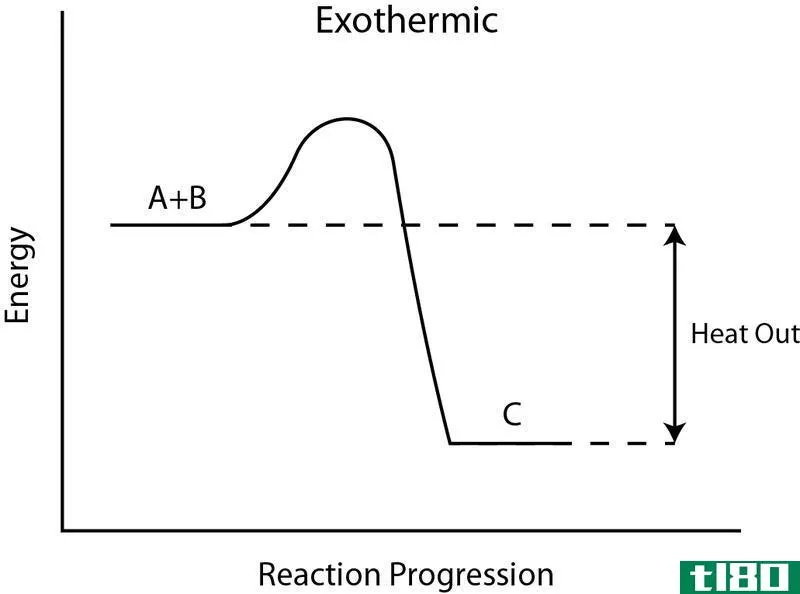
根据这个热力学定律,一个系统的熵从不减少,而是总是增加。熵是系统中随机性的无序程度。第一定律指出,能量永远不会被产生或破坏,这意味着能量可以一次又一次地循环利用。但是,根据开尔文-普朗克的说法,没有一个系统能够以100%的效率转换不同形式的能量。这意味着在一个过程中,总有一些能量以无用的形式流失。所以,系统的熵总是增加的。热力学第二定律也解释了能量转换只发生在一个特定的方向上,这在热力学第一定律中没有得到澄清。
示例
- 电灯泡可以把电能转换成光能,但反过来的过程是不可能的,即如果我们给灯泡提供相同数量的热量和光,它就会把它转变成电能。
- 房间里的取暖器使用电能为房间提供热量,而作为回报,房间不能为取暖器提供相同的能量。
方程式
ΔS=ΔS系统+ΔS箭头这是用来测量系统总熵变的方程。
主要区别
- 热力学第一定律是关于能量的,它说明能量不能被产生或破坏,只能转变成不同的形式,而热力学第二定律则是系统的熵从不减少而是总是增加的定律。
- 热力学第一定律也称为“能量守恒定律”,另一方面,热力学第二定律又称为“增加熵定律”
- ΔE=q+w是热力学第一定律的方程,如果已知另外两个量,则用来计算一个值。热力学第二定律表示,熵的总变化等于系统及其周围环境的熵变化之和
- 热力学第一定律方程表示,一个系统的内能的变化等于流入系统的总热量,并由周围环境对系统做功。另一方面,热力学第二定律表示,系统的总变化可以通过系统和周围环境的熵变化之和得到。
- 热力学第一定律的例子是光合作用,在光合作用中植物将太阳能转化为化学能,即葡萄糖,而房间里的加热器则是热力学第二定律的一个例子,它利用电能为房间提供热量,而反过来,房间不能向加热器提供相同的能量。
对比视频
结论
根据上述讨论,总结出根据热力学第一定律,能量不可能产生或破坏,只能转化为不同的形式,但它不能解释能量转换的方向,热力学第二定律阐明了系统的熵总是增加。