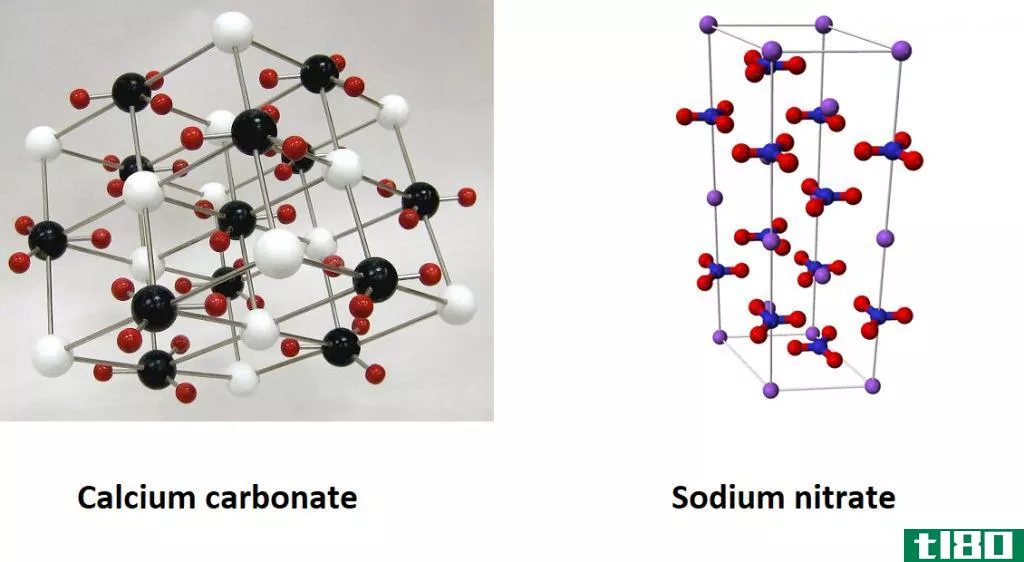
多态性与同素异形体的主要区别在于,多晶性发生在化合物中,而同素异形体则发生在化学元素中。
多态性是指同一固体物质存在几种不同形式。这意味着这类化合物可能有不止一种晶体结构。另一方面,同素异形是一个类似的化学概念,但它描述了同一化学元素的几种不同形式的存在。
目录
1. 概述和主要区别
2. 什么是多态性
3. 什么是同素异形
4. 并列比较-表格形式的多态性与同素异形体
5. 摘要
什么是多态性(polymorphi**)?
多态性是指固体材料以多种形式或晶体结构存在的能力。我们可以在任何晶体材料中发现这种特性,如聚合物、矿物、金属等。多态性有几种形式,如下所示:
- 填充多态性-取决于晶体填充的差异
- 构象多态性-同一分子存在不同的构象
- 假多态性-由于水合作用或溶剂化作用而出现的不同晶体类型。
结晶过程中条件的变化是导致结晶材料中多晶现象发生的主要原因。这些可变条件如下:
- 溶剂极性
- 杂质的存在
- 材料开始结晶的过饱和度
- 温度
- 搅拌条件的变化
什么是同素异形(allotropy)?
同素异形是指一种化学元素存在两种或两种以上不同的物理形态。这些形式存在于相同的物理状态,主要是固态。因此,这些都是同一化学元素的不同结构修饰。同素异形体含有相同化学元素的原子,它们以不同的方式相互结合。

图01:金刚石和石墨是碳的同素异形体
此外,这些不同的形式可能有不同的物理性质,因为它们有不同的结构和化学行为也可能不同。当我们改变压力、光照、温度等因素时,一种同素异形体可能会转化成另一种同素异形体,因此这些物理因素会影响这些化合物的稳定性。同素异形体的一些常见示例如下:
- 碳——金刚石、石墨、石墨烯、富勒烯等。
- 磷——白磷、红磷、二磷等。
- 氧气-氧气、臭氧、四氧等。
- 硼-无定形硼、α-菱形硼等。
- 砷——黄色砷、灰色砷等。
多态性(polymorphi**)和同素异形(allotropy)的区别
多态性是指固体材料以多种形式或晶体结构存在的能力。它只存在于化合物中。此外,还描述了化合物晶体结构的差异。同素异形是指一种化学元素存在两种或两种以上不同的物理形态。它只存在于化学元素中。除此之外,它还描述了具有相同化学元素原子的化合物在原子排列上的差异。下面的信息图以表格形式给出了多态性和同素异形之间的区别。

总结 - 多态性(polymorphi**) vs. 同素异形(allotropy)
多态性和同素异形是无机化学中的两个相关术语。多态性与同素异形的区别在于,多态性发生在化学化合物中,而同素异形发生在化学元素中。
引用
1“多态性(材料科学)。”维基百科,维基媒体基金会,2018年7月3日。这里有2个。大英百科全书的编辑。“同素异形体”,《大英百科全书》,大英百科全书,2017年4月21日。此处提供
2大英百科全书的编辑。“同素异形体”,《大英百科全书》,大英百科全书,2017年4月21日。