连锁与同素异序的关键区别在于,连锁是指一个元素对自身的吸附,形成链状或环状结构,而同素异形是指同一化学元素存在不同的物理形态。
尽管链式和同素异序表达了相同化学元素原子的不同排列方式的相似观点,但它们是描述物质不同状态的不同术语。
目录
1. 概述和主要区别
2. 什么是连锁
3. 什么是同素异形
4. 并列比较-链式和同素同素异序的表格形式
5. 摘要
什么是连锁(catenation)?
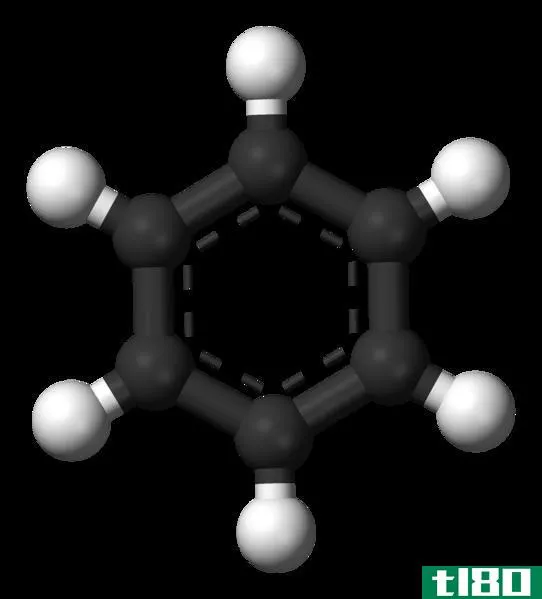
在无机化学中,链结是指某一特定化学元素的原子相互结合,形成链状或环状结构的能力。一般情况下,化学元素碳参与了链式反应,因为碳可以通过与大量碳原子结合而形成脂肪族和芳香族结构。此外,还有一些其他化学元素可以形成这些结构,如硫和磷。

图01:碳的长链结构
当某一化学元素发生链式反应时,该元素的原子价必须至少为2。此外,这种化学元素必须能够在同类原子之间形成强大的化学键,例如共价键。我们也可以把聚合称为一种链式反应。可以发生连环反应的化学元素包括碳、硫、硅、锗、氮、硒和碲。
什么是同素异形(allotropy)?
在无机化学中,同素异形是指一种化学元素存在两种或两种以上不同的物理形态。这些不同的物理形态存在于同一物理状态中,大部分是固态的。因此,我们可以说这些都是同一化学元素的不同结构修饰。此外,同素异形体含有相同化学元素的原子,它们以不同的方式相互结合。
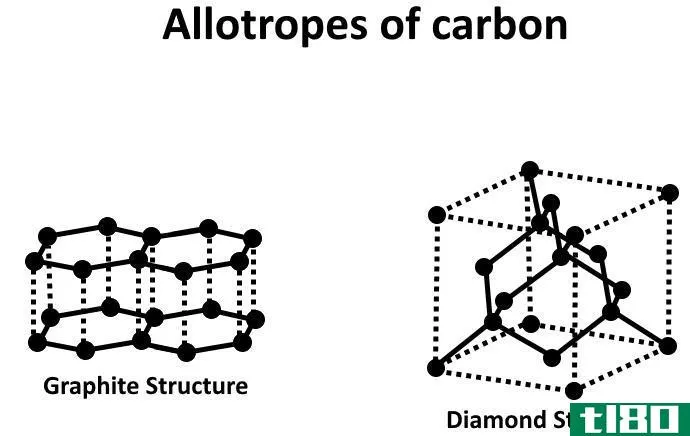
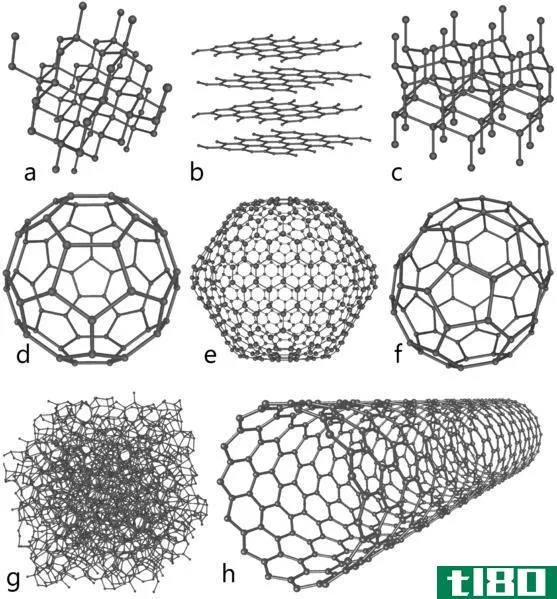
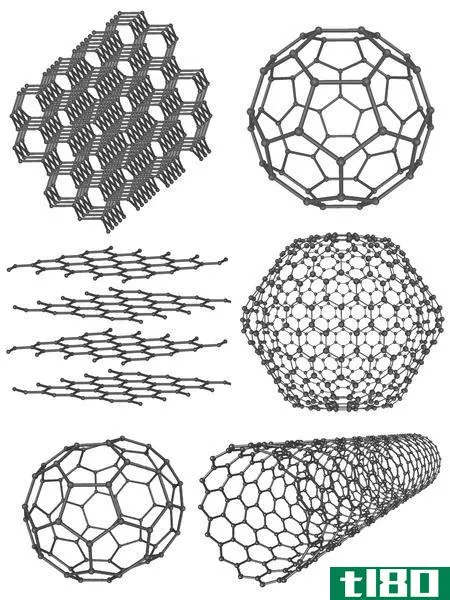
图02:碳的两个主要同素异形体
然而,这些不同的形式可能有不同的物理性质,因为它们有不同的结构和化学行为。当我们改变一些物理因素如压力、光照、温度等时,一种同素异形体能够转化成另一种同素异形体,因此这些物理因素影响了这些化合物的稳定性。同素异形体的一些例子包括:
- 碳的同素异形体——金刚石、石墨、富勒烯等。
- 磷的同素异形体——白磷、红磷等。
- 氧的同素异形体——氧、臭氧等。
- 砷的同素异形体——黄砷、灰砷等。
连锁(catenation)和同素异形(allotropy)的区别
根据原子排列的不同,连锁和同素异序是不同的。连锁是指某一特定化学元素的原子相互结合,形成链状或环状结构的能力。无机化学中的同素异形是指一种化学元素存在两种或两种以上不同的物理形态。因此,连锁与同素异形的关键区别在于,连锁是一种元素对自身的束缚,形成链状或环状结构,而同素异形则是同一化学元素存在不同的物理形态。
下表总结了连锁和同素异序的区别。
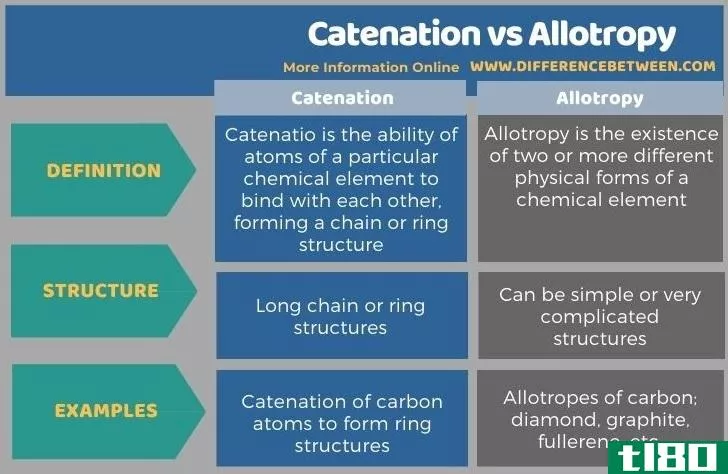
总结 - 连锁(catenation) vs. 同素异形(allotropy)
连锁和同素异形是重要的化学术语。连锁与同素异序的关键区别在于,连锁是指一个元素自身形成链状或环状结构,而同素异形是指同一化学元素存在不同的物理形态。
引用
1赫尔曼斯汀,安妮·玛丽。“连锁定义与实例”,ThoughtCo,2020年2月11日,