氮和硝酸盐的关键区别在于氮是一种元素,而硝酸盐是氮和氧的化合物。
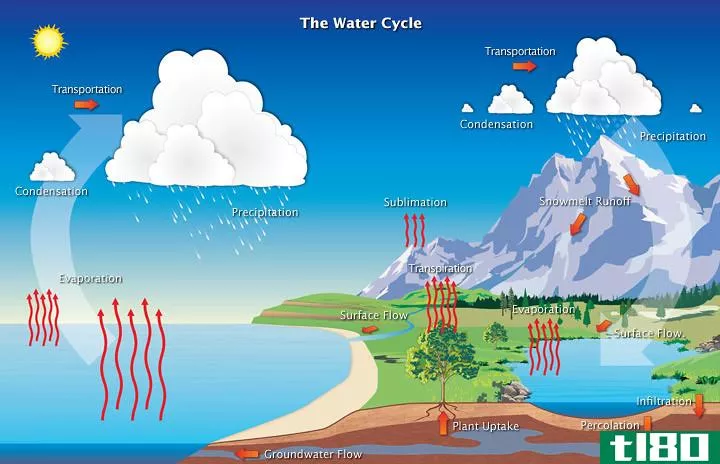
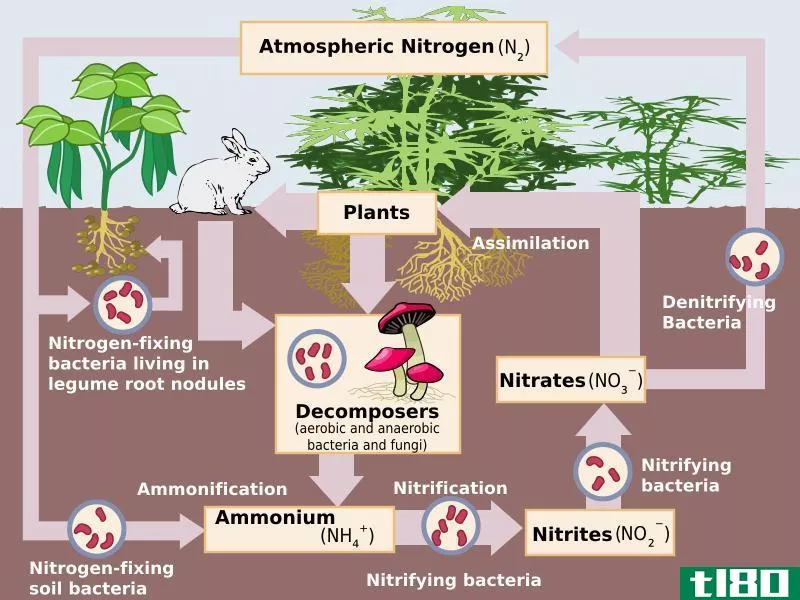
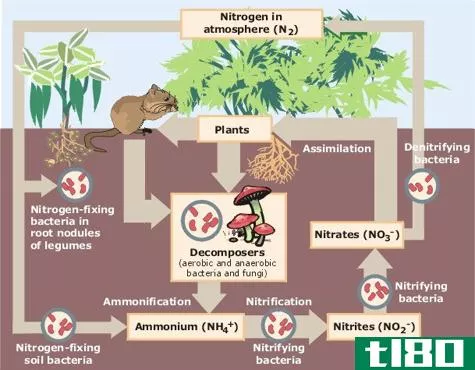
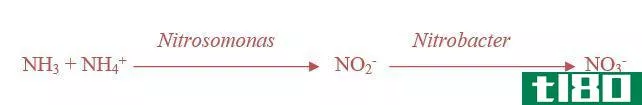
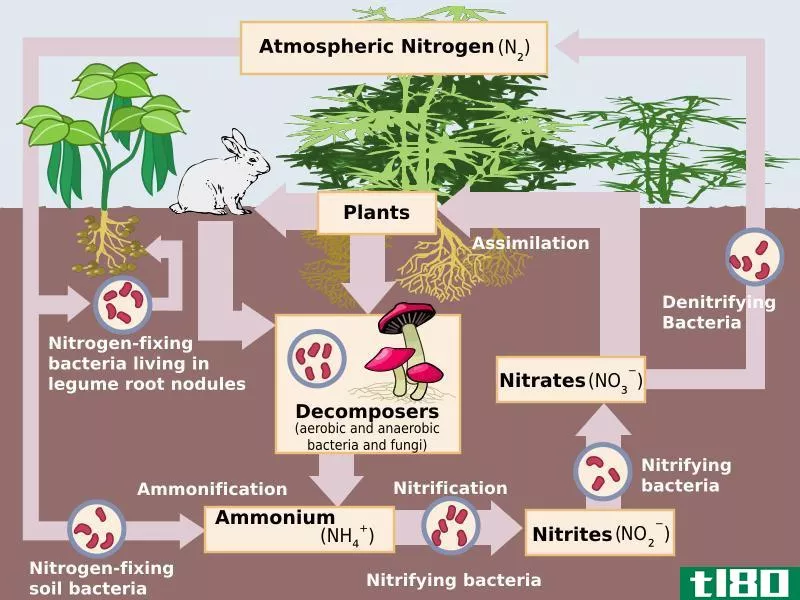
硝酸盐是一种高度有效的含氮阴离子形式。天然地,氮以气体的形式存在,是氮的主要储集层。植物不能直接使用这种气态氮,所以一些细菌倾向于将气态氮转化为水溶性的形式,如硝酸盐、亚硝酸盐或铵。大气中的氮通过工业固定、闪电作用和一些土壤微生物转化为硝酸盐。我们称之为固氮过程。土壤中的硝化细菌也能将氨和亚硝酸盐转化为硝酸盐。土壤中的硝酸盐随后被植物吸收以进行活动。此外,土壤硝酸盐可以通过反硝化硫杆菌等反硝化细菌转化回氮气。
目录
1. 概述和主要区别
2. 氮是什么
3. 硝酸盐是什么
4. 并列比较-氮与硝酸盐的表格形式
5. 摘要
什么是氮(nitrogen)?
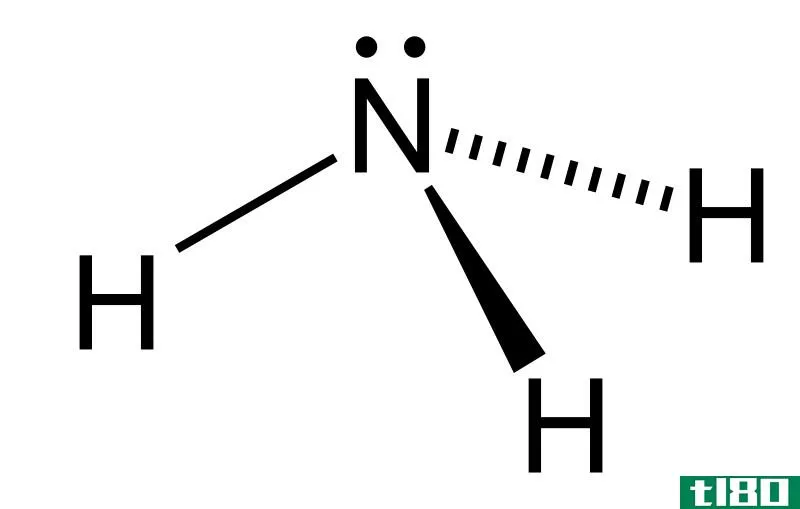
氮是我们体内第四丰富的元素。它在周期表的第15组,原子序数为7。氮是一种非金属,它的电子构型是1s2 2s2 2p3。p轨道是半满的,这使氮有能力再吸收三个电子,以获得稳定的稀有气体结构。因此,氮是三价的。
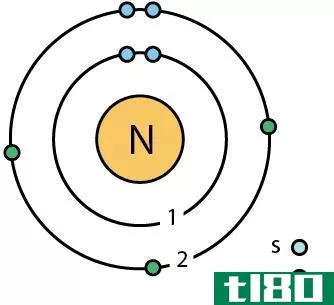
图01:氮原子
两个氮原子可以在它们之间形成三键,每个原子共享三个电子。这种双原子分子在室温下处于气相,形成无色、无味、无味的惰性气体。氮气是一种不可燃气体,不支持燃烧。这是地球大气中最丰富的气体(约78%)。
当然,氮有两种同位素,N-14和N-15。N-14更丰富。在很低的温度下,氮气变成液态。它的外观与水相似,但密度低于水。
氮在化学工业中有广泛的用途,是生物体所需的重要成分。氮最重要的商业用途是用作氨、硝酸、尿素和其他含氮化合物的原料。由于氮是植物生长所需的主要元素之一,这些化合物可能被纳入肥料中。氮在我们需要惰性环境的地方也很重要,特别是在进行化学反应时。此外,液态氮对于立即冻结物体以及在各种设备(如计算机)中作为冷却剂也很重要。
什么是硝酸盐(nitrate)?
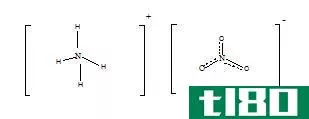
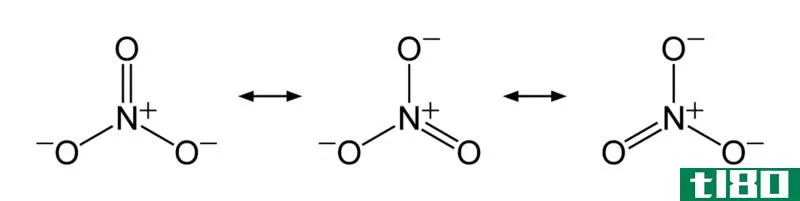
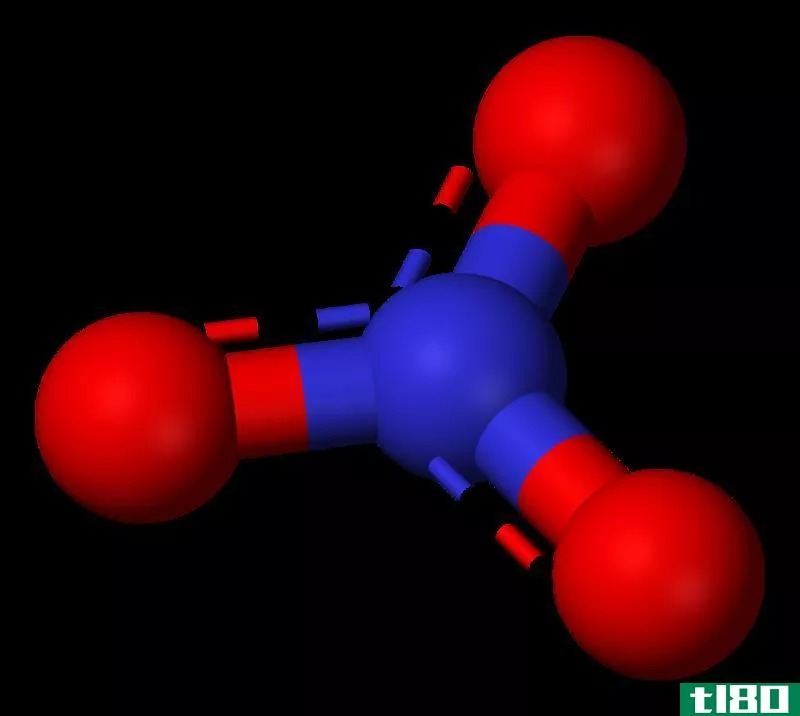
硝酸盐是一种含有氮和三个氧原子的多原子阴离子。氮原子处于+5氧化状态。这个分子的几何结构是三角平面的,它也显示出共振。这种单价阴离子可以与任何其他类型的阳离子结合形成各种有机和无机化合物。
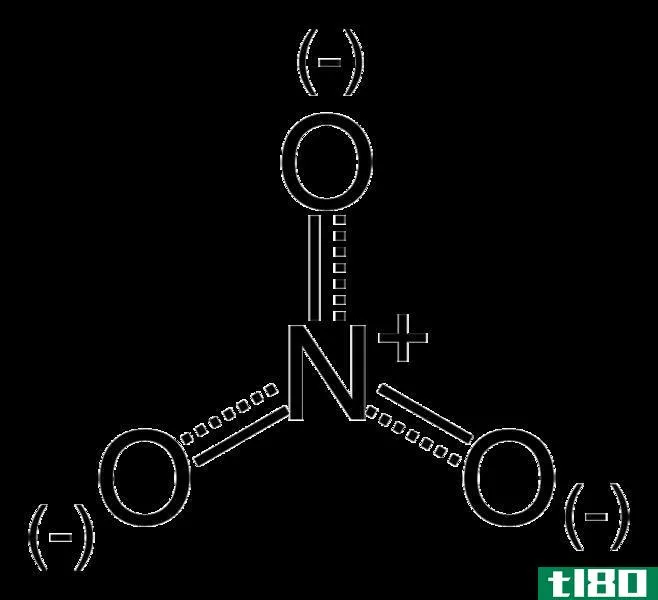
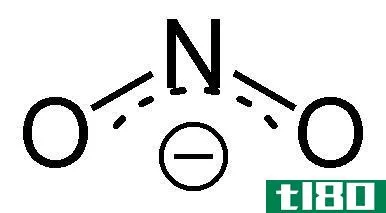
图02:硝酸根阴离子的共振稳定结构
含硝酸盐的化合物通常是水溶性的,在土壤、水和食物中含量丰富。硝酸盐在**肥料中最重要。它们对****也很重要。硝酸盐相对无毒。在我们体内,硝酸盐会转化为亚硝酸盐,因此,它会变得有毒。
氮(nitrogen)和硝酸盐(nitrate)的区别
虽然“氮”和“硝酸盐”这两个词听起来很相似,但它们却是截然不同的。氮和硝酸盐的关键区别在于氮是一种元素,而硝酸盐是氮和氧的化合物。换言之,氮是原子序数为7,符号为N的化学元素,而硝酸盐是化学式为NO3的阴离子。此外,氮原子是三价的,而硝酸根阴离子是一价的。考虑电荷时,自由氮原子为中性,而硝酸根阴离子为-1电荷。此外,自由氮原子的氧化态为零,而在硝酸根阴离子中为+5。

总结 - 氮(nitrogen) vs. 硝酸盐(nitrate)
氮是原子序数为7,符号为N的化学元素,而硝酸盐是化学式为NO3-的阴离子。氮和硝酸盐的关键区别在于氮是一种元素,而硝酸盐是氮和氧的化合物。
引用
1Powlson,D.s.和T.m.Addiscott。“土壤中的氮|硝酸盐”,《环境中的土壤百科全书》,2005年,第21-31页。,doi:10.1016/b0-12-348530-4/00905-x。