弱酸和强酸的关键区别在于弱酸在水中部分电离,而强酸则完全电离。
酸的强度是它在水溶液中与水发生反应时电离或提供氢离子的能力。酸离子化得越多,它就越强,氢离子的生成越少,说明酸是弱酸。这就是强酸和弱酸的区别。酸的水溶液中离子的浓度决定了酸的强弱。所以,你可以得到弱酸的浓溶液,而强酸的稀溶液是完全可能的。
目录
1. 概述和主要区别
2. 什么是弱酸
3. 什么是强酸
4. 并列比较-弱酸与强酸的表格形式
5. 摘要
什么是弱酸(weak acid)?
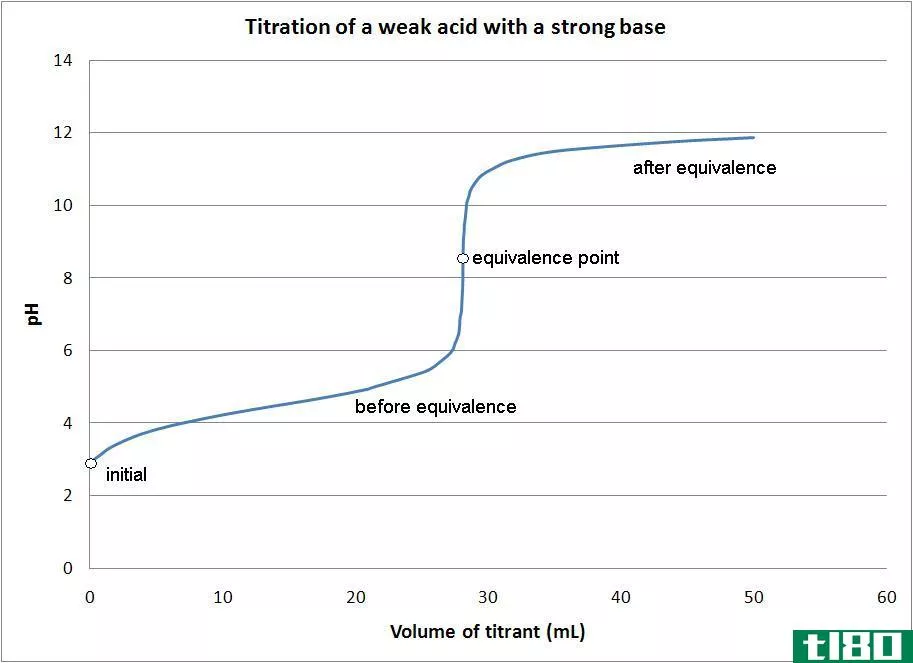
弱酸是指在水溶液中部分分解成离子的化合物。它们不会将可释放氢离子(H+)的总量释放到溶液中。对于这些酸,酸离解常数Ka是一个小值。这些溶液的pH值在3到5之间。这主要是因为这些弱酸不能像强酸那样提高溶液中的氢离子含量。
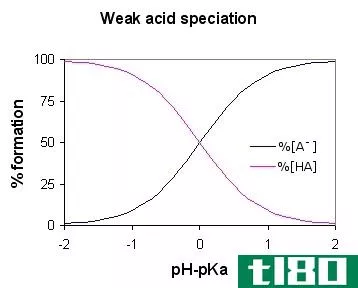
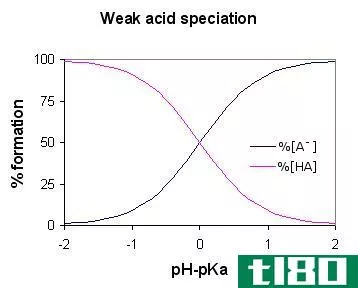
图01:弱酸形态图(弱酸HA)
由于弱酸部分解离,水溶液中含有三种主要成分:氢离子、结合酸分子和共轭碱(与酸分子中的氢离子结合的阴离子)。一些常见的例子包括亚硫酸、磷酸、亚硝酸等。
什么是强酸(strong acid)?
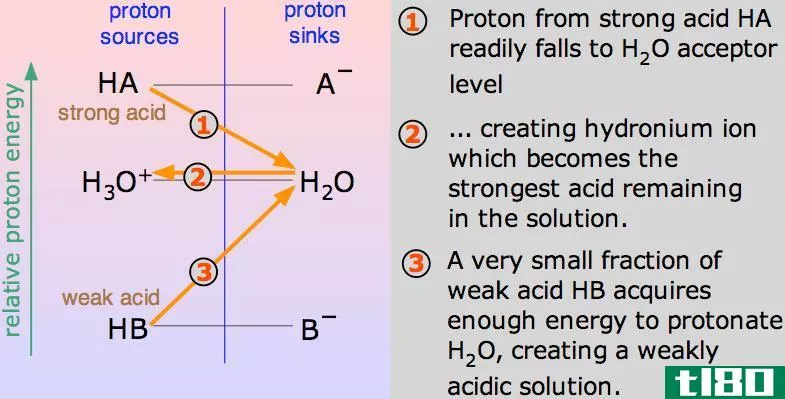
强酸是指在水溶液中完全分解成离子的分子。因此,这些化合物在水中完全电离。对于这类酸,酸离解常数(Ka)值较高。酸越强,氢离子越容易释放。这主要是由于H-A键的极性很高,其中H是氢原子,A是共轭基。为了获得高极性,这种键两边原子之间的电负性差应该很高。
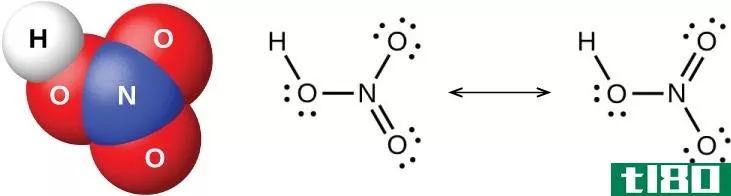
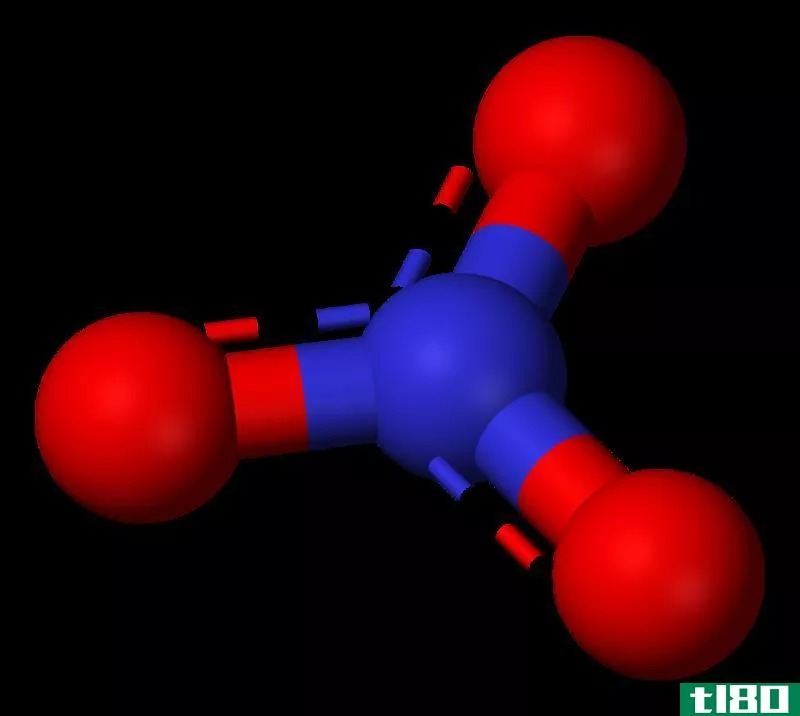
图02:强酸硝酸(硝酸)的化学结构
此外,氢离子的释放还取决于与氢离子相连的阴离子(共轭碱)的大小。如果阴离子较大且较稳定,则很容易释放氢离子。与弱酸不同,这些强酸会将所有可能的氢离子释放到水溶液中。这些水溶液的pH值很小,范围在1到3之间。
虚弱的(weak)和强酸(strong acid)的区别
弱酸在水中部分电离,而强酸则完全电离。因此,电离是弱酸和强酸的关键区别。此外,弱酸和强酸之间的另一个区别是弱酸不能去除所有可释放的氢原子。相反,强酸会释放所有可能的氢原子。
此外,弱酸和强酸在pH值上也存在差异。也就是说,弱酸的pH值在3到5之间,而强酸的pH值在1到3之间。强酸和另一种酸之间的持续离解也有助于强酸和强酸之间的差异。弱酸的酸离解常数比强酸小。

总结 - 虚弱的(weak) vs. 强酸(strong acid)
酸是能将氢离子释放到水溶液中的分子。我们可以把所有的酸分为强酸、中等强酸和弱酸。简而言之,弱酸和强酸的关键区别在于弱酸在水中部分电离,而强酸则完全电离。
引用
1Helmenstine,Anne Marie博士,“强酸和弱酸列表”,ThoughtCo,2018年9月24日。这里有2个。Helmenstine,Anne-Marie博士,《化学中弱酸的定义和示例》,ThoughtCo,2018年6月18日。此处提供
2Helmenstine,Anne-Marie博士,《化学中弱酸的定义和示例》,ThoughtCo,2018年6月18日。