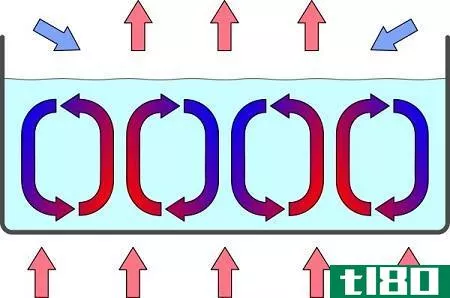
功和热的关键区别在于功是一个方向上的有序运动,而热是分子的随机运动。
功和热是热力学中最重要的两个概念。功和热是高度相关的,但它们并不完全相同。对功和热的理解可以追溯到很久以前。随着这两个概念的澄清,经典热力学成为物理学中“完整”的领域之一。热和功都是能量的概念。热和功理论在热力学、电机力学和机械中有着巨大的意义。
目录
1. 概述和主要区别
2. 什么是工作
3. 什么是热
4. 并列比较-工作与热量的表格形式
5. 摘要
什么是工作(work)?
在物理学中,我们把功定义为一个力通过一段距离所传递的能量。功是一个标量,这意味着只有一个量值可以做功,没有方向。考虑一个我们在粗糙表面上拖动的物体。物体上有摩擦力。对于给定的点A和B,它们之间存在着无限多条路径,因此从A到B有无限多条路径。如果物体在某条路径上移动的距离为,s,则长方体上摩擦力所做的功为F.s(仅考虑标量值)。不同的路径有不同的x值。因此,所做的工作是不同的。
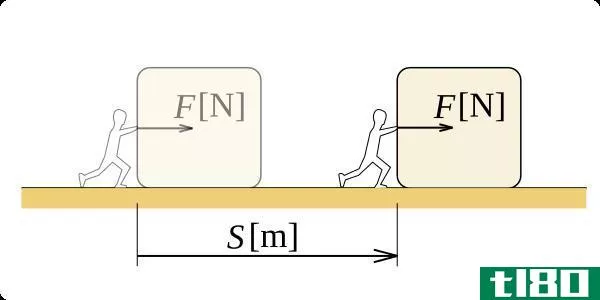
图01:用“F”力移动物体“s”距离时所做的功
我们可以证明功取决于所走的路径,也就是说功是路径的函数。对于保守力场,我们可以把所做的功看作是状态的函数。国际单位制单位是焦耳,以纪念英国物理学家詹姆斯·焦耳命名。CGS的工作单位是erg。在热力学中,当我们说功时,我们通常指的是压力功,因为内部或外部的压力是做功的力发生器。在恒定压力的情况下,所做的功是P。ΔV,其中P是压力,ΔV是体积变化。
什么是热(heat)?
热是能量的一种形式。我们可以用焦耳来测量。热力学第一定律是关于能量守恒的。它指出,供给系统的热量等于该系统的内能增量加上系统对周围环境所做的功。因此,这表明我们可以将热转化为功,反之亦然。

图02:火产生热能
此外,我们可以把热定义为分子或原子随机运动所储存的能量。系统中的热量只取决于系统所处的状态;因此,热量是状态的函数。
工作(work)和热(heat)的区别
功是一个力通过一段距离所传递的能量,而热是能量的一种形式。功和热的关键区别在于功是一个方向上的有序运动,而热是分子的随机运动。此外,功是路径的函数,而热是状态的函数。
作为功和热的另一个重要区别,我们可以证明功可以完全转化为热,但热不能100%地转化为功。此外,热是能量的一种形式,而功是一种传递能量的方法。下面的关于工作和热的区别的信息图给出了一个更详细的比较。
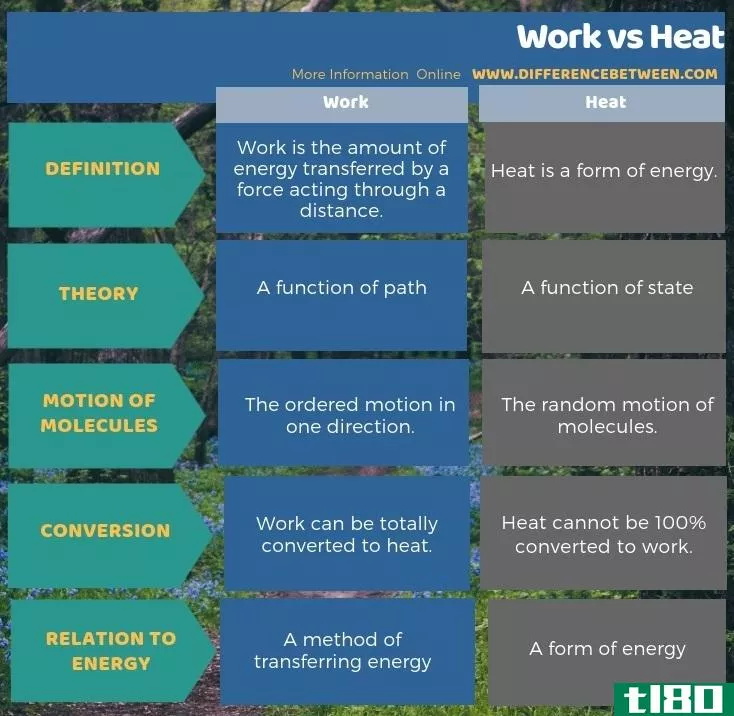
总结 - 工作(work) vs. 热(heat)
功和热是我们在物理和化学中使用的概念。功和热是相互关联的,但它们之间也有一些区别。功和热的关键区别在于功是一个方向上的有序运动,而热是分子的随机运动。
引用
1OpenStaxCollege。“大学物理”,《社会学导论》——加拿大第1版,BCcampus,2012年1月23日。可在此处获取2。琼斯,安德鲁·齐默尔曼。“定义热能的科学方法”,ThoughtCo,2018年10月11日。此处提供
2琼斯,安德鲁·齐默尔曼。“定义热能的科学方法”,ThoughtCo,2018年10月11日。