热力学与动力学
热力学和动力学都是源于物理科学的科学原理,在科学领域带来了许多进步,其应用已渗透到科学和工程的许多领域。在化学科学中,这两个术语实际上是密切相关的。
更多关于热力学的知识
“热力学”这个名字本身就暗示了这个术语的含义,它可以被称为与温度有关的“热”和与变化有关的“动力学”。因此,更宽松地说,它可以被认为是由于温度而发生的变化。这些变化可能是物理和/或化学性质的。化学上发生的变化被称为“化学反应”,这就产生了化学热力学。
在更一般的参考文献中,热力学可以描述为与物体/状态和过程相关的原理。通常所涉及的过程是能量转移,它可以分为两个不同的组,即热和功。如果一种能量状态变为另一种,我们说功就完成了。能量基本上就是做功的能力。如果一个系统的能量因温差而改变,我们称之为有热流。
因此,热力学主要与能量学有关,对这些变化的发生率没有任何解释。在化学科学领域,状态/物体和过程所涉及的速率和能量学的区别是非常明显的,在化学科学领域,热力学只关心化学反应的能量学和平衡位置。
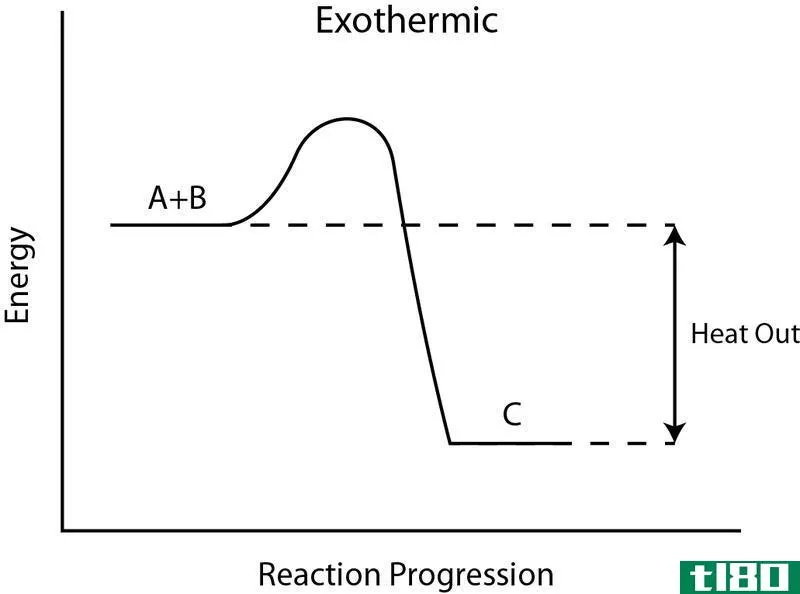
平衡的位置是反应物和产物都存在,所有物种的浓度都不会随时间而变化,当反应在标准条件下进行时,它对特定的反应是特定的。热力学可以预测一个反应肯定会发生,因为产物的能量小于反应物的能量。然而,在实践中,人们可能需要动力学原理,使反应发生在一个可观的速度。
更多关于动力学
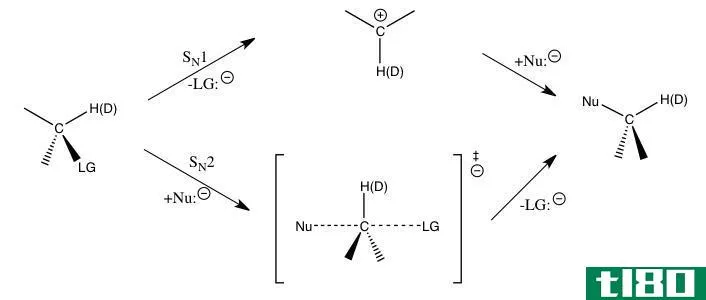
动力学在化学科学领域中经常涉及。因此,它与化学反应发生的速度或达到化学平衡点的速度有关。各种参数与控制化学反应速率有关。
所涉及的分子必须以足够的能量以正确的方向碰撞。任何满足这一要求的条件都会增加化学反应的速率。发生任何化学反应都有一个能垒。这就是所谓的活化能。分子的能量应该大于这个能量,才能发生反应。提高温度,向更高比例的分子提供大于活化能的能量,从而提高反应速率。增加表面积允许更多的碰撞,增加浓度可以增加反应分子的数量,从而提高反应速率。催化剂用于降低活化能垒,从而为反应的发生提供一条简单的路线。
- 热力学只关心从一种状态到另一种状态时的能量学和平衡位置;而动力学则与状态间过程的速率有关。
- 在化学科学中,热力学告诉我们反应发生的距离,而动力学告诉我们反应发生的速度。