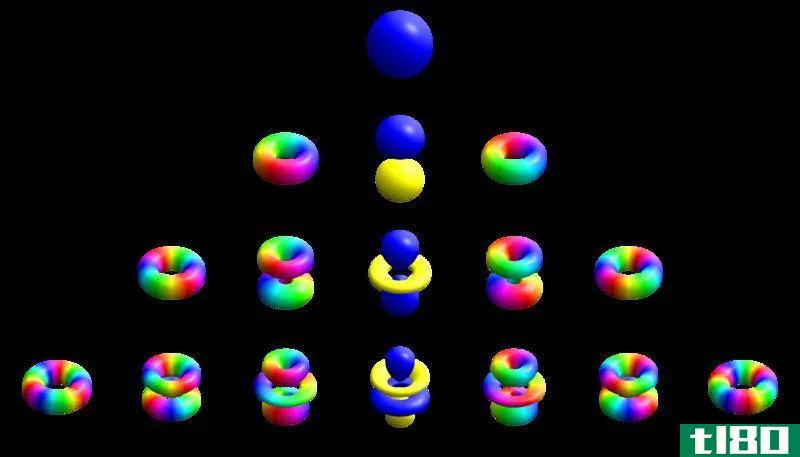量子数定义
量子数是描述原子和分子可用能级时使用的值。原子或离子中的电子有四个量子数来描述其状态,并产生氢原子薛定谔波方程的解。


有四个量子数:
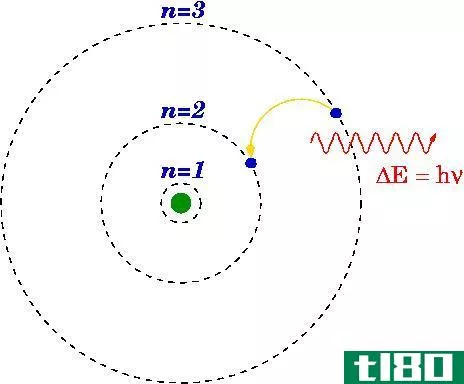
- n-主量子数:描述能级
- ℓ - 方位角或角动量量子数:描述子壳层
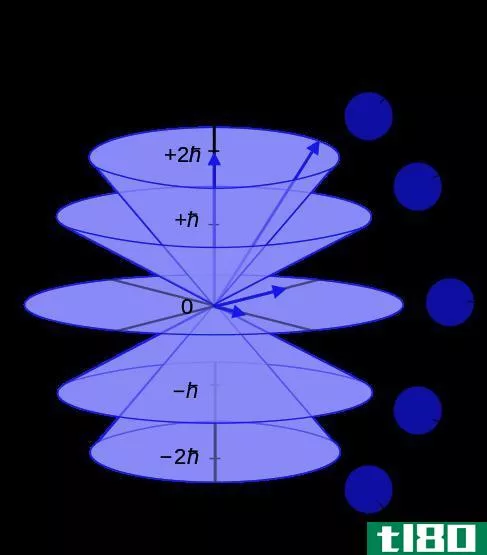
- Mℓ磁量子数:描述子壳层的轨道
- ms或s自旋量子数:描述自旋
量子数值
根据泡利不相容原理,原子中的两个电子不可能有相同的量子数。每个量子数由半整数或整数值表示。
- 主量子数是一个整数,即电子壳层的数目。该值为1或更高(从不为0或负)。
- 角动量量子数是一个整数,是电子轨道的值(例如,s=0,p=1)ℓ 大于或等于零且小于或等于n-1。
- 磁量子数是轨道的方向,其整数值范围为-ℓ 到ℓ. 对于p轨道,在哪里ℓ=1,m的值可以是-1,0,1。
- 自旋量子数是一个半整数值,它是-1/2(称为“自旋下降”)或1/2(称为“自旋上升”)。
量子数示例
对于碳原子的外层价电子,电子位于2p轨道。用来描述电子的四个量子数是n=2,ℓ=1,m=1,0或-1,s=1/2(电子具有平行自旋)。
不仅仅是电子
虽然量子数通常用来描述电子,但也可以用来描述原子或基本粒子的核子(质子和中子)。
- 发表于 2021-10-14 07:34
- 阅读 ( 149 )
- 分类:数学
你可能感兴趣的文章
方位角(azimuthal)和主量子数(principal quantum number)的区别
方位角量子数和主量子数的关键区别在于,方位角量子数描述的是原子中电子的角动量,而主量子数描述的是电子轨道的大小。 量子数是描述原子能级的重要数值。我们可以用四个量子数来描述电子在原子中的位置。它们是...
- 发布于 2020-10-07 18:13
- 阅读 ( 694 )
磁量子数(magnetic quantum number)和自旋量子数(spin quantum number)的区别
磁性量子数和自旋量子数的关键区别在于,磁量子数在区分子壳层内可用的轨道时很有用,而自旋量子数则描述了轨道的能量、形状和方向。 量子数是描述原子中电子的唯一量子态的一组值。具体的量子数有四种:主量子数...
- 发布于 2020-10-15 03:08
- 阅读 ( 1303 )
玻尔(bohr)和量子模型(quantum model)的区别
玻尔(bohr)和量子模型(quantum model)的区别 玻尔模型和量子模型是解释原子结构的模型。玻尔模型又称卢瑟福玻尔模型,因为它是对卢瑟福模型的修正。玻尔模型是尼尔斯·玻尔在1915年提出的。量子模型是原子的现代模型。玻尔...
- 发布于 2020-10-25 03:52
- 阅读 ( 581 )
壳次壳(shell subshell)和轨道(orbital)的区别
...。壳层-子壳层和轨道的主要区别在于壳层由共享相同主量子数的电子组成,子壳层由共享相同角动量量子数的电子组成,而轨道由处于相同能级但自旋不同的电子组成。 覆盖的关键领域 1.什么是壳-定义、结构和属性2.什么是子...
- 发布于 2021-06-29 12:03
- 阅读 ( 1256 )
s轨道(s orbital)和p轨道(p orbital)的区别
...因此而得名。由于原子轨道是由一个确定的能级(能量是量子化的)组成的,所以它们被赋予一个量子数。S轨道指定原子的角动量量子数。 Figure 1: The size of the s orbital increases with the increasing of principle quantum number s轨道上的两个...
- 发布于 2021-06-29 12:41
- 阅读 ( 814 )
玻尔(bohr)和量子模型(quantum model)的区别
玻尔的主要区别(main difference bohr) vs. 量子模型(quantum model) 许多科学家提出了不同的模型来解释原子的结构。玻尔模型和量子模型就是这样两种模型。玻尔模型是一种先进的模型,但它不能解释大原子线谱中观察到的塞曼效应和...
- 发布于 2021-06-29 18:32
- 阅读 ( 483 )
径向的(radial)和角节点(angular nodes)的区别
...电子壳层。这些电子壳层是由子壳层组成的。根据角动量量子数,子壳层包含一个或多个轨道:s轨道、p轨道、d轨道和f轨道。这些轨道可以在不同的平面上。一个特定平面上的每个轨道称为波瓣。在这些波瓣中发现了电子。但...
- 发布于 2021-06-29 21:27
- 阅读 ( 1516 )
有机化学术语汇编
...酰胺 胺 氨基酸 无定形 两性氧化物 阿穆 角动量量子数 负离子 无水的 阳极 反键轨道 反马尔可夫加成 反叠 水的 水溶液 芳香化合物 阿伦尼乌斯酸 阿累尼乌斯盐基 芳基 原子 原子质量 原子质量单...
- 发布于 2021-09-06 22:04
- 阅读 ( 207 )
量子数与电子轨道
...电子的能量、角动量和磁矩。原子电子构型的性质由四个量子数描述:n,ℓ, m、 和s。 第一量子数 第一个是能级量子数,n。在轨道中,较低能量的轨道靠近吸引源。你在轨道上给一个物体的能量越多,它走得越远。如果你...
- 发布于 2021-09-15 15:00
- 阅读 ( 207 )
角动量量子数定义
角动量量子数,ℓ, 是与原子电子的角动量有关的量子数。角动量量子数决定了电子轨道的形状。 也称为:方位量子数,第二量子数 例如:p轨道与等于1的角动量量子数相关联。 历史 角动量量子数来自Arnold Sommerfeld提出...
- 发布于 2021-09-15 16:44
- 阅读 ( 602 )