1.0摩尔溶液和1摩尔溶液之间的关键区别在于1.0摩尔的溶液中溶解了1摩尔的溶质,而1摩尔的溶液中溶解了1摩尔的溶质。
很久以前,阿伏伽德罗就假设有一个特定的数,代表一摩尔物质中原子或分子的数量。因此,每种元素的一摩尔含有相等数量的原子,而与该元素的原子量无关。因此,摩尔浓度和摩尔浓度的概念也被发展用来描述溶液中溶质的浓度。摩尔浓度是一升溶液中溶质摩尔数的量度,摩尔浓度是1kg溶液中的摩尔数。因此,很容易找出1.0摩尔溶液和1摩尔溶液之间的差异。
目录
1. 概述和主要区别
2. 什么是1.0摩尔溶液
3. 什么是1摩尔溶液
4. 并列比较-1.0摩尔溶液与1摩尔溶液的表格形式
5. 摘要
什么是1.0摩尔溶液(a 1.0 molar solution)?
1.0摩尔溶液是一种含有一摩尔溶质溶解在一升溶液中的溶液。此外,这是一个浓度项,我们称之为溶液的“摩尔浓度”。
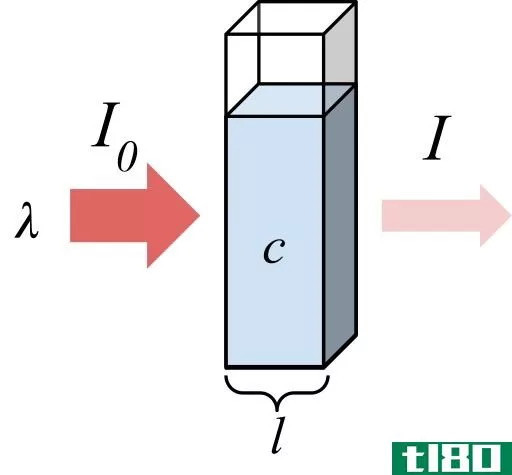
图01:不同的溶液有不同的摩尔浓度和摩尔浓度
这个术语的符号是“M”。测量单位为mol/L。例如,1.0摩尔NaCl水溶液(氯化钠)是指含有1摩尔NaCl的氯化钠溶液溶解在一升水中。
什么是1摩尔溶液(a 1 molal solution)?
1摩尔浓度的溶液是一种含有一摩尔溶质溶解在一公斤溶液中的溶液。因此,测量单位为mol/kg。
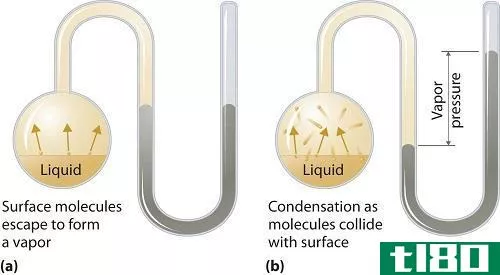
图02:1摩尔氯化钠水溶液在一公斤水中含有一摩尔氯化钠。
此外,这也是一个浓度项,我们称之为溶液的“摩尔浓度”。我们可以用“m”来表示。例如,1摩尔氯化钠溶液是指含有一摩尔氯化钠的氯化钠水溶液,溶解在一千克水中。
1.0摩尔溶液(a 1.0 molar solution)和1摩尔溶液(a 1 molal solution)的区别
1.0摩尔溶液是一种含有一摩尔溶质溶解在一升溶液中的溶液,而1摩尔浓度的溶液是含有一摩尔溶质溶解在一公斤溶液中的溶液。因此,这是1.0摩尔和1摩尔浓度溶液之间的关键区别。此外,1.0摩尔溶液的计量单位为mol/L,1摩尔溶液的计量单位为mol/kg。然而,如果水是溶剂,1.0摩尔的溶液和1摩尔的溶液之间的差别不大。这是因为,在室温下,水的密度取为1 kg/L。因此,这导致溶液的摩尔浓度和摩尔浓度相等。
总结 - 1.0摩尔溶液(a 1.0 molar solution) vs. 1摩尔溶液(a 1 molal solution)
摩尔浓度和摩尔浓度是化学中非常重要的术语,我们用来测量溶液的浓度。1.0摩尔溶液和1摩尔溶液的关键区别在于,1.0摩尔溶液中溶解有1摩尔溶质。而1摩尔浓度的溶液在一公斤溶液中溶解了一摩尔的溶质。
引用
1“摩尔浓度”,维基百科,维基媒体基金会,2018年10月17日。这里有2个。莫特,瓦莱丽。“化学导论”。流明。可在这里买到
2莫特,瓦莱丽。《化学导论》,Lumen