α螺旋(alpha helix)和贝塔褶皱床单(beta pleated sheet)的区别
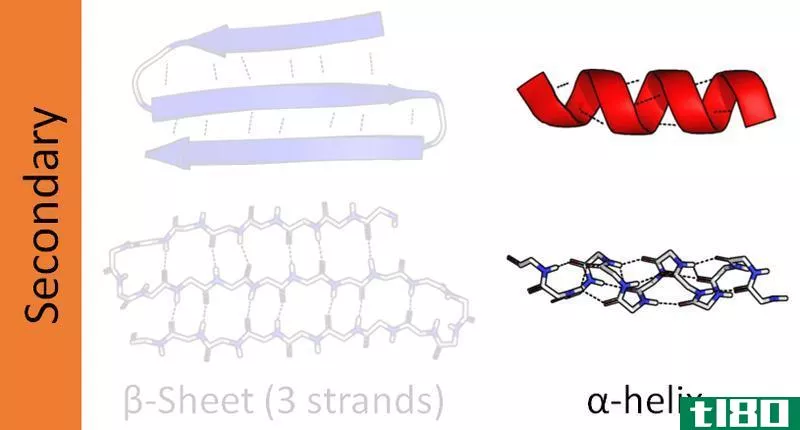
α螺旋和β折叠片是多肽链中最常见的两种二级结构。这两个结构成分是折叠多肽链过程中的第一个主要步骤。Alpha螺旋和Beta褶皱片的主要区别在于它们的结构;它们有两种不同的形状来完成特定的工作。
什么是α螺旋(alpha helix)?
α螺旋是多肽链上氨基酸残基的右旋螺旋。氨基酸残基的范围从4到40个不等。在顶部线圈的C=O基团的氧和底部线圈的N-H基团的氢之间形成的氢键有助于将线圈固定在一起。以上述方式,链中每四个氨基酸残基就形成一个氢键。这种均匀的图案赋予了它明确的特征,如线圈的厚度,并规定了沿螺旋轴的每一整圈的长度。α-螺旋结构的稳定性取决于几个因素。
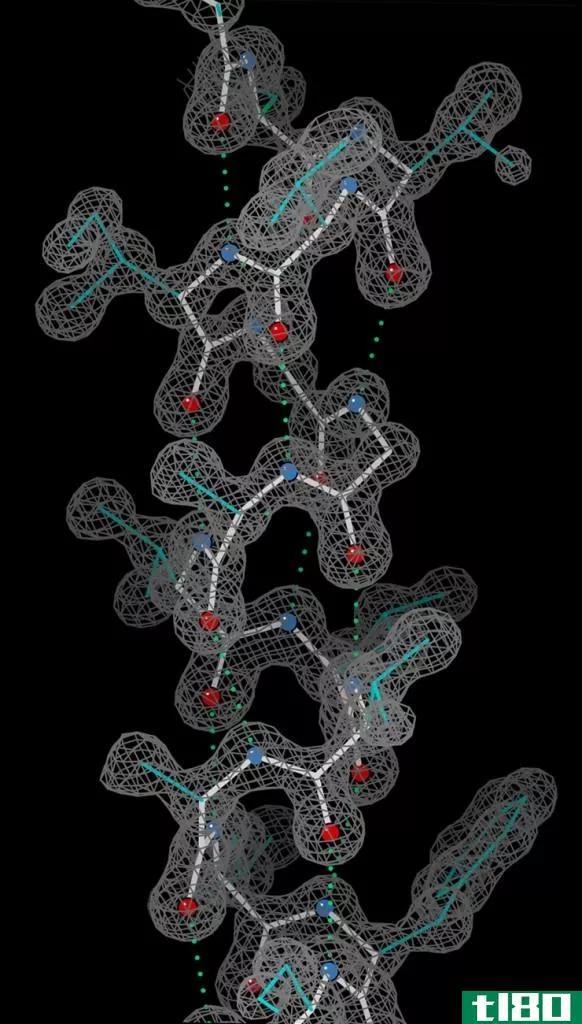
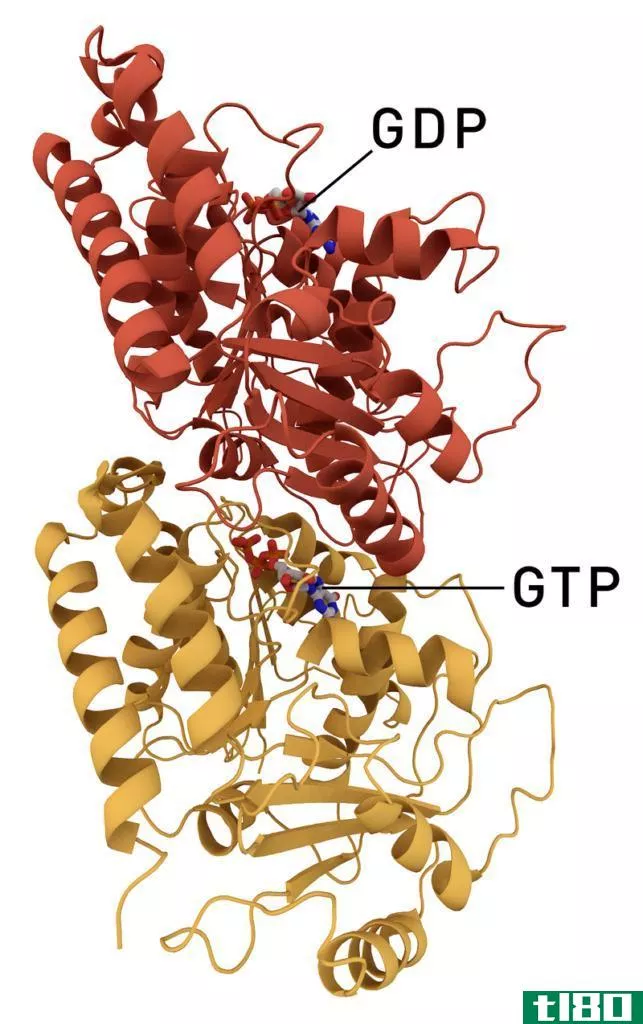
红色为O原子,蓝色为N原子,绿色虚线为氢键
什么是贝塔褶皱床单(beta pleated sheet)?
β折叠片,又称β折叠片,是蛋白质二级结构的第二种形式。它包含β链,这些链通过至少两个或三个主链氢键横向连接,形成扭曲的褶皱薄片,如图所示。β链是多肽链的延伸,它的长度一般等于3到10个氨基酸,包括延伸确认的主链。
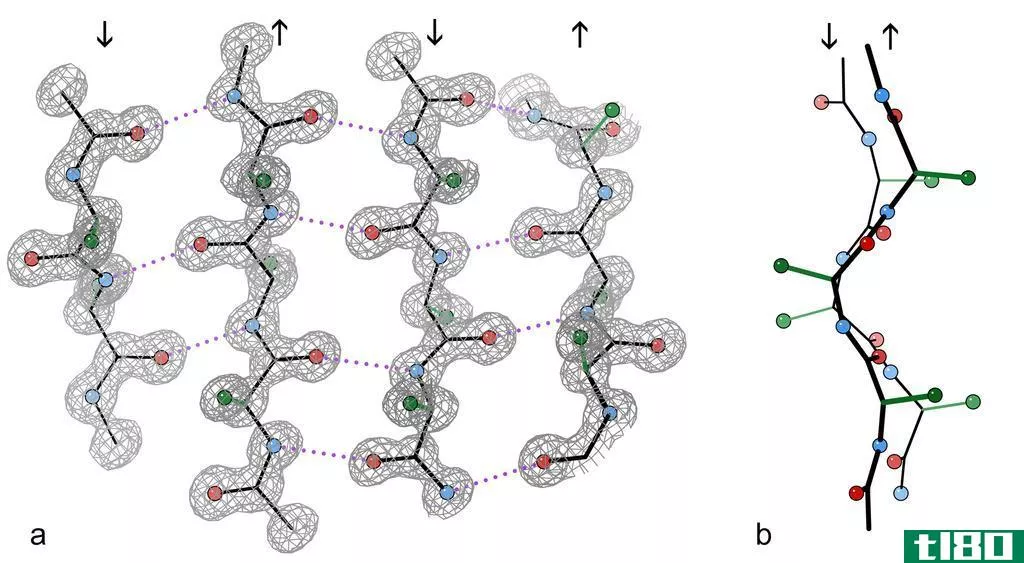
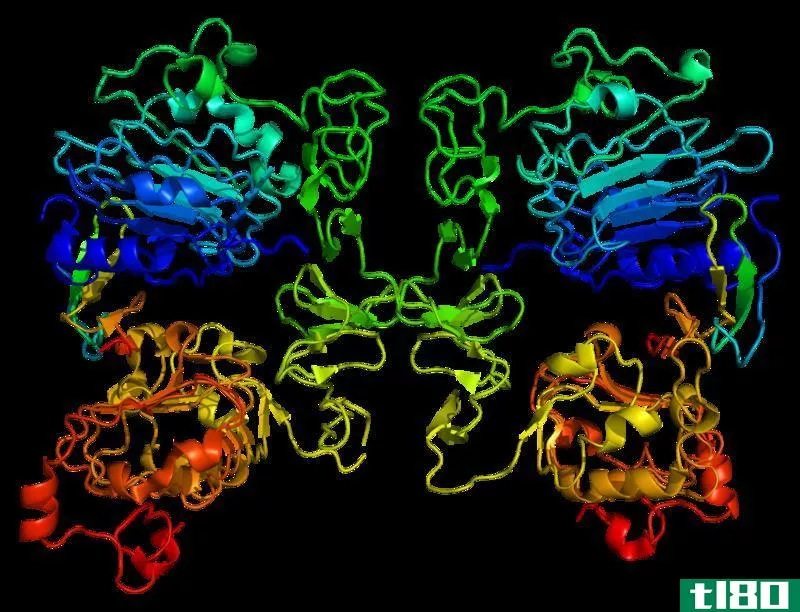
过氧化氢酶晶体结构中的4链反平行β片片段。a)显示相邻链上肽NH和CO基团之间的反平行氢键(点)。箭头表示链方向,电子密度轮廓勾勒出非氢原子。O原子是红色的球,N原子是蓝色的,为了简单起见省略了H原子;侧链只显示在中央两条β链的第一个侧链C原子(绿色)b)边上
在β-折叠片中,多肽链彼此并排排列。由于结构的波浪状外观而得名“褶皱片”。它们通过氢键连接在一起。这种结构允许通过伸展多肽链形成更多的氢键。
α螺旋(alpha helix)和贝塔褶皱床单(beta pleated sheet)的区别
α-螺旋结构和β-折叠片
α螺旋:
在这个结构中,多肽主链紧紧地围绕着一个假想的轴,形成一个螺旋结构。它也被称为螺旋链排列。
当多肽链被扭曲成螺旋状时,α-螺旋结构的形成就发生了。这使得链中的所有氨基酸相互之间形成氢键(氧分子和氢分子之间的键)。氢键使螺旋保持螺旋形状,形成紧密的线圈。这种螺旋形状使α螺旋非常强。
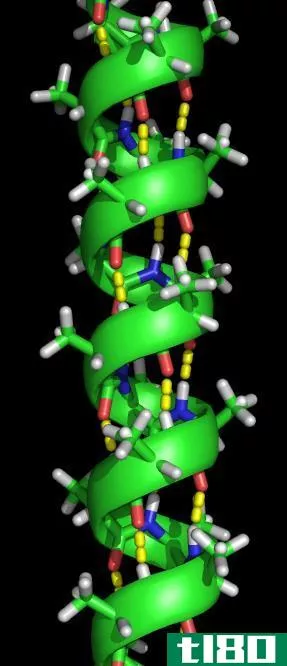
氢键用黄点表示。
贝塔褶皱床单:
当两个或多个多肽链片段相互重叠,形成一排氢键时,可以发现以下结构。它可以通过两种方式发生:平行排列和反平行排列。
结构示例:
α螺旋:指甲或脚趾甲可以作为α螺旋结构的一个例子。
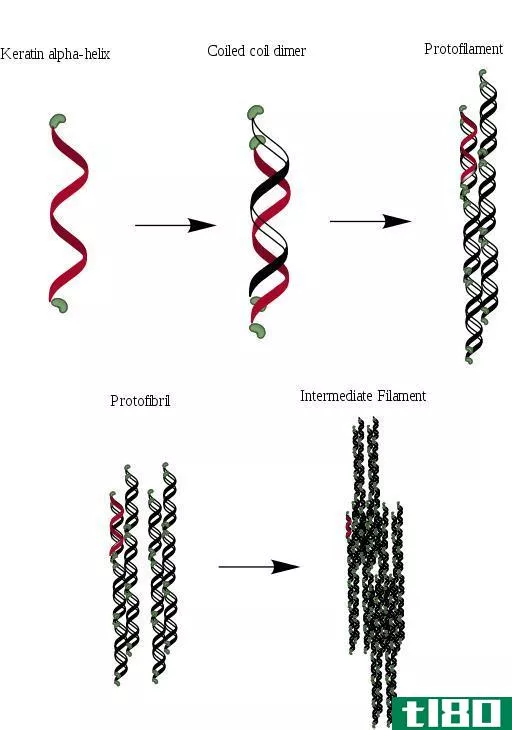
β褶片:羽毛的结构与β褶片的结构相似。
结构特点:
α-螺旋:在α-螺旋结构中,每转一圈有3.6个氨基酸。所有的肽键都是反式的和平面的,并且肽键中的N-H基团指向同一个方向,与螺旋轴大致平行。所有肽键的C=O基团指向相反的方向,它们平行于螺旋轴。每个肽键的C=O基团与肽键的N-H基团结合形成氢键。所有的R-群从螺旋线向外指向。
β折叠片:β折叠片中的每个肽键都是平面的,具有反式构象。相邻链上肽键的C=O和N-H基团在同一平面上,相互指向,在它们之间形成氢键。任何链中的所有R-群可以交替地出现在薄板平面的上方和下方。
定义:
References: “Protein Structure”. ChemWiki: The Dynamic Chemistry Hypertext “Protein Secondary Structure: α-Helices and β-Sheets” . Proteinstructures.com by Salam Al Karadaghi “Organic Chemistry”. The Virtual Cell Textbook “Beta Sheet”.Wikipedia Image Courtesy: “Helix electron density myoglobin 2nrl 17-32” By Dcrjsr – Own work (CC BY 3.0) via Comm*** Wikimedia “Protein secondary structure” by en:User:Bikadi (CC BY-SA 3.0) via Comm*** Wikimedia “1gwe antipar beta Sheet both” by Dcrjsr – Own work (CC BY 3.0) via Comm*** Wikimedia