门捷列夫周期表与现代周期表的关键区别在于,现代周期表的基础主要是元素的电子构型,我们称之为原子序数,而在门捷列夫周期表中,它是元素的原子质量。
让我们看看什么是门捷列夫周期表和什么是现代周期表,然后比较两者以了解门捷列夫周期表和现代周期表的区别。门捷列夫是现代元素周期表的先驱,在对旧版周期表进行了多次修改之后。这两种尝试对科学界同样重要;因为如果不发明元素周期关系,科学的现代发展就不会达到今天这样的发展时代。
目录
1. 概述和主要区别
2. 什么是门捷列夫周期表
3. 什么是现代元素周期表
4. 并列比较——门捷列夫与现代元素周期表的表格形式
5. 摘要
什么是门捷列夫周期表(mendeleev periodic table)?
1869年,俄罗斯化学家门捷列夫(Dmitri mendelev)和德国化学家洛萨·迈耶(Lothar Meyer)提出了一种基于性质周期性递推的周期元素表。1864年,在门捷列夫之前,英国化学家约翰·纽兰兹按照原子质量的顺序排列元素,每八种元素都有相似的性质。他把这种特殊的关系称为“八度律”。然而,我们不能为钙以外的元素制定他的定律。因此,科学界并不接受。

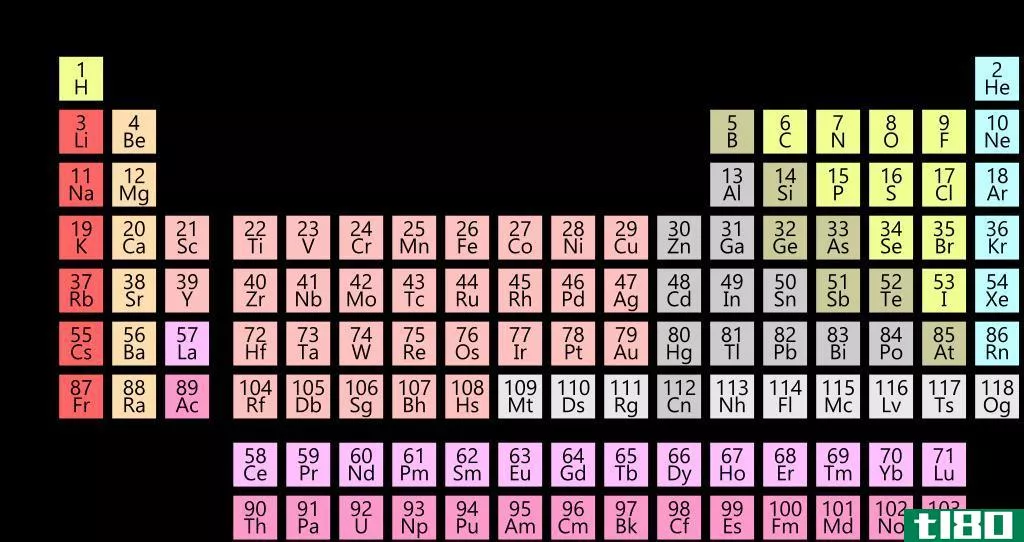
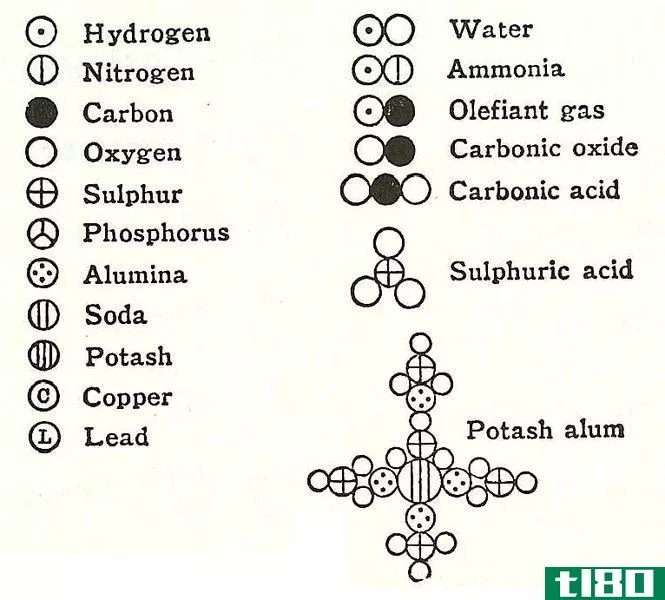
图01:门捷列夫周期表
与纽兰分类法相比,门捷列夫的分类法有了很大的改进,原因有二。第一个因素是,它根据元素的属性更准确地将它们组合在一起。其次,对几种未发现元素的性质进行了可能的预测。例如,门捷列夫提出了一种未知元素eka-aluminum的存在,并预测了它的一些性质。(Eka在梵语中的意思是“第一”。因此,eka铝是铝组中的第一个元素)。当科学家们在四年后发现镓时,它的性质与eka铝的预测特性非常吻合。
因此,提到这些将如下所示:;

在门捷列夫周期表中,有66个元素。到1900年,科学家又增加了30种元素,填补了表中的一些空白。
什么是现代元素周期表(modern periodic table)?
现代元素周期表考虑元素的最外层基态电子组态。根据充满电子的亚壳层的类型,我们可以将元素分为代表性元素、惰性气体、过渡元素(或过渡金属)和锕系元素。代表元素是(我们称之为主群元素)IA到7A中的群,所有元素都不完全填充最高主量子数的s或p子壳层。除了氦(He)之外,所有8A元素都填充了p-subshell。
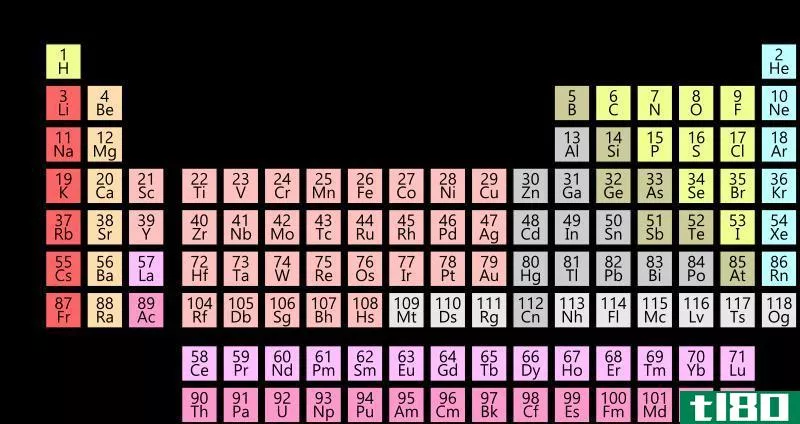
图02:现代元素周期表
过渡金属是1B和3B到8B的元素,其中分子有不完全填充的d-亚壳层。镧系元素和锕系元素有时被称为f块元素,因为这些元素具有不完整的f轨道。
门捷列夫(mendeleev)和现代元素周期表(modern periodic table)的区别
门捷列夫周期表是我们今天使用的现代周期表的基础。它有65个已知元素,但与新发现的元素相比,现代元素周期表中有103个元素。门捷列夫周期表与现代周期表的关键区别在于,现代周期表的基础主要是元素的电子构型,我们称之为原子序数,而门捷列夫周期表考虑元素的原子质量。
下面的信息图表详细列出了门捷列夫和现代元素周期表之间的区别。

总结 - 门捷列夫(mendeleev) vs. 现代元素周期表(modern periodic table)
在现代元素周期表中,化学和物理性质相似的元素以一定的间隔出现,大约有103个元素。当门捷列夫对它们进行分类时,元素周期表中只有66个元素。然而,门捷列夫在元素周期表中为未发现的元素留下了空白。他还假设了元素性质的周期性变化。门捷列夫周期表与现代周期表的关键区别在于,现代周期表的基础主要是元素的电子构型,我们称之为原子序数,而门捷列夫周期表考虑元素的原子质量。
引用
1歌词。“3.1:Mendeleev的元素周期表”,《化学LibreTexts》,LibreTexts,2016年10月14日。可在此处查阅2。“周期表”,维基百科,维基媒体基金会,2018年10月7日。此处提供
2“周期表”,维基百科,维基媒体基金会,2018年10月7日。