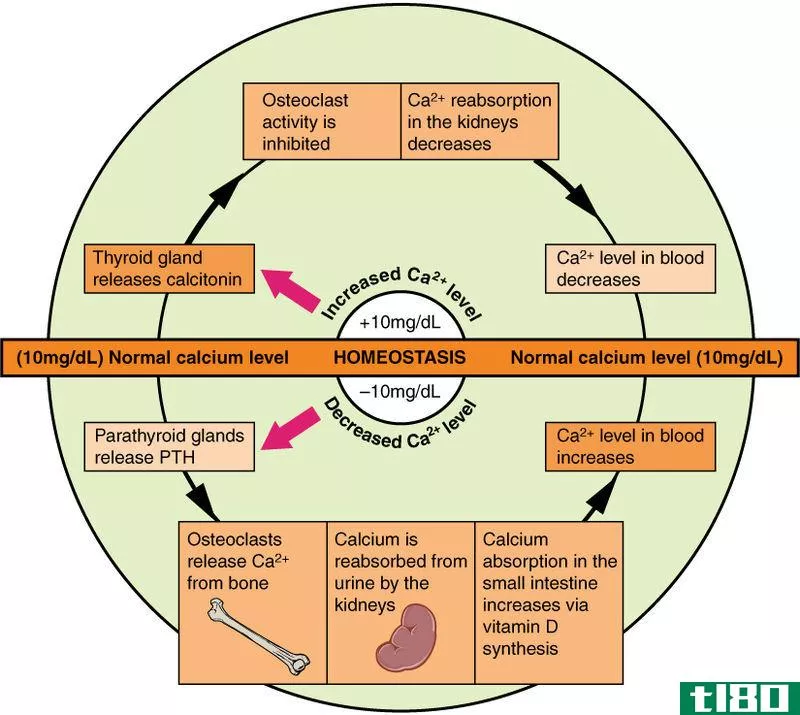
平衡态和稳态的关键区别在于,在平衡状态下,所有组分的浓度保持恒定,而在稳态下,只有一些组分保持恒定。
当一个或多个反应物转化为产物时,它们可能经过不同的改性和能量变化。反应物中的化学键被破坏,形成新的键,生成与反应物完全不同的产物。这就是我们所说的化学反应。平衡态和稳态是不同化学反应的重要化学概念。
目录
1. 概述和主要区别
2. 什么是平衡
3. 什么是稳态
4. 并列比较-平衡与稳态的表格形式
5. 摘要
什么是平衡(equilibrium)?
有些反应是可逆的,有些反应是不可逆的。在反应中,反应物转化为产物。在某些反应中,反应物又从产物中生成。我们称这种反应为可逆反应。在不可逆反应中,一旦反应物转化为产物,它们就不再从产物中再生。
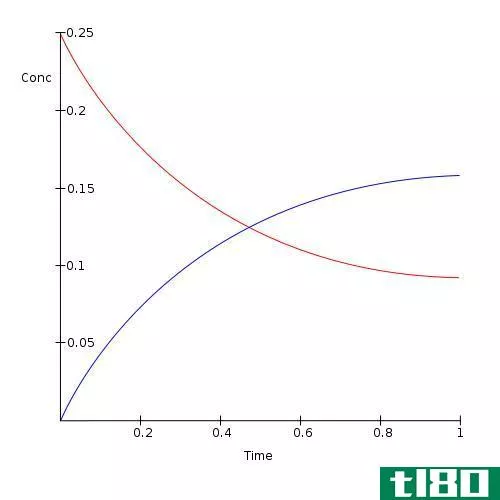
在可逆反应中,当反应物转化为产物时,我们称之为正向反应。当产物转化为反应物时,我们称之为反向反应。当正向和反向反应速率相等时,反应处于平衡状态。因此,反应物和产物的量在一段时间内不会发生变化。
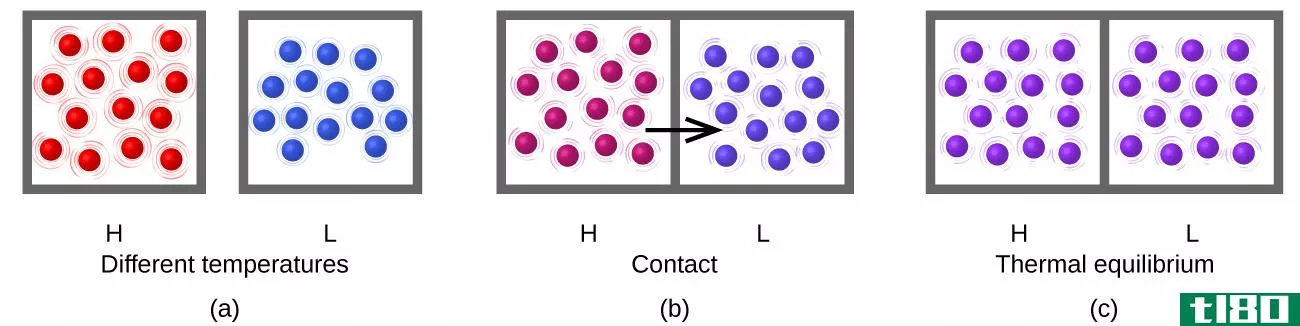
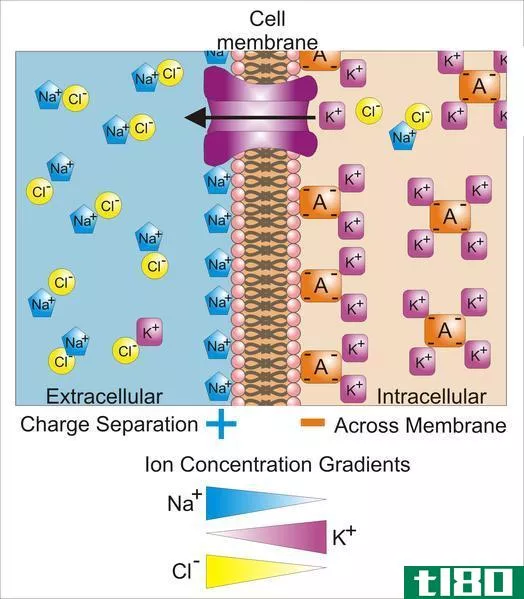
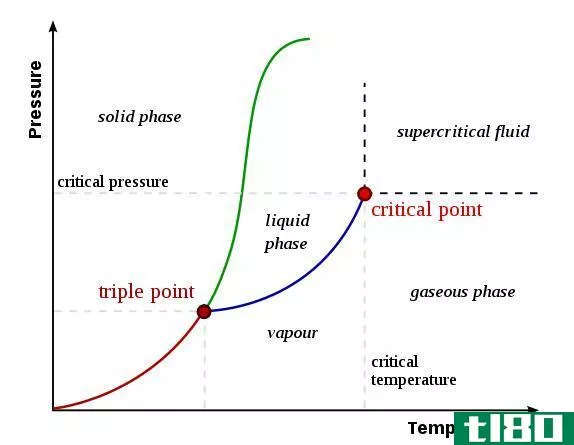
图01:热平衡
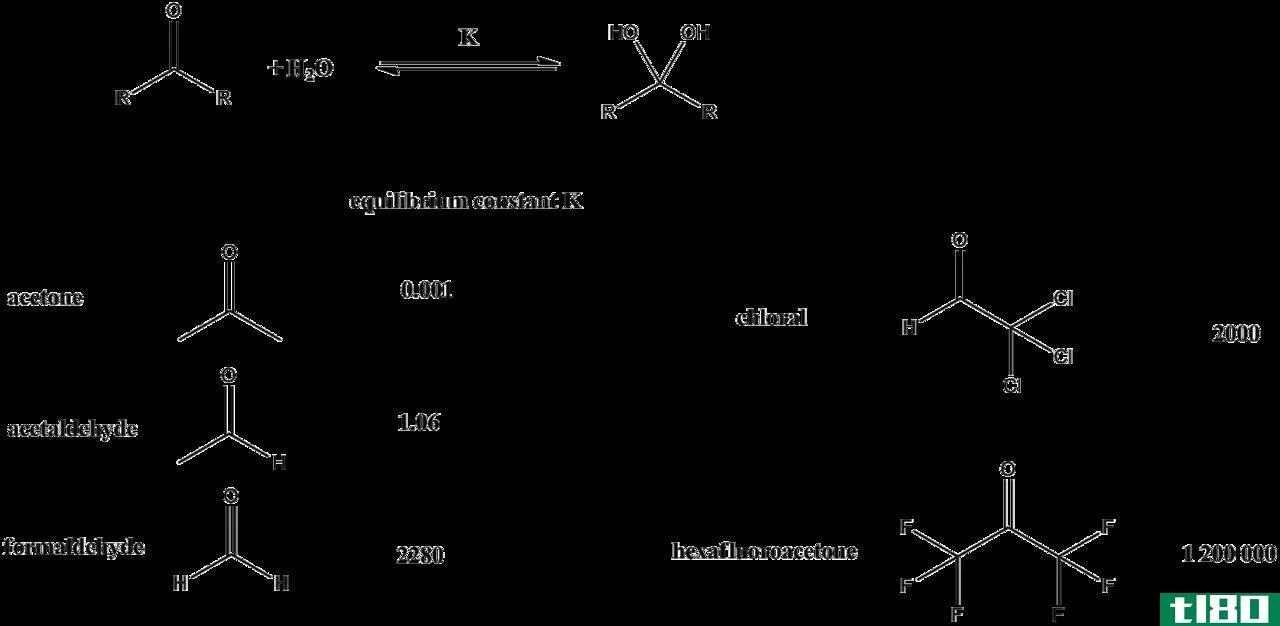
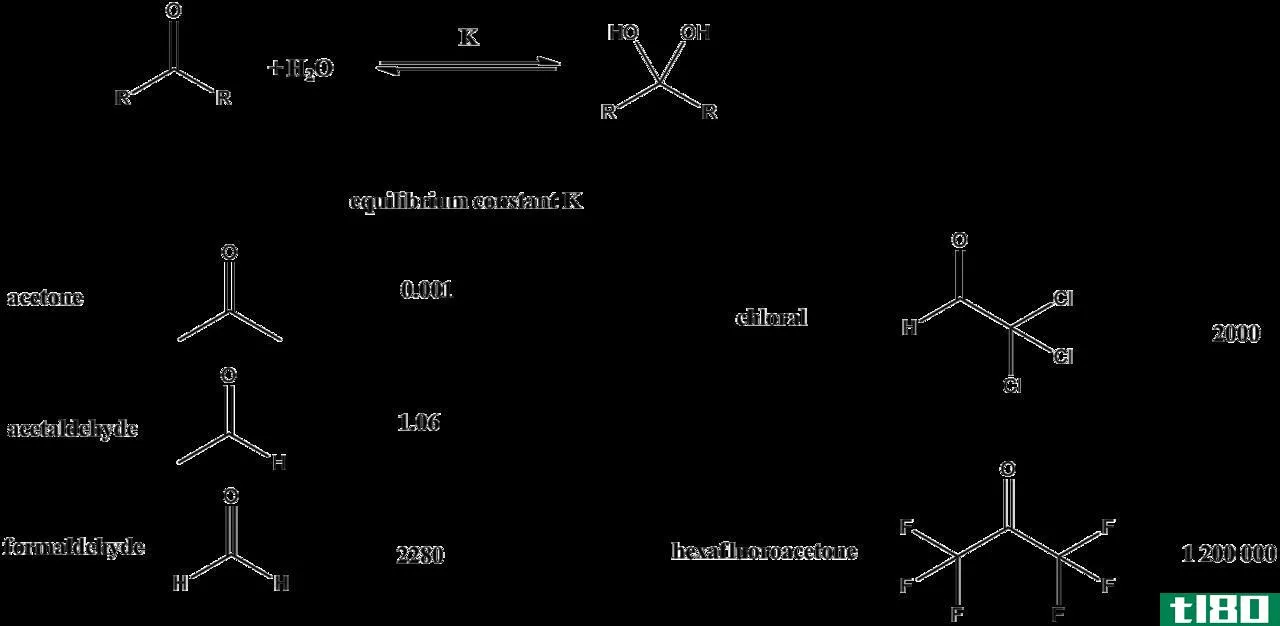
可逆反应总是趋向于平衡并保持平衡。当体系处于平衡状态时,产物和反应物的量不必相等。反应物的数量可能比产物多,反之亦然。平衡方程的唯一要求是,随着时间的推移,两者的量都保持恒定。对于处于平衡状态的反应,我们可以定义一个平衡常数,它等于产物浓度与反应浓度之比。
什么是稳态(steady state)?
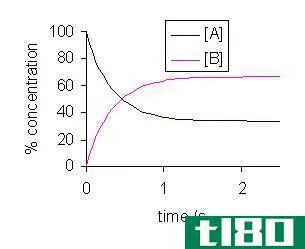
考虑一个反应,反应物a通过中间物B进入产物C。在这样的反应中,B由a形成,然后经过耗尽形成C。在反应开始之前,只有a,B慢慢开始积聚。然而,随着时间的推移,A的量减少了,C的量增加了,但是B的量随着时间的推移大致保持不变。在这种状态下,一旦有更多的B形成,它就会以很快的速度耗尽,以保持稳定的浓度。因此,B的合成速率=B的消耗速率。
A⟶B⟶C
稳态假设:d(B)/dt=0。
平衡(equilibrium)和稳态(steady state)的区别
Equilibrium and steady state are important chemical concepts. The key difference between equilibrium and steady state is that in equilibrium, the concentrati*** of all components are held c***tant whereas, in steady state, only some components are kept c***tant. In equilibrium, the concentrati*** of components are c***tant because the reaction rates are equal in the forward and backward reaction. In steady state, only some components are c***tant because its synthesis rate and c***umption rate are equal. For this, the reacti*** need not necessarily be in equilibrium.
总结 - 平衡(equilibrium) vs. 稳态(steady state)
平衡态和稳态是重要的化学概念。平衡态和稳态的关键区别在于,在平衡状态下,所有组分的浓度保持恒定,而在稳态下,只有一些组分保持恒定。
引用
1.赫尔曼斯汀,安妮·玛丽。“化学反应中的化学平衡”,ThoughtCo,2019年2月3日,可在这里查阅。