平衡常数和速率常数的关键区别在于,平衡常数用反应物和产物的浓度来表示,而速率常数用反应物或产物的浓度来表示。
平衡常数和速率常数都是特定反应的常数。这意味着,在一个恒定的反应中,温度、平衡常数的值和速率常数等条件不会随时间而改变。此外,在表示平衡常数时,还必须考虑化学计量系数。但是,对于速率常数,我们只能用实验方法来确定。
目录
1. 概述和主要区别
2. 什么是平衡常数
3. 什么是速率常数
4. 并列比较-平衡常数与速率常数的表格形式
5. 摘要
什么是平衡常数(equilibrium c***tant)?
平衡常数是平衡时产物浓度与反应物浓度之比。我们只能用在平衡的反应上。对于处于平衡状态的反应,反应商和平衡常数是相同的。
此外,我们必须用化学计量系数的幂次来给出这个常数。平衡常数取决于体系的温度,因为温度影响组分的溶解度和体积膨胀。然而,平衡常数的方程式不包括反应物或产物中固体的任何细节。只考虑液相和气相的物质。
例如,醋酸与醋酸离子的平衡如下:
CH3COOH⇌CH3COO–+H+
该反应的平衡常数Kc如下:
Kc=[CH3COO–][H+]/[CH3COOH]
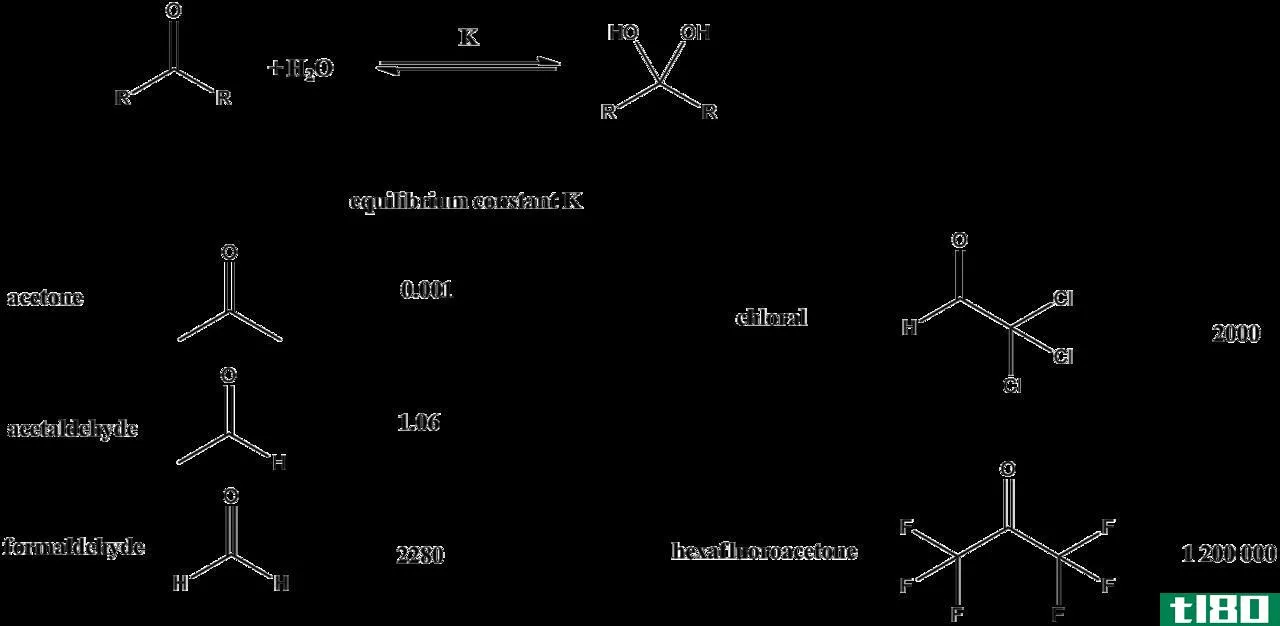
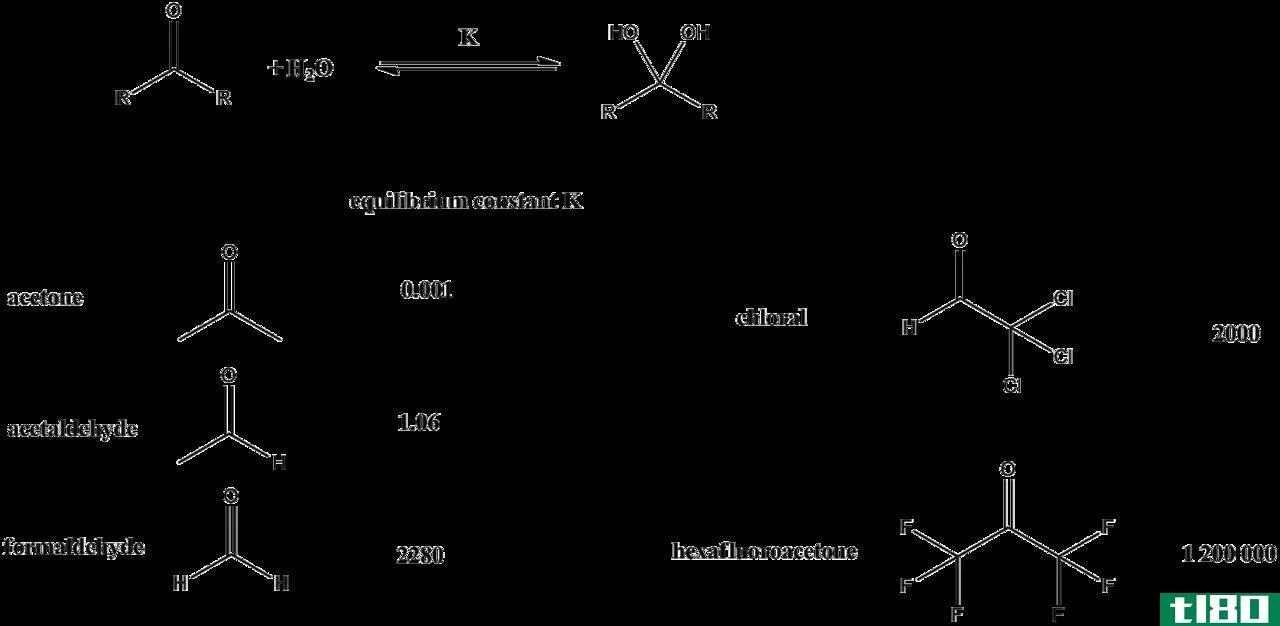
图01:不同化合物的平衡常数
什么是速率常数(rate c***tant)?
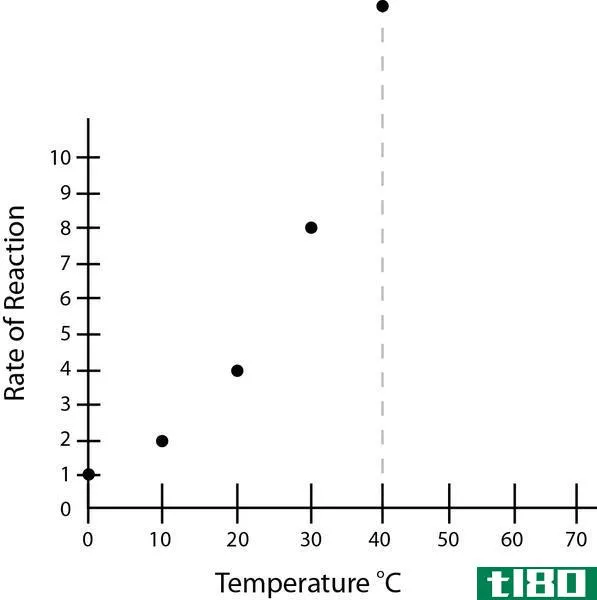
速率常数是一种比例系数,它将给定温度下的化学反应速率与反应物或反应产物的浓度相关联。对于下面给出的反应,如果我们写出反应物A的速率方程,如下所示。
aA+bB⟶cC+dDR=-K[A]A[B]B
在这个反应中,k是速率常数。它是一个比例常数,取决于温度。我们可以通过实验来确定反应的速率和速率常数。
平衡常数(equilibrium c***tant)和速率常数(rate c***tant)的区别
平衡常数和速率常数的关键区别在于,平衡常数用反应物和产物的浓度来表示,而速率常数用反应物或产物的浓度来表示。此外,对于一个平衡反应给出了平衡常数,而对于任何反应都可以给出速率常数。
此外,在表示平衡常数时,我们可以使用反应物和产物的浓度以及化学计量系数,而在表示速率常数时,我们不能使用化学计量系数,因为我们必须通过实验确定常数的值。此外,平衡常数描述的是不变的反应混合物,而速率常数描述的是随时间变化的反应混合物。

总结 - 平衡常数(equilibrium c***tant) vs. 速率常数(rate c***tant)
总之,如果不改变反应条件,如温度,平衡常数和速率常数都不会随时间变化。然而,平衡常数和速率常数的关键区别在于,平衡常数用反应物和产物的浓度来表示,而速率常数用反应物或产物的浓度来表示。
引用
1赫尔曼斯汀,安妮·玛丽。化学中的速率常数是多少?“ThoughtCo,2018年9月27日,可在此处获取。2。“平衡常数,K.”化学剧本,歌词,2019年6月5日,可在这里查阅。
2“平衡常数,K.”化学剧本,歌词,2019年6月5日,